博文
Meatbolites 从降脂到免疫:ApoB100如何开启动脉粥样硬化治疗新时代?
||
提到心血管疾病的元凶,大多数人会立刻想到低密度脂蛋白胆固醇 (LDL-C),即我们常说的“坏胆固醇”。然而,近年来的研究不断揭示,真正在血管壁下驱动动脉粥样硬化进程的关键因素,或许并非LDL-C本身,而是其结构中的核心蛋白——载脂蛋白B100 (ApoB100)。来自希腊雅典伊凡吉利斯莫斯总医院的Natalia G. Vallianou博士团队,近期在 Metabolites 期刊发表了一篇题为《ApoB100与动脉粥样硬化:21世纪的新见解》的重要综述。该文系统地梳理了ApoB100的结构、功能与代谢机制,并深入探讨了其在心血管风险评估与靶向治疗中的新兴价值。本文将为您解读这篇综述的核心内容,一同探索ApoB100的奥秘。
ApoB100是动脉粥样硬化的“核心推手”
ApoB100是肝脏来源的致动脉粥样硬化脂蛋白家族——包括VLDL、IDL、LDL和Lp(a)——共同拥有的核心结构蛋白。每个这样的脂蛋白颗粒中,恰好只含有一个ApoB100分子。这意味着,血液中ApoB100的浓度,直接反映了致动脉粥样硬化颗粒的总数量,堪称“一个颗粒,一个信号”。
图1清晰展示了ApoB100脂蛋白的完整代谢旅程:肝脏首先合成并分泌含有ApoB100的VLDL,随后在脂蛋白脂肪酶 (LPL) 和肝脂肪酶 (HL) 的接力作用下,VLDL逐步代谢为IDL,最终转变为LDL。这些LDL颗粒一部分通过肝脏的LDL受体被清除出血液,完成“回收”;而另一部分则可能被氧化修饰,滞留于血管内膜下,触发炎症反应,吸引巨噬细胞吞噬脂质,最终形成泡沫细胞和动脉粥样硬化斑块。
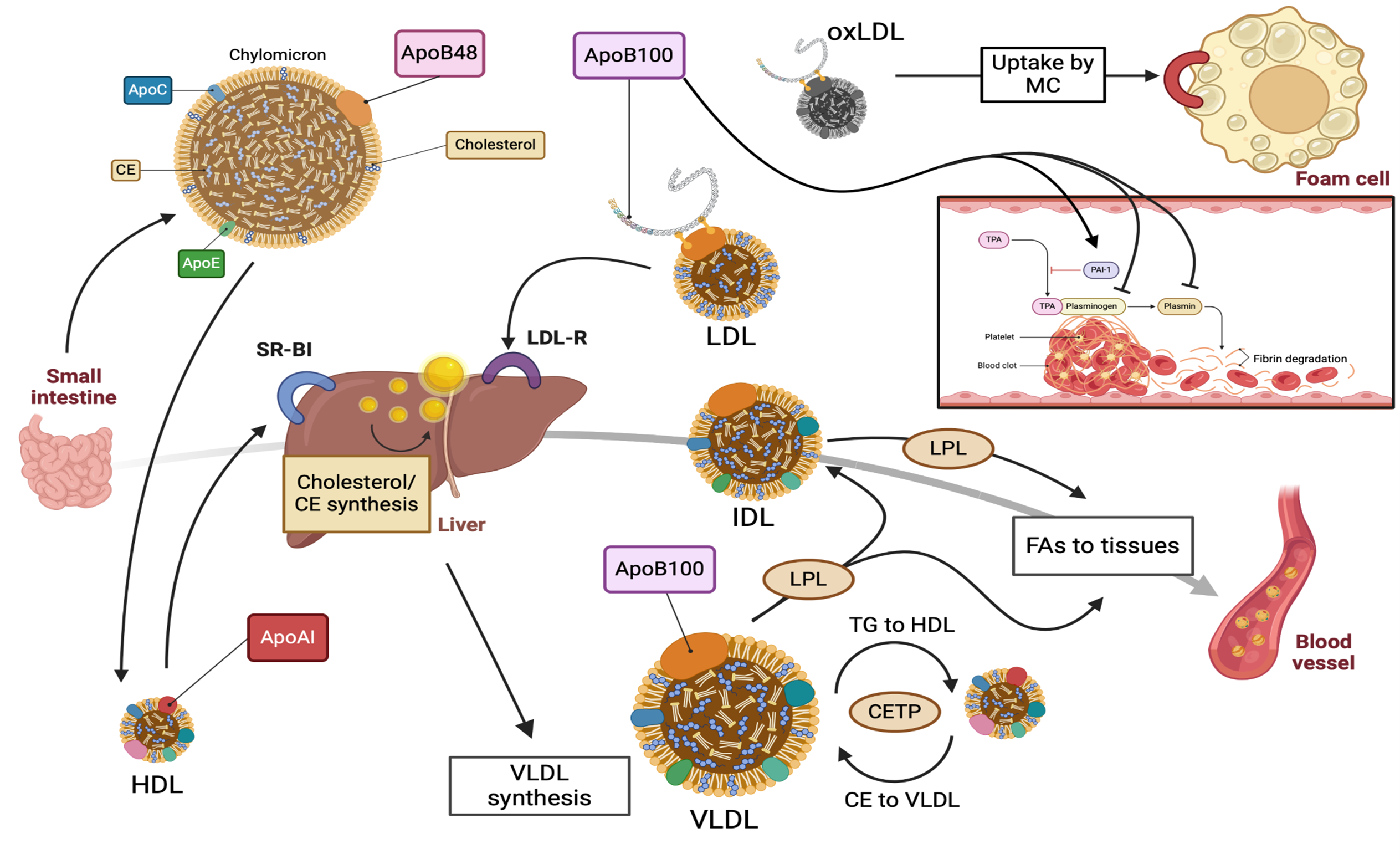
图1:ApoB100脂蛋白的代谢过程
ApoB100如何“点燃”炎症反应?
动脉粥样硬化本质上是一种慢性炎症性疾病,而ApoB100在此过程中扮演着“点火器”的关键角色。具体来说,它通过以下三条途径点燃并维持炎症反应:
首先是氧化修饰。滞留于血管内膜的LDL被氧化为Ox-LDL,这一“变质”的脂蛋白会激活内皮细胞,激活内皮细胞表达黏附分子 (如VCAM-1、ICAM-1),招募单核细胞进入内膜。
其次是免疫激活。进入内膜的单核细胞分化为巨噬细胞,吞噬Ox-LDL后变成泡沫细胞。更值得注意的是,ApoB100本身可作为抗原,被CD4+ T细胞识别,从而激活适应性免疫,诱发Th1型炎症反应,让局部炎症进一步升级。
最后是炎症通路的放大。Ox-LDL还能激活NLRP3炎症小体,促进IL-1β等炎症因子的释放,形成一个正向反馈循环,进一步加剧斑块的不稳定性。
图2系统总结了上述分子机制,从脂蛋白滞留、氧化修饰、炎症细胞招募到斑块形成,全景式展示了动脉粥样硬化的演进过程。
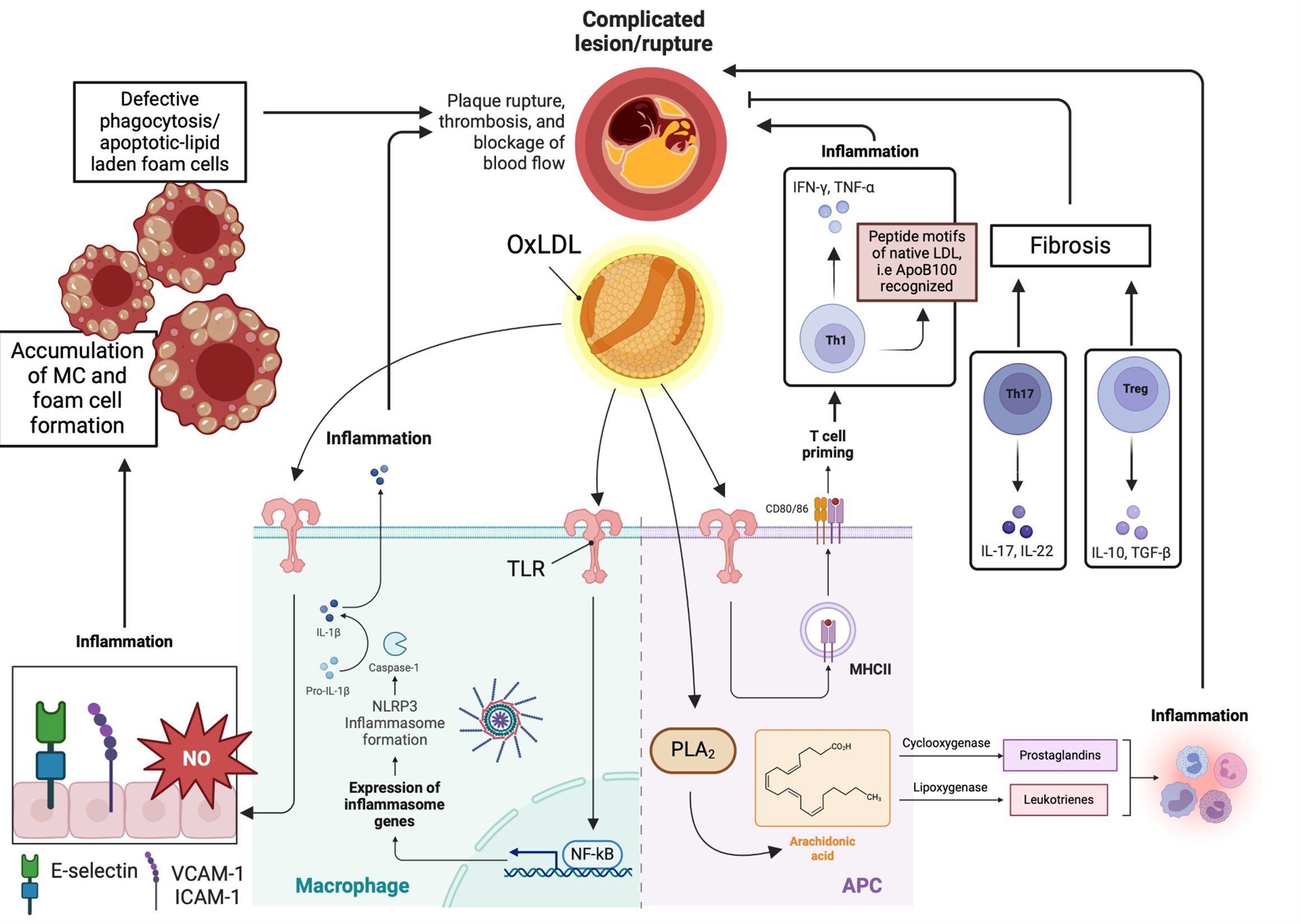
图2:动脉粥样硬化的分子机制
ApoB100是超越LDL-C的“心血管风险预测新星”
长期以来,LDL-C一直被奉为评估心血管风险的“金标准”。但近年来,越来越多的研究开始挑战这一认知,ApoB100在风险预测方面的优势日益凸显。
首先,ApoB100反映的是颗粒数量,而非仅仅胆固醇含量。每个致动脉粥样硬化脂蛋白颗粒都有且只有一个ApoB100分子,因此ApoB100的浓度直接等同于血液中“坏颗粒”的总数。这一点在代谢综合征、糖尿病、高甘油三酯血症患者中尤为关键——这些患者体内小而密LDL(sd-LDL)颗粒增多,每个颗粒携带的胆固醇较少,但致动脉粥样硬化能力却更强。如果只看LDL-C,可能会低估风险,而ApoB100则能精准捕捉到这些“小而凶悍”的颗粒。
此外,还有临床数据的支持。著名的AMORIS研究证实,在预测致死性心肌梗死方面,ApoB100的表现优于传统LDL-C。而Marston等人的研究更进一步指出:无论脂蛋白类型或脂质含量如何,ApoB100水平与心肌梗死风险的关联都是最密切的,换句话说,重要的不只是脂蛋白里装了多少胆固醇,而是有多少个脂蛋白颗粒。
ApoB100基因突变与疾病
ApoB100由APOB基因编码,其突变可导致两种截然不同的临床表型。
一种是“功能丧失型”突变:家族性载脂蛋白B100缺陷 (FDB)。以经典的R3500Q位点突变为例,它会导致ApoB100与LDL受体结合能力下降,使得LDL无法被肝脏有效清除,只能滞留在血液中。表现为高胆固醇血症和早发动脉粥样硬化。另一种是“生产不足型”突变:家族性低β脂蛋白血症 (FHBL)。这类突变多为APOB基因的截短突变,导致ApoB100合成量大幅减少。表现为极低的LDL-C水平,通常对心血管具有保护作用,但可能伴随肝脂肪变性。
ApoB100作为治疗靶点:从传统药物到新兴疗法
随着对ApoB100认识的深入,它已成为降脂治疗的重要靶点。从传统药物到新型生物制剂,各类药物通过不同环节干预ApoB100脂蛋白的代谢。
传统药物:他汀类药物通过上调LDL受体,加速ApoB100脂蛋白从血液中清除;依折麦布则从源头上抑制肠道胆固醇吸收,间接促进ApoB100脂蛋白的分解代谢;而贝特类药物通过激活PPAR-α,增强VLDL-ApoB100的清除,尤其适合高甘油三酯血症患者。
新型生物制剂精准打击:
1) PCSK9抑制剂 (依洛尤单抗、阿利西尤单抗):通过阻断PCSK9与LDL受体的结合,增加LDL受体数量,从而大幅增加LDL-C和ApoB100的清除效率;
2) ANGPTL3抑制剂 (埃维那单抗):通过激活脂蛋白脂肪酶 (LPL) 和内皮脂肪酶 (EL),加速ApoB100脂蛋白的分解代谢,为难治性高胆固醇血症提供了新武器;
3) CETP抑制剂 (obicetrapib):通过抑制胆固醇酯转移蛋白,改变脂蛋白间的脂质交换,从而降低ApoB100水平,目前正处于临床试验阶段;
4) ApoB100合成抑制剂 (米泊美生):这是一种反义寡核苷酸药物,直接抑制ApoB100的合成,主要用于纯合子家族性高胆固醇血症。
免疫调节与ApoB100疫苗
近年来,ApoB100作为动脉粥样硬化免疫治疗靶点的潜力日益凸显。研究发现,ApoB100经氧化修饰后可产生特异性抗原表位 (如p210),激活T细胞免疫反应。这一发现为“主动免疫治疗”铺平了道路。基于此,研究者正在探索ApoB100疫苗,并取得初步进展。
1) p210肽疫苗:在动物模型中成功诱导调节性T细胞应答,显著减少动脉粥样硬化斑块面积。
2) 鼻黏膜免疫:将ApoB100肽与霍乱毒素B亚单位融合,经鼻黏膜免疫可诱导抗原特异性调节性T细胞,显著减轻主动脉病变。
这些研究为动脉粥样硬化的防治开辟了全新方向,从被动降脂走向主动免疫调控,未来可期。
研究总结
作者总结指出,ApoB100不仅是致动脉粥样硬化脂蛋白的核心结构蛋白,更是连接脂代谢、炎症与免疫反应的关键分子。相较于传统LDL-C指标,ApoB100在心血管风险评估中展现出更高的敏感性和准确性。随着PCSK9抑制剂、ANGPTL3抑制剂等新型药物的问世,以及ApoB100疫苗等免疫疗法的探索,我们正迎来一个更加精准、个性化的心血管疾病防治新时代。未来,ApoB100有望成为临床实践中不可或缺的“心血管健康坐标”,助力更多患者远离动脉粥样硬化的威胁。
阅读英文原文:https://www.mdpi.com/2218-1989/14/2/123
Metabolites 期刊介绍
主编:Amedeo Lonardo, Azienda Ospedaliero-Universitaria, Italy
Metabolites (ISSN 2218-1989) 是一本国际同行评审的代谢和代谢组学开放获取期刊。期刊致力于为研究代谢物与代谢相关的学者提供一个快速发表的平台,内容涵盖代谢组学、代谢生物化学、计算和系统生物学、生物技术和医学领域相关的代谢物以及代谢方面的研究。期刊在Web of Science Journal Citation Reports数据库的Biochemistry and Molecular Biology分区中为 2 区。期刊5年 IF 为4.1。
2024 Impact Factor:3.7
2024 CiteScore:6.9
Time to First Decision:17 Days
Acceptance to Publication:3.6 Days
期刊主页:https://www.mdpi.com/journal/metabolites

https://blog.sciencenet.cn/blog-3516770-1530144.html
上一篇:Lubricants 中国矿业大学朱少禹博士和合肥工业大学孙军教授主持特刊:轴承润滑的多物理场建模
下一篇:解答用户常见问题,助力科研探索 | MDPI 答疑周报