博文
Biomolecules:纳米递送技术——mRNA疫苗的研究新方向
||
新冠疫情让mRNA疫苗这一项生物技术被人们广泛熟知。但很多人并不知道,mRNA疫苗真正的核心难题,并不在mRNA本身,而在于如何把它安全、稳定、精准地送进人体细胞。近日发表于 Biomolecules 的综述文章“Revolutionizing mRNA Vaccines Through Innovative Formulation and Delivery Strategies”,系统梳理了当前mRNA疫苗递送领域的最新进展,从脂质纳米颗粒 (LNP) 到DNA纳米结构,全面展示了一场正在发生的“递送技术革命”。
mRNA递送
mRNA作为一种天然存在的遗传物质,理论上安全、可编程、生产速度快,是理想的疫苗和治疗工具。但在真实的生物环境中,mRNA极易被体内核酸酶降解,并且因为难以穿越细胞膜,易聚集或失活,还会因为免疫激活过强反而影响翻译效率。正因如此,单独注射mRNA几乎无法产生有效免疫反应。真正让mRNA疫苗走向成功的关键,是一整套递送系统——递送载体。
mRNA递送载体
脂质纳米颗粒 (LNPs)
LNPs通常由四部分组成:可离子化阳离子脂质、胆固醇、磷脂和PEG-脂质LNPs可以将mRNA包裹其中,保护其不被降解,并通过内吞作用进入细胞。在内体酸性环境下,脂质电荷发生变化,促使mRNA释放到细胞质中完成蛋白翻译。研究指出,通过化学结构优化和免疫佐剂整合,LNP不仅能提升递送效率,还能精准调控免疫强度。
聚合物纳米颗粒
聚合物载体具有高度可设计性,可通过调节分子结构实现更长效、更靶向的递送。如聚β-氨基酯 (PBAE) 可显著提升mRNA表达效率;可吸入聚合物纳米颗粒,为呼吸道疫苗和肺部疾病提供新思路;经过特殊设计的聚合物纳米载体可靶向树突状细胞,增强抗肿瘤免疫。
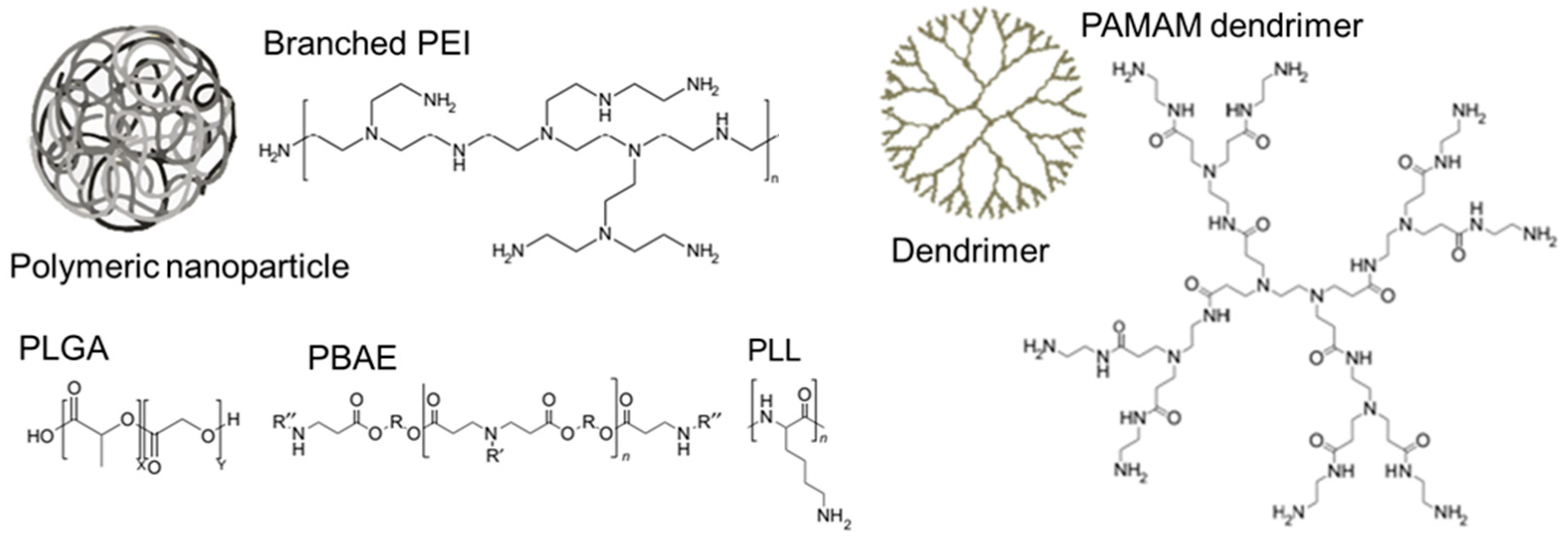
聚合物纳米颗粒和树枝状大分子结构
树枝状大分子纳米颗粒
树枝状分子具有高度分支结构,能高效结合mRNA并促进精确递送。通过表面修饰,可在递送效率与细胞毒性之间取得平衡,在癌症疫苗和基因治疗中前景广阔。
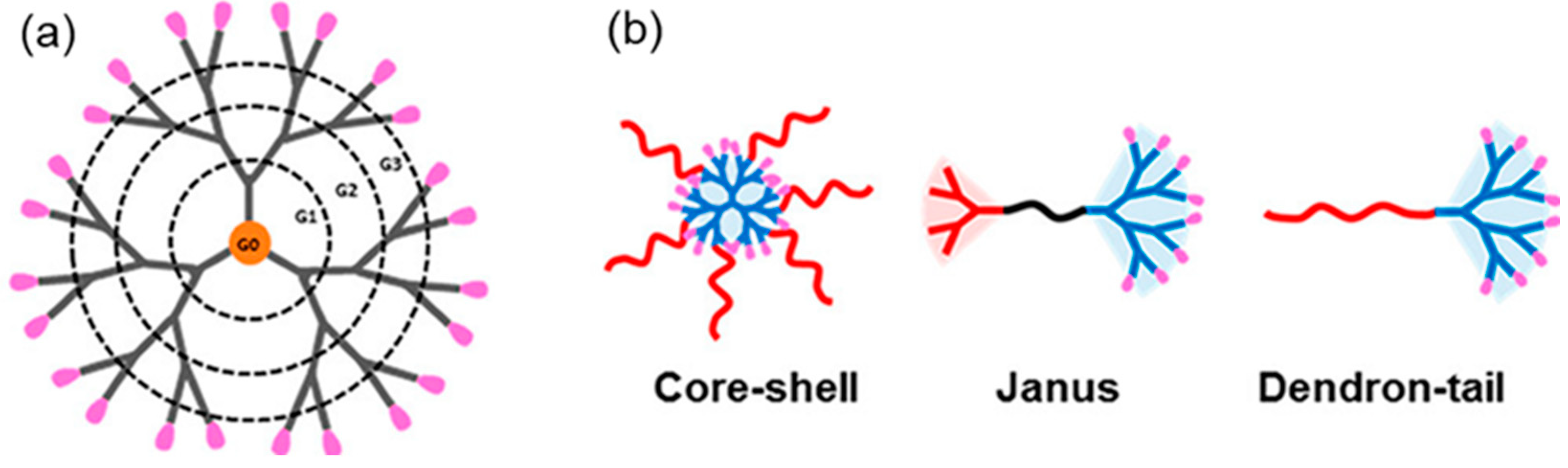
树枝状大分子的示意图
多糖基纳米颗粒
天然来源的壳聚糖、透明质酸、多肽等多糖材料经过改造产生的纳米颗粒,因其良好生物相容性和免疫调节特性备受关注,这类载体尤其适合黏膜系统给药。
肽基纳米颗粒
肽分子和纳米颗粒可通过自组装形成复合物保护mRNA,促进细胞摄取和细胞内递送。这些纳米颗粒的一个优势是能够针对特定靶向进行定制,通过调整氨基酸的组成,可以整合多样功能以改善 mRNA 的递送,实现器官特异性递送。
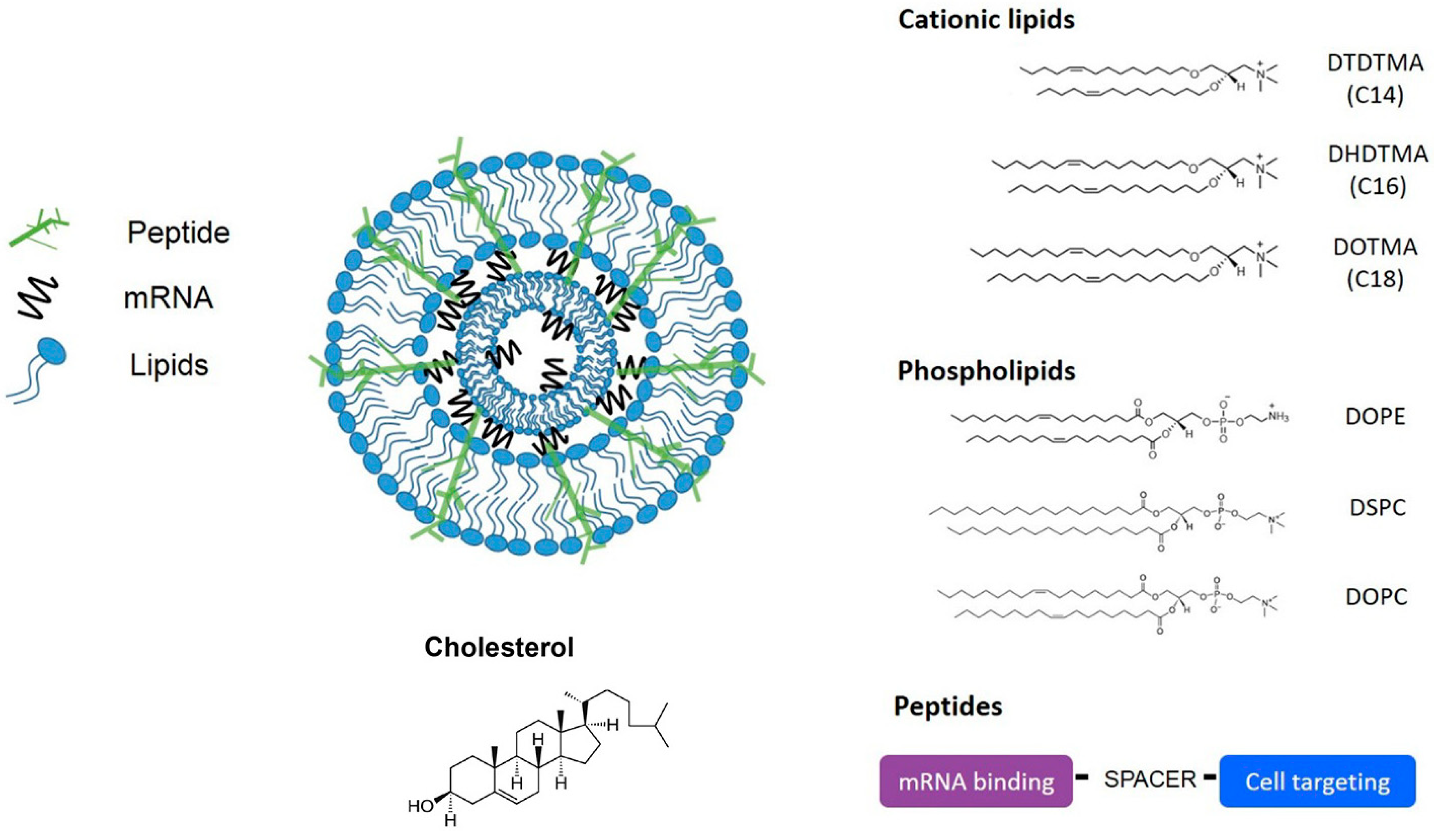
mRNA 疫苗递送中脂肽纳米复合物的结构
其他纳米颗粒
碳基与金属纳米材料:通过碳纳米管、金属-酚网络等新材料与纳米颗粒结合而成,显示出良好mRNA保护与递送潜力。DNA纳米结构:利用DNA自组装技术构建精准载体,具备pH响应释放能力。杂化纳米颗粒:融合了脂质与聚合物优势,提高稳定性和负载效率。脂质体和细胞外囊泡:具备天然递送能力,生物相容性极佳,这些颗粒提高了 mRNA 递送的有效性,显著提升了细胞摄取和转染率。
面临挑战与发展方向
尽管技术不断进步,mRNA递送仍面临以下核心挑战。
储存与运输:多数mRNA疫苗需-20°C至-80°C保存,限制了其全球可及性。冻干技术是重要发展方向;
免疫毒性:部分载体可能引发非特异免疫反应或自身免疫问题;
靶向精度:如何实现器官/细胞特异性递送,减少脱靶效应;
临床转化:从实验室到临床,需克服规模化生产、质控与监管审批等复杂环节。
未来mRNA递送系统将朝着以下方向发展。
刺激响应型载体:实现pH、温度、酶触发释放;
非侵入递送路径:口服、鼻喷等途径提升接种可接受度;
长效稳定保存:通过冻干、载体修饰实现常温储存。
结语
总之,mRNA疫苗递送技术的进展显著提升了治疗效果,纳米载体在确保疫苗安全传递至靶细胞方面发挥了重要作用。尽管取得了显著成果,仍面临免疫优化、毒性降低和冷链存储等挑战。未来,通过合理的修饰和刺激响应型纳米载体的开发,能够进一步提升mRNA的递送效率,减少副作用和毒性风险。随着研究的深入,纳米载体在mRNA治疗中的潜力将继续拓展,为疫苗和基因治疗带来更多突破。
阅读英文原文:https://www.mdpi.com/2218-273X/15/3/359
Biomolecules 期刊介绍
主编:Lukasz Kurgan, Virginia Commonwealth University, USA; Peter E. Nielsen, University of Copenhagen, Denmark
期刊研究范围涉及化学、生物学、分子医学和材料科学之间的交叉学科,重点关注生物活性和生物源物质的结构和功能、具有生物和医学意义的分子机制以及生物材料及其应用。已被Scopus、SCIE (Web of Science)、PubMed等数据库收录。
2024 Impact Factor:4.8
2024 CiteScore:9.2
Time to First Decision:17.9 Days
Acceptance to Publication:2.9 Days
期刊主页:https://www.mdpi.com/journal/biomolecules

https://blog.sciencenet.cn/blog-3516770-1527167.html
上一篇:Veterinary Sciences:螺旋藻补充剂对提高蛋鸡生产性能、鸡蛋品质、保质期和血液生化指标的影响
下一篇:Agriculture华南农业大学农学院的莫钊文副教授创建特刊:粮食作物对施肥和保护性耕作的响应——第二卷