博文
Viruses:从Pandemic Response Box中筛选宿主导向的广谱抗哺乳动物沙粒病毒化合物
||
研究背景
哺乳动物沙粒病毒属 (Mammarenaviruses, MaAv) 是一类具有双节段负链RNA基因组的包膜病毒,会在其天然啮齿动物宿主中引起持续性感染的病毒,并通过人畜共患事件导致人类严重疾病。例如,西非的拉沙病毒 (LASV) 和阿根廷的胡宁病毒 (JUNV) 均可引起高死亡率的出血热。此外,全球分布的淋巴细胞性脉络丛脑膜炎病毒 (LCMV) 是一种未被充分认识但具有重要临床意义的人类病原体,可在新生儿和免疫缺陷个体中引起严重感染。尽管对人类健康构成威胁,但目前尚无美国FDA批准的MaAv疫苗或特异性抗病毒疗法。现有的疗法仅限于利巴韦林的超适应症用药,其疗效仍存争议,其它广谱聚合酶抑制剂如法匹拉韦对拉沙病毒的效力也有限。因此,开发广谱抗病毒药物以对抗MaAv至关重要。
药物再利用策略可显著缩短候选抗病毒药物进入临床所需的时间和资源,并可以为病毒生物学提供宝贵见解。本研究旨在从日内瓦疟疾药品创投组织 (MMV) 和被忽视疾病药物研发倡议组织 (DNDi) 共同构建的“Pandemic Response Box”(PRB) 中进行筛选,该资源库包含400余种具有抗菌及抗病毒活性化合物,以发现对MaAv有效的宿主导向抗病毒药物。
研究内容
1. PRB化合物库的高通量筛选与验证
为从PRB中识别潜在的抗MaAv化合物,作者建立了一种基于细胞感染的高通量筛选方法:使用携带GFP-P2A-NP报告基因的重组LCMV(rLCMV/GFP)感染A549细胞后,通过检测GFP信号和细胞活力,初步筛选出22个阳性化合物 (条件:感染抑制率≥50%,细胞毒性≤20%)。经过重复实验确定了三种对LCMV复制具有强效抑制作用的化合物:Ro-24-7429(RO)、WO 2006118607 A2 (WO) 和verdinexor (VE)。
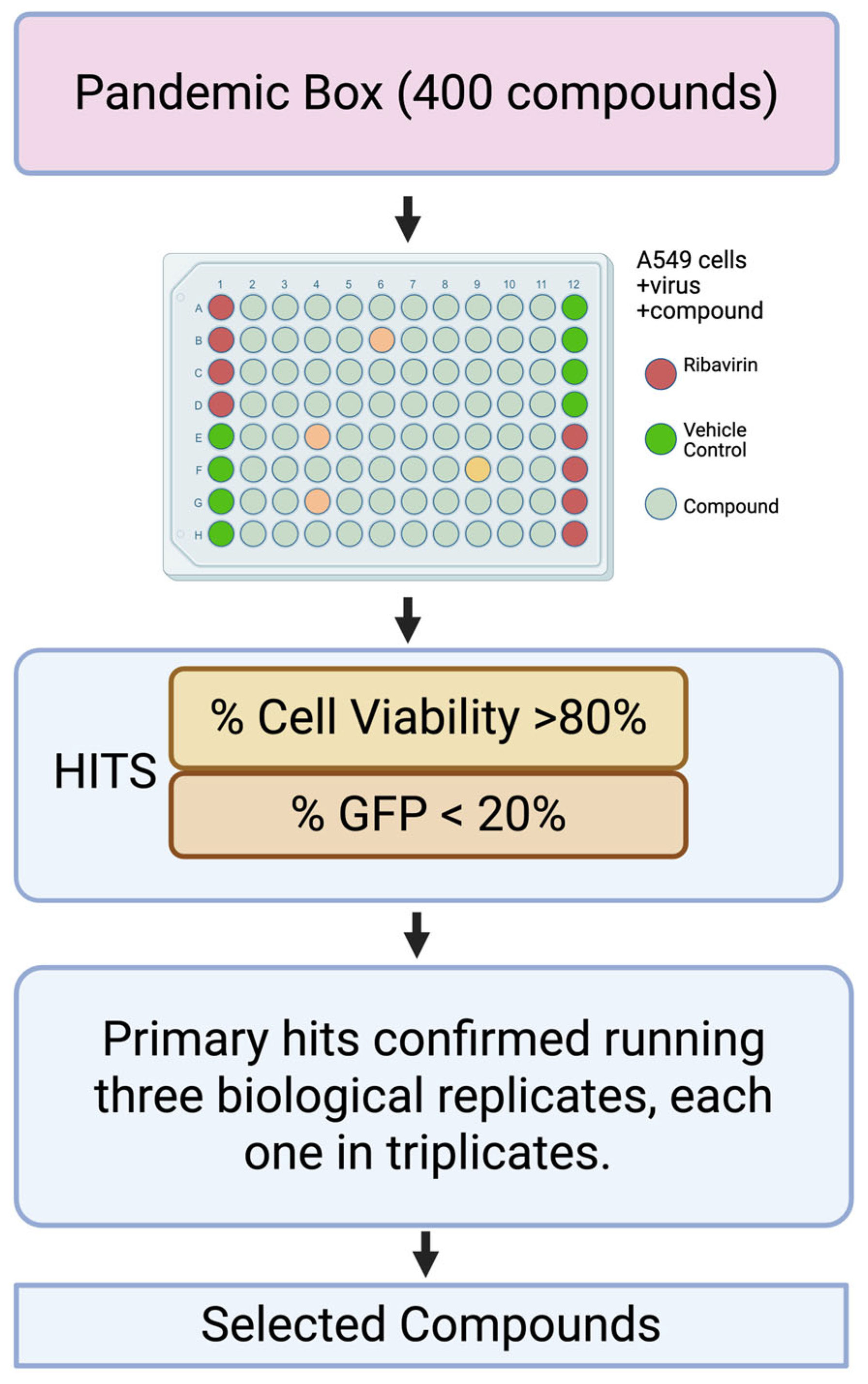
图1. 筛选流程图
为了进一步评估这三种化合物对MaAv的广谱抗病毒活性,除了LCMV以外作者还测定了它们对遗传距离较远的JUNV 的有效性。在rLCMV/GFP和 rJUNV/GFP 感染细胞后分别用候选药物的三倍系列稀释对细胞进行处理。发现化合物 VE、RO 和 WO 在不同浓度下均表现出有效的抗LCMV活性且细胞毒性较低;VE和WO对JUNV同样表现出强效抑制活性,而RO的活性较弱。这表明VE和WO具有更广谱的抗MaAv潜力。
2. 作用机制探究
通过加药时间点实验对三种化合物的作用阶段进行检验。发现VE、RO和WO在感染前2小时或感染后2小时添加均能抑制病毒报告基因表达 (图 2A),表明它们作用于病毒进入细胞后的阶段。再利用基于细胞的LCMV和LASV微型基因组(MG)报告系统评估化合物对病毒核糖核蛋白复合体 (vRNP,负责病毒RNA合成) 活性的影响。结果显示,VE和WO能强效抑制LCMV和LASV的MG活性,而RO的抑制效率较低 (图 2B和2C)。接着通过基于Gaussia荧光素酶 (GLuc) 的报告系统评估化合物对病毒基质Z蛋白介导的出芽过程的影响。结果显示,VE和WO能显著抑制LCMV Z蛋白的出芽效率,而RO没有显著效应 (图 2D和2E)。
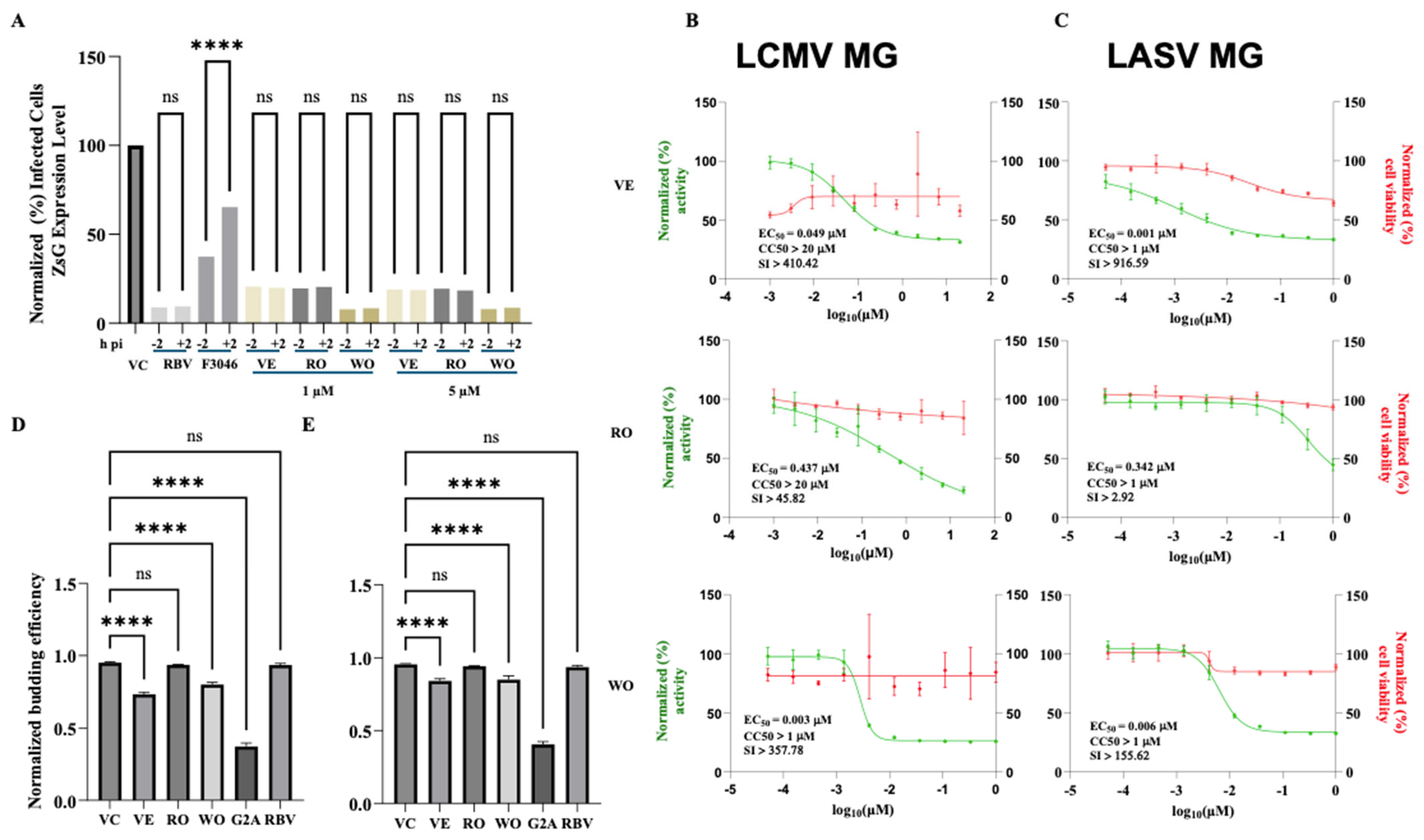
图2. 所选化合物对LCMV生命周期不同环节的影响
VE是一种靶向核输出蛋白XPO1/CRM1的选择性抑制剂,已被证明对甲型流感病毒 (IAV) 和呼吸道合胞病毒 (RSV) 具有抗病毒活性。为了进一步确定作用靶点,作者通过siRNA敲低A549细胞中的XPO1基因,模拟了VE的作用。结果显著减少了LCMV感染性子代病毒的产生,证实了VE是通过靶向XPO1发挥抗MaAv活性。此外,干扰素 (IFN) 反应并非VE抗LCMV活性的主要贡献者。
3. 协同抗病毒效应评估
为探索联合疗法的潜力,作者采用零相互作用效力 (ZIP) 模型评估了VE与WO或RO联合使用的协同效应。结果显示,VE与WO联合使用时表现出强烈的协同抗病毒活性,其中在0.11 μM (VE) 和0.0003 μM (WO) 的浓度下观察到最高的协同评分。相比之下,VE与RO的联合仅表现出微弱的协同效应。这表明VE与WO的联合疗法具有开发价值,可能有助于降低各自用药剂量、减少潜在副作用并提高耐药屏障。
作者介绍
本研究由尼日利亚纳姆迪·阿齐基韦大学医学微生物学与公共卫生系的Chinedu A. Ofodile、美国斯克里普斯研究所免疫学与微生物学系的Beatrice Cubitt以及同系的Juan C. de la Torre教授 (通讯作者) 等多个团队合作完成。研究获得了美国国立卫生研究院国家过敏和传染病研究所 (NIH/NIAID) 的资助。
阅读英文原文:https://www.mdpi.com/1999-4915/18/1/103
Viruses 期刊介绍
主编:Eric O. Freed, Center for Cancer Research, USA
涵盖人类病毒和病毒疾病,动物病毒,植物病毒,病毒免疫、疫苗和抗病毒药物以及朊病毒等各方面研究,目前已被SCIE (Web of Science)、MEDLINE (PubMed) 等数据库收录。
2024 Impact Factor:3.5
2024 CiteScore:7.7
Time to First Decision:17.2 Days
Acceptance to Publication:2.7 Days
期刊主页:https://www.mdpi.com/journal/viruses

https://blog.sciencenet.cn/blog-3516770-1526096.html
上一篇:Pathogens文献清单:2025年精选封面文章
下一篇:Animals 中国水产科学研究院珠江研究所田晶晶老师主持特刊:鱼类的脂质消化和脂肪酸吸收机制
