博文
北京航空航天大学李彬等综述:从电化学视角看水系锌金属负极  精选
精选
|
研究背景
水溶液锌离子(AZIB)电池因其电解质的不燃性、环保性和经济性,以及金属锌与水溶液电解质良好的相容性,成为高安全性、低成本储能系统的理想选择。然而,水溶液电解质作为电池的重要组成部分,会直接或间接的与锌负极相互作用,引起析氢反应、电极钝化和锌枝晶生长等寄生反应,导致AZIB的库仑效率差、使用寿命短。为了抑制或减轻AZIBs中的这些寄生反应,人们进行了许多研究来平衡水性电解质的优点和缺点。这些研究方法主要可以分为两类,一种方法通过增强AZIB中电解质和锌阳极的固有热力学稳定性,例如通过使用盐包水电解质,将水簇(网络水和通过氢键连接的水分子)转化为阳离子的溶剂鞘,进而调节水分子的配位环境来增强水分子中的O-H键。另一种方法是通过降低前驱体(如H₂O和阴离子)与电极之间的接触(或碰撞)频率来减少寄生反应的动态过程。从动力学的角度来看,调节电解质/电极界面以通过吸附剂和人工(或衍生)固体电解质界面(SEI)来阻断活性位点可以有效地最小化寄生反应。
本篇综述全面总结了近些年来AZIB的相关研究,深入揭示了水溶液锌离子电池中水溶液电解质化学、锌阳极寄生反应和体系储能的机理及其关系,从增强电解质与锌阳极的热力学稳定性和降低锌/电解质界面处的寄生反应动力学的角度,阐述了抑制水溶液锌离子电池中寄生反应的策略,展望了锌电解质、锌阳极和锌/电解质界面的未来发展方向。
An Electrochemical Perspective of Aqueous Zinc Metal Anode
Huibo Yan, Songmei Li, Jinyan Zhong*, Bin Li*
Nano-Micro Letters (2024)16: 15
https://doi.org/10.1007/s40820-023-01227-x
本文亮点
1. 对水溶液锌离子电池中的水溶液电解质化学、寄生反应化学和储能化学及其相互关系进行了详细的讨论和总结。
2. 从热力学角度综述了近年来提高电解液和锌阳极固有稳定性以抑制寄生反应的研究进展。
3. 从动力学角度综述了吸附剂和固体电解质界面对电解质/电极界面阻断寄生反应的调控策略。
内容简介
随着对安全、无毒、低成本、长循环寿命以及高能量和功率密度的储能系统的需求,水溶液电池逐渐成为研究的焦点。锌金属具有较小的离子半径及相对较低的氧化还原电位(-0.76V vs SHE),锌阳极制造成本低,水溶液锌离子电池安全性高、可匹配多种阴极材料使用,因而成为最具潜力的水溶性金属电池。尽管AZIBs具有很好的前景,但其工作过程中会发生不可控的寄生反应,包括锌枝晶、钝化、析氢和阳极侧腐蚀,影响了AZIB的循环性能,阻碍了其大规模使用。这些反应是由水分子和锌阳极直接或间接引起的。通过对电解液成分进行改性、对电解质/电极界面进行调控、对锌负极进行修饰改性等手段,可以有效抑制水溶液电解质与锌阳极之间的寄生反应,进而提升AZIB的循环性能。北京航空航天大学李彬等详细分析了AZIB工作过程中水溶液电解质化学、寄生反应化学和储能化学的机理及其相互关系,从提高电解液和锌阳极的热力学稳定性和改善电解质/电极界面动力学两个角度分析了现有措施对AZIB的调控策略,为未来AZIB的发展提供了理论指导。
图文导读
I AZIB中的水溶液电解质化学
水分子(H₂O)是一种极性分子,含有一对非共线的极性共价键(O-H键),导致氧原子末端带负电荷,氢原子末端带正电荷,如图1a所示。氢键是由一个水分子的O原子和相邻水分子的H原子之间的静电相互作用形成的(图1b)。在液态水中,多个水分子通过氢键形成水簇((H₂O)ₙ)。一旦向液态水中加入可溶性盐(如ZnSO₄),溶液中的单个Zn2⁺离子将通过水合作用形成的Zn(H₂O)ₙ 2⁺,其结构如图1c。
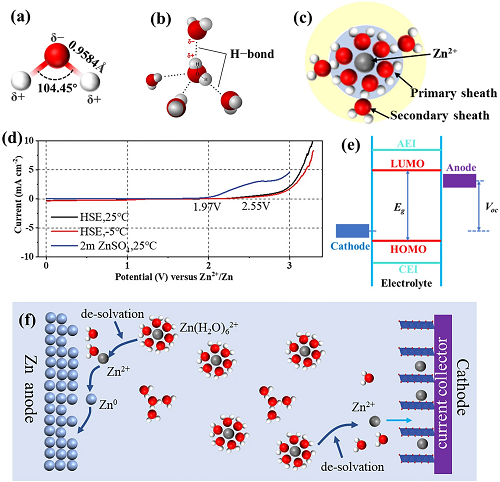
图1.AZIB中的水溶液电解质化学。
在含水电解质中,各种水构型处于动态平衡,单个游离水分子倾向于形成水簇或溶剂化阳离子。因此,电解质中的水分子构型包括水分子团簇(水分子之间的氢键)、溶剂鞘水分子(水分子与离子之间的静电力)以及微量的独立水分子,这三种形态表现出不同的热力学稳定性。水合盐电解质可以抑制水簇的存在,并将分解电压提高到2.55 V(相对于Zn2⁺/Zn),高于2M ZnSO₄电解液中1.98 V的低分解电压(图1d),表明氢键的形成降低了水分子的热力学稳定性。
Zn(H₂O)₆2⁺作为电解质中的电流导体,在电场的作用下在阴极和阳极之间迁移形成回路,实现能量的储存和释放。由于Zn2⁺以溶剂化的Zn(H₂O)₆2⁺的形式存在,不能直接参与再电极表面的嵌入/脱出。因此,位于电极界面处的溶剂化锌离子Zn(H₂O)₆2⁺需要去溶剂化并释放水分子,AZIB中Zn2⁺的在阳极的沉积/溶解及阴极的嵌入/脱出反应如图1f所示。与水分子团簇和溶剂鞘水分子相比,去溶剂化释放出的独立的自由水分子热力学稳定性差,导致电极界面上的寄生反应严重。电极界面的稳定性与电极/电解质界面高度相关,包括阴极-电解质界面(CEI)和阳极电解质界面(AEI)。对于有机LIB,全电池的最大工作电压范围是最低未占分子轨道(LUMO)和最高已占分子轨道(HOMO)的能量之差。μA和μC分别是阳极和阴极的电化学电势,当μA高于LUMO能量时,电解质溶剂被还原形成AEI;同样地,如果μC低于HOMO能量,电解质溶剂被氧化形成CEI(图1e)。AEI和CEI都可防止寄生反应的进一步发生。然而,在AZIB中没有AEI和CEI膜。在电池循环过程中,多变的溶剂环境、不稳定的电解质以及缺失的AEI/CEI膜层都会促进电极界面处的严重寄生反应。电解质中水的构型活性顺序为独立水>水分子团簇>溶剂化水。理解和调节AZIBs中的水分子化学是构建稳定AZIBs的有效突破。
II 水溶液中的锌负极反应化学
在AZIBs的运行过程中,水合锌离子在电极界面发生去溶剂化,改变了局部环境,导致各种副反应,包括腐蚀、钝化和锌阳极上的枝晶。水的电离产生的H⁺和OH⁻,OH⁻与Zn2⁺络合,导致H⁺的浓度的增加,Zn(H₂O)ₙ 2⁺中的配位水分子水解也会产生H⁺。因此,电解质的pH显示酸性(pH < 7)。从锌的Pourbaix图来看(图2a),金属锌在酸性电解质中表现出热力学不稳定性。由于没有AEI保护层,置换反应会直接在锌阳极上发生,H⁺被还原成H₂,Zn被氧化成Zn2⁺,这个过程被称为腐蚀析氢(CHE)。CHE会发生在AZIB的充电,放电和怠速过程中(如图2b)。如图2c所示,在1 M硫酸锌电解液中浸泡一周的锌箔被腐蚀并失去光泽。CHE速率非常缓慢,并将持续很长一段时间,这种腐蚀会引发锌的无效消耗和电池膨胀。在锌沉积过程中,从溶剂鞘中除去的水分子在锌阳极表面上积累,这些水分子更可能在金属表面上得到电子形成H⁺和OH⁻(图2b),进一步触发电化学析氢(EHE)。严重的EHE过程导致极碱性微区,这又导致严重的锌腐蚀。图2d是由原位光学显微镜观察的EHE和锌枝晶的情况。锌腐蚀会导致电解液溶剂耗尽、消耗和腐蚀金属锌、形成钝化产物和锌枝晶,导致电池的库仑效率降低,生成的气体引发电池体积膨胀导致电池破裂,阻碍电池的长期、稳定循环。
微区HER过程消耗H⁺,并产生OH⁻,导致高浓度OH⁻的积累。锌离子、阴离子和游离水分子遇到的碱性微区会导致钝化产物的形成。这些钝化产物堆积松散,且锌离子的传导。钝化产物在锌阳极上的积累它增加了锌离子沉积的过电位,促进了不均匀的锌离子沉积,导致电解质组分(包括盐和水)不受控制的消耗,加速HER过程和枝晶生长,降低了离子电导率。
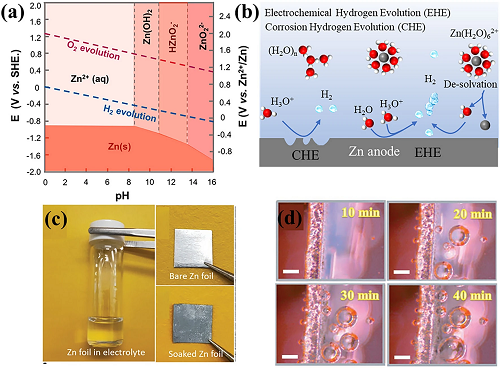
图2. AZIB中的锌负极反应化学。
与其他金属电池类似,锌金属阳极基于离子沉积/溶解机制运行。锌阳极的沉积/溶解速率主要受液相中锌离子的传质控制,其影响因素已被广泛研究,如锌表面织构、电场分布和盐浓度。锌枝晶的形成原理如图3a-c所示。锌离子在外部电场下移动到锌电极表面,它们优先沉积在能量活性位点(如晶界和缺陷),形成小突起。在突起处产生强电场分布,这诱导更多的锌离子聚集在活性位点,并且导致锌离子在电解液中的分布更不均匀,引发进一步的浓度极化,加剧锌离子在液相中的不均匀传质。随着沉积的继续,尖端效应在初始沉积位置放大,导致离子浓度、电场分布和沉积速率的更不均匀,最终导致枝晶的形成。图3d-f的模拟也验证了锌枝晶的沉积过程。锌枝晶逐渐生长,有刺穿隔膜并导致短路的风险。更重要的是,锌枝晶从根部脱离并游离到电解质中,成为“死锌”,显著降低锌的利用率。因此,锌枝晶的不可控生长已成为AZIBs发展的主要障碍。

图3. AZIB中的枝晶形成原理。
2.1 三种寄生反应的相互关系
在沉积过程中,电解液促进了不均匀的锌离子流动,促进了枝晶的严重生长。枝晶的无序生长增加了锌电极和电解质之间的接触面积,为寄生反应的发生提供了更多的活性位点,从而加快了寄生反应的速率。锌枝晶的生长伴随着锌表面上Zn(H₂O)₆2⁺的去溶剂化产生活性水分子,该活性水分子会引起寄生反应。HER为锌钝化提供碱性微区,这促进了副产物的形成,副产物在锌表面的积累增加了电化学过电位,从而促进析氢腐蚀。总之,锌枝晶、钝化、HER之间的是相关的,其关系的总结如图4所示。
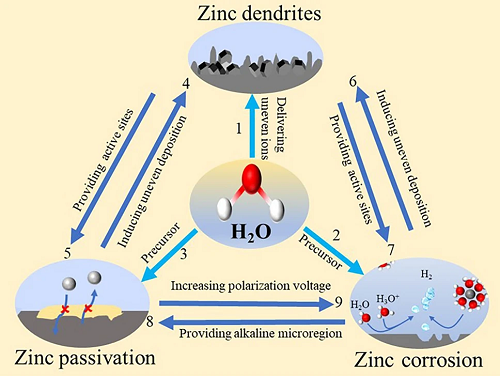
图4. AZIB中锌阳极寄生反应的相互关系。
III 提升电解液及锌阳极的热力学稳定性
3.1 提升电解液热力学稳定性
电解质的组成,包括添加剂和锌盐,可以对电解质的热力学稳定性产生深远的影响。因此,调节电解质的稳定性和避免寄生反应有多种模式,包括选择合适的锌盐、通过浓缩电解质调节水的形态和使用添加剂。
3.2 电解质锌盐种类调控
如图5所示,Zn(CF₃SO₃)₂、ZnSO₄、ZnCl₂和Zn(NO₃)₂电解质的四种锌盐的CV曲线表现出不同的电化学行为,表明不同的热力学稳定性,这与阴离子的作用有关。Cl-的渗透作用导致窄的阳极电位窗口和低CE(图5c);NO₃⁻阴离子作为强氧化剂会氧化锌箔,导致锌阳极严重腐蚀(图5d)。因此,由于其差的热力学稳定性,稀的 ZnCl₂和Zn(NO₃)₂电解质很少用于AZIB中。相比之下,因为SO₄2⁻的稳定结构和CF₃SO₃⁻ 的庞大体积,1 M ZnSO₄和1 M Zn(CF₃SO₃⁻)₂提供了高CE和宽电化学窗口(图5a-b)。1 M Zn(ClO₄)₂电解质同样展现了良好阳极稳定性和99.0%的高CE,电池运行期间ClO₄-的微量还原会在锌电极上构建含Cl⁻的保护层。然而,Zn2⁺会与ClO₄⁻配位生成ZnO钝化层,这增加了Zn2⁺的扩散势垒,导致反应动力学缓慢。综上所述,未来AZIB电解液市场仍将由与各种阴极和锌阳极具有优异相容性、价格低廉且热力学稳定性高的锌盐主导,例如ZnSO₄和Zn(ClO₄)₂。

图5. 不同电解质中锌阳极的稳定性。
3.3 电解质浓度调控
除了锌盐的种类外,浓度也决定电解质的热力学稳定性。在ZnCl₂电解质中,随着盐浓度的增加,水分子被转化到锌离子的溶剂鞘中,电位窗口从相对于1.6 V(5M ZnCl₂)增加到2.3 V(30M ZnCl₂),如图6a所示。由于高浓度电解质中极度缺乏水分子,Zn2⁺离子的溶剂鞘被阴离子取代,因此增加盐浓度可以增强水分子中O-H键的强度。此外,在电解质中加入另一种可溶性盐也能破坏水分子团簇的氢键网络。如图6b所示,在1M Zn(TFSI)2⁺ 10M LiTFSI电解质中,TFSI⁻取代了原来的水鞘,当LiTFSI的浓度增加到20 M时,六个水分子均被TFSI⁻取代,完全避免了溶剂化锌离子去溶剂化过程中电极表面独立水分子的积累。水分子团簇和Zn(H₂O)₆2⁺被显著抑制,水分子中O−H键的强度增强,有助于提高电解质的热力学稳定性。如图6c所示,随着LiTFSI浓度的增加,H₂O的氢键峰逐渐消失,这表明氢键网络被破坏,水分子的热力学稳定性增强。1⁷O的NMR结果显示较低的化学位移和较窄的半高信号(图6d),表明先前过量的水O原子被添加的Li⁺直接占据和消耗。这种独特的电解液能够实现几乎100%的CE电镀/剥离工艺,并且水的挥发性得到了很好的抑制。
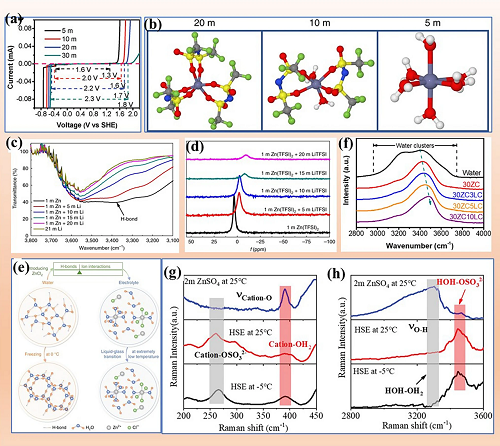
图6. 不同浓度电解质的稳定性。
具有LiCl添加剂的二元ZnCl₂基盐包水电解质(WiSE)通过将水簇转化为溶剂化水分子来减轻析氢。O−H键强度和盐浓度之间的关系可以通过拉曼光谱(FSRS)获得(图6f),氢键振动峰消失表明了水簇(氢键)的消除。水合盐电解质(HSE)体系会触发Zn(H₂O)₆2⁺的不饱和水化结构,SO₄2⁻进入Zn2⁺的溶剂化鞘层(图6g),电解质中的水簇不存在H₂O(图6h),进一步证实HSE中没有水簇。另一种贫水电解质是低共熔溶剂(DES)电解质。DES与WiSE的区别在于DES不仅含有可溶性盐,还含有极性分子,它们通过氢键与H₂O结合,进入Zn2⁺的溶剂化鞘层。局部高浓度电解质(LHCE)中几乎没有游离水分子,这就避免了水参与寄生反应。以上几种电解质浓度调控方式增强了电解液在锌电极周围环境中的热力学稳定性,从而避免了副反应的发生。
3.4 电解质添加剂调控策略
除了增加盐浓度和选择合适的锌盐外,还可以在电解液中加入添加剂,以提高电解液的热力学稳定性。根据添加剂在电解质中的分布位置,将其分为三类:(1)通过破坏水分子团簇结构,降低水分子团簇含量;(2)与阳离子配位,取代阳离子壳层的溶剂化水分子;(3)促进阴离子进入阳离子壳层,实现阴离子与添加剂共配位阳离子溶剂壳层。第一类添加剂的机理和作用类似于在稀电解液中增加盐浓度,即添加剂打破原有的氢键网络(水簇),将水分子转化为阳离子溶剂鞘或通过化学键固定水分子,形成不饱和溶剂化结构(Zn(H₂O)ₙ2⁺,n < 6)。这种类型的添加剂包括可溶性盐和含有极性官能团的有机物质。而另一类添加剂,例如葡萄糖,通过减少水分子簇的含量和吸引独立的水分子来有效抑制副反应,从而增强电解质的稳定性。还有一类添加剂不仅具有与第二类添加剂类似的功能,而且还可以促进阴离子(如TFSI⁻和CF₃SO₃⁻ )与阳离子的配位,实现添加剂和阴离子与阳离子的共配位结构。此外,溶剂化鞘中的添加剂分子和阴离子会在电极表面分解形成保护层(AEI),隔离电解质溶剂,进一步有效保护电极。与电极改性相比,电解质工程提供了一种更多功能和更全面的方法。它不仅可以提高电解质和电极的热力学稳定性,而且可以动态调节AZIBs中的寄生反应。但在使用添加剂的过程中,其分解产物相关的潜在毒性和污染至关重要,在选择添加剂时仍需要仔细考虑并进行广泛的实验研究。
3.5 提高锌阳极热力学稳定性
锌阳极的热力学稳定性受固有性质影响。Zn金属具有六方密排(HCP)晶体构型,其中晶格参数为a=b=2.63μm,c=5.21μm。Zn(002)晶面作为致密堆积晶面的显示最低的表面能(2.08 eV nm⁻1),而Zn(100)面具有最高的表面能(4.60 eV nm⁻1)。Zn(100)平面显示出比Zn(002)更负的锌原子吸附能,这意味着锌优先沉积在Zn(100)晶面上(图7a-b)。然而,在溶解过程中,锌原子从Zn(002)的剥离能量比Zn(100)的剥离能量更高(图7c),这表明沿着Zn(002)的缓慢剥离速率阻碍了Zn阳极的均匀电化学溶解,在电池工作中会更多的暴露不稳定的(100)晶面。此外,氢在Zn(002)上的吸附自由能大于Zn(100)的吸附自由能,表明HER可以通过暴露更多的Zn(002)平面来抑制。也就是说,在电池循环期间将暴露更多的Zn(002)面,可以使锌电极更加稳定。
3.6 织构化锌电极
为了获得高度暴露的Zn(002)晶面,可以直接使用具有暴露的Zn(002)的单晶或高度织构化的锌作为AZIB的阳极。如图7e所示,单晶Zn金属衬底在整个电镀过程中沿着Zn(002)提供无差异和无应力的沉积基底。无应力的同质外延沉积确保了沉积层的最低能垒、最低内应力、最小晶格畸变,确保了内能的最小化。此外,由于(002)晶面有利于横向生长和晶格匹配,可以保持完美的原子间拼接,确保没有缺陷形成,从而消除非平面Zn成核(Zn枝晶)的来源。这类电极可以实现超过500小时、高度稳定可逆的锌剥离/电镀,CE为97.71%。然而,单晶锌的超高价格和商品化锌箔前处理工艺的不完善,要求研究人员不断探索织构化锌电极的构建。调节锌织构的另一种策略是在具有与Zn(002)的低晶格失配率(< 25%)的衬底上进行异质外延生长。为了保持较小的界面能和晶格畸变,Zn原子倾向于沿着衬底晶格生长,形成半共格或共格界面。如图7f所示,单层石墨烯(Gr)衬底作为用于锌沉积的异质外延衬底,以实现高度暴露的Zn(002)阳极和改善的循环性能,Gr层和Zn(002)之间的低晶格失配(7.5%)促进了沿Zn(002)面的生长,并实现了低界面能(0.212 J·m⁻2),从而增强了电沉积层的热力学稳定性,有效地抑制了寄生反应。
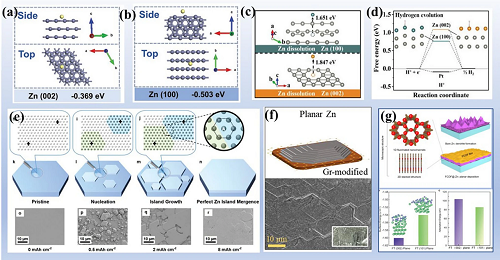
图7. 锌阳极的稳定性调控。
3.7 SEI膜和工作电流调控锌沉积
另一种策略是通过SEI和工作电流提高吸附能,并降低Zn原子沿着Zn(002)的扩散能垒。Zn原子会优先沉积在Zn(100)上以形成枝晶,如果能够改变这种趋势,则可以有效地实现Zn原子沿沿着Zn(002)面的沉积。氟化多孔共价有机框架(FCOF)膜作为Zn阳极的保护层(FCOF@Zn),可以实现Zn(002)平面的优先生长(图7g)。在FCOF膜中,电负性F原子与锌离子强烈相互作用,促进锌离子的流动,且降低Zn(002)相对于Zn(101)的表面能,从而使得锌原子能够沿Zn(002)面沿着沉积并实现片状形态。工作电流影响锌沉积的过电位,进而影响锌离子沉积的热力学行为。正如所证明的,随着工作电流密度从1 mA/cm⁻2增加到100 mA/cm⁻2,锌电镀行为化学上有利的Zn片到动态控制的堆积晶体,然后到扩散限制的金属柱。为了规避通过外延沉积获得织构化电极的策略,使用控制工作电流的新策略来获得织构化锌电极。在低电流密度下,外延成核占主导地位,晶核的取向强烈依赖于衬底,无纹理衬底上的锌沉积演变为随机取向的锌;在中高电流密度下,过电位的增加促进了水平Zn(002)核的形成,削弱了基体的影响。即使在随机取向的衬底上,也可以形成致密的织构化Zn(002)。高度暴露的Zn(002)阳极可以通过使用新型电解质、添加剂和隔离物来实现,从而调节Zn沉积的热力学行为。这些策略的共同目标是控制Zn离子的原子级沉积,导致Zn(002)晶面的暴露。这些工作为进一步构建无寄生反应的锌阳极提供了有意义的参考。

图8. 使用解耦电解质的电池工作示意图。
3.8 解耦电池提高锌阳极和电解液稳定性
pH环境会影响电解质和电极的热力学稳定性。碱性环境对阳极侧的电化学HER更具抗性,而酸性环境抑制水分子在阴极侧的阳极过程。因此,为阳极和阴极创建解耦的电解质环境可以增强电解质和电极两者的热力学稳定性,最终扩大电化学窗口。传统的带有隔膜(如玻璃纤维和滤纸)的两室电池无法有效隔离电解液。随着膜材料的发展,具有两个离子选择性膜的三室电池可以有效地解耦电解质环境。例如图8a中的Zn||MnO₂电池,具有中性电解质(0.1M K₂SO₄)和两个离子选择性膜的夹层室隔开了具有碱性电解质(6M KOH + 0.2M ZnO + 5 mM香草醛)的Zn阳极和具有酸性阴极电解质(3M H₂SO₄ + 0.1M MnSO₄)的MnO₂阴极。Zn||MnO₂表现出高开路电位和几乎恒定的放电容量在各种电流密度。类似地,双极膜(BPM)也可以代替的夹层室,用于分离Zn电解质的碱性电解质和酸性电解质,提供高电压和高能量密度(图8b)。与具有可渗透隔膜的传统电池相比,这种设计提高了AZIB的热力学稳定性,减轻了寄生响应,并拓宽了电解质工作窗口。
IV 从动力学角度抑制寄生反应
除了调节AZIBs系统中电池组分的固有稳定性外,还可以通过外部手段来抑制寄生反应,例如减少活性位点和构建人工AEI。本节主要从动力学的角度综述了抑制寄生反应的先进策略。阻断电解质与电极之间的接触区域可以减少副反应。一种方法是利用可以吸附在锌活性位点上的吸附剂,防止反应物(例如Zn金属和H₂O)之间的接触。另一种是在锌电极上使用电子绝缘但离子导电的AEIs,包括人工SEI和衍生物SEI。
4.1 吸附剂屏蔽活性位点
吸附剂通过静电力、官能团和其他物理效应与锌基底相互作用,而不与锌电极发生任何反应。吸附剂需要具有热稳定性、化学稳定性和电化学稳定性,以及强吸附能力以抑制水与电极接触。有机和无机吸附剂都可以作为添加剂添加到电解液中。
4.2 有机吸附剂
如十六烷基三甲基溴化铵(CTAB)、十二烷基硫酸钠(SDS)、聚乙二醇(PEG)、硫脲(TU)、聚环氧乙烷(PEO)、聚丙烯酰胺(PAM)和环糊精(CD)的应用对AZIB中寄生反应的具有良好屏障性能。将10mM α-CD添加到3M ZnSO₄电解质中可抑制Zn表面的寄生反应。如图9a所示,α-CD分子的外表面显示出集中的负电荷(蓝色区域),这意味着它在金属基底上具有较强的吸附能力。如图9b-c中的Tafel和LSV曲线所示,α-CD具有强吸附作用,Zn电极表面自吸附的α-CD层作为保护层,降低了H₂O与电极界面的接触频率,从而抑制了寄生反应。一些富含极性官能团的有机吸附剂(如PEO和PAM)不仅可以吸附在锌电极界面上阻断溶剂与电极界面的接触,还可以通过官能团提高锌离子在电极界面的浓度,促进锌离子反应。如图9d所示,将长链PEO吸附剂引入到水性电解液中,其可以吸附在锌表面以形成PEO层,并提高锌金属阳极的稳定性。此外,醚基(−O−CH₂)与Zn2⁺之间的强相互作用使得Zn2⁺在电极界面富集,并实现均匀的镀锌/退锌过程。因此,PEO的吸附抑制了副反应的发生,并促进了有效的电荷转移。 锌自腐蚀的交换电流密度降低,证明吸附层阻止了寄生反应的发生(图9e)。某些具有电荷和极性的小分子吸附剂在吸附暴露位点时表现出显著的选择性。极性(带电)分子可以通过吸附在突起上的分子来阻挡活性位点。如图9f所示,将阳离子表面活性剂Na₂TBA₂SO₄作为添加剂引入水性电解质中,Na₂TBA⁺离子吸附在Zn阳极表面上以调节初始成核并抑制活性位点,Zn2⁺离子只能吸附在活性位点的相邻区域上,直到形成光滑的沉积层。与上述有机阳离子表面活性剂类似,高度极化的乙醚分子优先吸附在突起的尖端,以减少活性锌的暴露面积,减轻副作用的发生。表面有机吸附剂对寄生反应的抑制作用与链长、浓度、官能团和电解质pH值有关,其致密性也显著影响电池性能,因此,在选择吸附剂时应平衡多种因素。
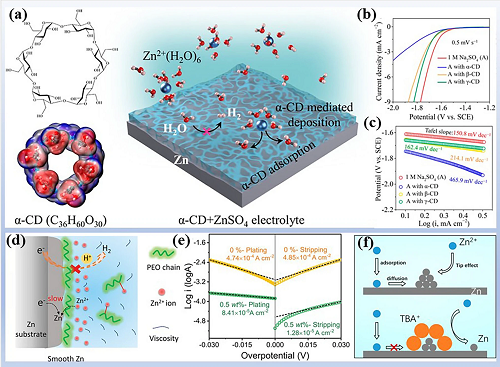
图9. 有机吸附剂的改性原理。
4.3 无极吸附剂
无机吸附剂包括可溶性离子吸附剂(如LiCl 、硫酸铟、硼酸、La(NO₃)₃ 、氢氧化铵)和不溶性吸附剂(ZnF₂ 、SnO₂、g-C₃N₄、石墨烯量子点、Ti₃C₂Tₓ)。可溶性无机吸附剂主要依靠静电屏蔽效应来限制活性中心的生长,具有比电极阳离子还原电位的阳离子添加剂可以吸附在突起上。如图10a-b所示,在沉积过程中,活性位点表现出强电场,阳离子添加剂优先吸附在活性位点上,促使Li⁺离子在活性位点的相邻区域中进一步沉积,直到形成平滑的沉积层。不溶性无机吸附剂,其作用机理与有机吸附剂相同,主要为减少副反应前体的接触频率和调节锌离子的流动。如图10c所示,作为电解质添加剂的Ti₃C₂Tₓ可以通过静电相互作用吸附Zn2⁺,然后沉淀在Zn阳极的表面上。Ti₃C₂Tₓ层的存在可以使沉积过程中的Zn2⁺的分散和流动均匀化,并阻断活性位。然而,这些物理吸附剂在电极表面上的不连续分布和弱结合力导致对副反应的抑制有限。此外,该方法增加了电解质的粘度并降低了电解质的离子电导率。

图10. 无机吸附剂的工作原理。
4.4 构建导电锌离子的SEI膜
与非水电池不同,Zn阳极上不存在原位固体电解质中间相(SEI),导致持续的寄生反应。从有机电池中获得灵感,已经探索了使用衍生物SEI和人工SEI来减轻这些寄生反应。
4.5 衍生SEI
原位衍生SEI可以通过电池中的自发化学反应或添加剂和阴离子在LUMO电位以下的分解形成。衍生的SEI可以与锌电极的无缝连接,并确保均匀分布,有效地调节活性位点并抑制寄生反应。KPF₆在水系电解液通过PF₆⁻与水反应衍生原位SEI,如图11a所示。PF₆⁻与水反应形成POF₃、HF、HPO₂F₂、H₂PO₃F和H₃PO₄,这些物质与锌金属自发反应,形成含Zn₃(PO₄)₂和ZnF₂的原位SEI。某些添加剂可以直接在电池运行过程中产生SEI,例如多巴胺可通过空气中的自氧化或水溶液中的电化学聚合转化为聚多巴胺(PDA)。如图11b所示,通过将DA引入电解质中在Zn阳极上构建原位PDA,其用作隔离层以抑制副反应。同时,SEI层调节了Zn2⁺的均匀分布,促进了Zn的均匀成核。另一种衍生SEI是调整Zn2⁺的溶剂化结构,减少锌盐和有机助溶剂的阴离子。在该衍生物SEI中,通常包括无机内层和有机外层。例如,1,2-二甲氧基乙烷(DME)可以在DME和OTF⁻的共同参与下产生独特的Zn2⁺溶剂化结构,通过DME和OTF⁻的分解,在Zn阳极上产生有机外层和无机ZnF₂−ZnS内层(图11c),保护Zn表面免受水的侵蚀,引导Zn2⁺的扩散,使Zn阳极实现99.7%的高CE和5000 h的长循环寿命。衍生的SEI在将溶剂与Zn阳极隔离中起着至关重要的作用,有效地抑制了Zn表面上的寄生反应。然而,这些衍生的SEI的显著缺点是由于其前驱体的固有热力学性能不稳定性,在电池循环期间就容易快速消耗。

图11. 生成原位衍生SEI。
4.6 构建人工SEI
根据人工SEI在锌离子沉积动力学中的作用,可以将它们分类为:(1)加速锌离子沉积速率;(2)调节Zn2⁺沉积过程的溶剂化结构;(3)排斥寄生反应的前体(如SO₄2⁻和OH⁻)。第一类人造SEI也是最常见的,其特征在于多孔或具有宽层间距(二维材料)。例如蒙脱土(MMT)人工SEI(图12a),MMT的层间为Zn离子传输提供了高速通路,实现高离子电导率。此外,Zn-MMT膜的致密结构阻断了金属电极与电解液中的水分子团簇等离子的接触行为,实现了较高的阳离子迁移数,抑制了寄生反应。第二种类型是一些人工SEI膜不仅可以防止Zn和电解质的副反应前体之间的直接接触并调节锌离子沉积,而且可以有效地中断沉积过程中锌离子的溶剂化鞘,从而减少寄生反应。使用具有2.94 μ m小孔径的ZIF-7涂层,受ZIF-7的小隧道限制,大体积的Zn(H₂O)₆2⁺不能通过。因此,Zn(H₂O)₆2⁺在锌沉积之前先进行脱溶剂化,显著降低了锌电极附近的水浓度。最后一种具有定向布置的某些极性或带电人工SEI可以有效地防止寄生反应前体接近电极表面。例如,在锌电极上构建PbBaTiO₃层作为人工SEI,PbBaTiO₃可以在外部电场下极化,极化方向平行于电场。如图14 c所示,在外加电场作用下,Ti⁴⁺可以偏离TiO₆八面体的中心。随后,定向电偶极子在表面上诱导极化电场。在电镀过程中,由于BTO表面的有序电场,负电荷会集中在Ti-O中的O元素上。BTO层排斥SO₄2⁻和OH⁻阴离子,这些离子与Zn2⁺的碰撞频率降低,进而抑制副反应。

图12. 人工构建SEI。
V 总结与展望
这篇综述介绍了水溶液锌离子电池的最新进展,重点分析了水性电解质中的化学反应和锌阳极的寄生反应,阐述了热力学和动力学两方面抑制寄生反应的解决方案。通过增强热力学稳定性,可以最小化副反应的发生;通过调节和改性电解质/电极界面的动力学,可以减少前体和电极之间的接触频率。通过优化电解质和电极之间的相互作用,可以有效地减轻寄生反应的发生。本文对这些方面进行了总结和展望,强调了热力学和动力学方法在解决与AZIBs中寄生反应相关的挑战方面的重要性,提高固有稳定性和调节电解质/电极界面,可以使AZIBs在储能系统中得到更广泛的应用。
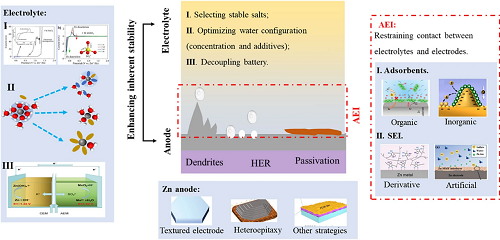
图13. 未来阳极和电解质抑制锌侧寄生反应的改性策略。
作者简介

李彬
本文通讯作者
北京航空航天大学 副教授
▍主要研究领域
(1)新能源材料:金属锂/锌负极材料、硫正极材料等;(2)固态电池:聚合物电解质、复合电解质、电池/电解质界面工程;(3)储能电化学:储能电化学原理研究。
▍主要研究成果
北京航空航天大学材料科学与工程学院副教授。2009年于北航获得学士学位,2016年于北航获得博士学位。留校任教。2019年聘任为博士生导师。主要研究方向为新能源材料及器件,包括锂金属电池、固态电池、锂硫电池及储能电化学等。承担了国家自然科学基金青年项目、科技部重点研发项目子课题等多个项目。已授权国家发明专利14项,转化应用2项。在《Advanced Material》《Advanced Energy Material》,《Advanced Functional Material》,《Nano-Micro Letters》等期刊上发表SCI论文80余篇,其中一作/通讯论文42篇,他引4600余次,个人H因子39。
▍Email:li_bin@buaa.edu.cn

李松梅
本文作者
北京航空航天大学 教授
▍主要研究领域
(1)材料电化学;(2)新能源材料;(3)金属材料腐蚀与防护。
▍主要研究成果
北京航空航天大学教授,北京市教学名师。主讲过本科生和研究生课程6门,其中长期主讲本科生专业核心课程“电化学原理”、专业选修课“分析化学”和硕士生专业课“材料腐蚀与防护技术”。完成6项国家级和校级教学改革项目,出版教育部高等学校材料类教学指导委员会规划教材1部、工信部规划教材1部、专著1部,获得北京市高等教育教学成果奖2项、北航“立德树人奖”优秀奖等教学奖励20余项。作为负责人承担国家自然科学基金面上项目等科研项目10余项,获得四项省部级科研奖励。在《Nature》、《Advanced Materials》、《Science Advances》、《Advanced Energy Materials》等著名学术期刊上发表论文100余篇,已获授权国家发明专利10余项。

钟锦岩
本文通讯作者
北京航空航天大学 助理研究员
▍主要研究领域
(1)航空航天材料的腐蚀科学;(2)表面功能材料与先进防护技术;(3)纳米功能材料与技术。
▍主要研究成果
助理研究员,2014年9月考入北京航空航天大学材料科学与工程学院攻读博士学位,2019年1月于北京航空航天大学材料科学与工程学院获工学博士学位,2015年10月-2017年10月在美国加州大学伯克利分校联合培养博士研究生。2019年2月加入北京航空航天大学材料科学与工程学院,任助理研究员。承担了国家自然科学基金面上项目、青年项目等多个国家级/省部级项目。在《Journal of Energy Chemistry》,《Corrosion Science》,《Nano-Micro Letters》等期刊上发表SCI论文20余篇。
▍Email:jinyanzhong@buaa.edu.cn
撰稿:原文作者
编辑:《纳微快报(英文)》编辑部
关于我们

Nano-Micro Letters《纳微快报(英文)》是上海交通大学主办、在Springer Nature开放获取(open-access)出版的学术期刊,主要报道纳米/微米尺度相关的高水平文章(research article, review, communication, perspective, highlight, etc),包括微纳米材料与结构的合成表征与性能及其在能源、催化、环境、传感、电磁波吸收与屏蔽、生物医学等领域的应用研究。已被SCI、EI、PubMed、SCOPUS等数据库收录,2022JCR影响因子为 26.6,学科排名Q1区前5%,期刊分区1区TOP期刊。多次荣获“中国最具国际影响力学术期刊”、“中国高校杰出科技期刊”、“上海市精品科技期刊”等荣誉,2021年荣获“中国出版政府奖期刊奖提名奖”。欢迎关注和投稿。
Web: https://springer.com/40820
E-mail: editor@nmlett.org
Tel: 021-34207624
https://blog.sciencenet.cn/blog-3411509-1417504.html
上一篇:NML文章集锦| 电解水综述
下一篇:NML文章集锦| 电解水研究论文(一)
