博文
“活体骨膜”:“信号接力”攻克难治性骨缺损  精选
精选
||
浙大谢志坚、贺永团队开发“活体骨膜”:“信号接力”攻克难治性骨缺损
大面积骨缺损的中心区域实现理想的骨愈合存在巨大挑战,近日,浙江大学口腔医院谢志坚教授、潘珲副主任医师团队与机械工程学院贺永教授团队合作构建了一种仿生活体骨膜(BioLiving periosteum)模拟天然骨膜的核心功能,通过理化信号接力模式启动挑战性骨缺损的向心性骨再生及口腔中的垂直骨增量,为严重骨缺损提供了有效的治疗策略。相关研究“A BioLiving Periosteum Evokes Centripetal Regeneration in Challenging Bone Defects”发表于Advanced Science(DOI: 10.1002/advs.202518401)。浙大口腔颌面外科史洋医师、浙大机械工程学院刘念博士及浙大口腔研究生顾静怡为本文共同第一作者。
仿生设计:从天然骨膜中汲取灵感
天然骨膜是覆盖在骨表面的高度血管化结缔组织,既充当“屏障”防止成纤维细胞干扰,又为骨修复提供细胞与信号来源。然而,传统人工骨膜往往在致密结构与生物活性之间难以平衡——结构过密则阻碍营养渗透与细胞迁移,材料过惰则需外源性生长因子补充,后者又难以精准匹配骨修复的动态过程。研究团队受此启发,构建了一种兼具屏障功能与生物活性的“活体骨膜”。其核心是一个通过液体基底培养(LSC)技术制备的细胞膜片迷你组织,并用具有仿生拓扑结构的双层水凝胶作为支持性结构:上层为天然骨膜成纤维层样的平行结构,引导成纤维细胞有序排列;下层为放射状微结构,以募集内源性再生细胞向缺损中心迁移。
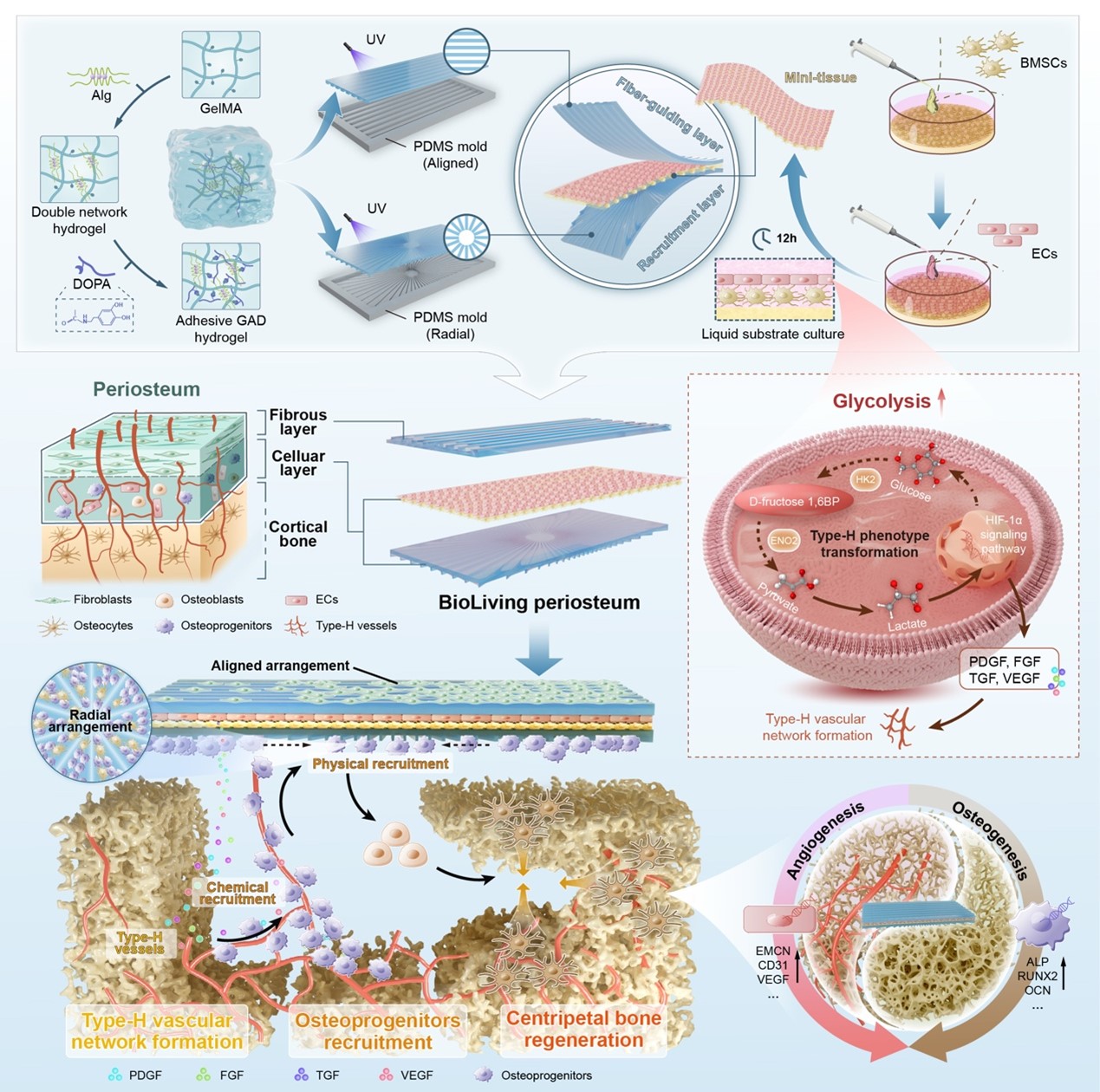
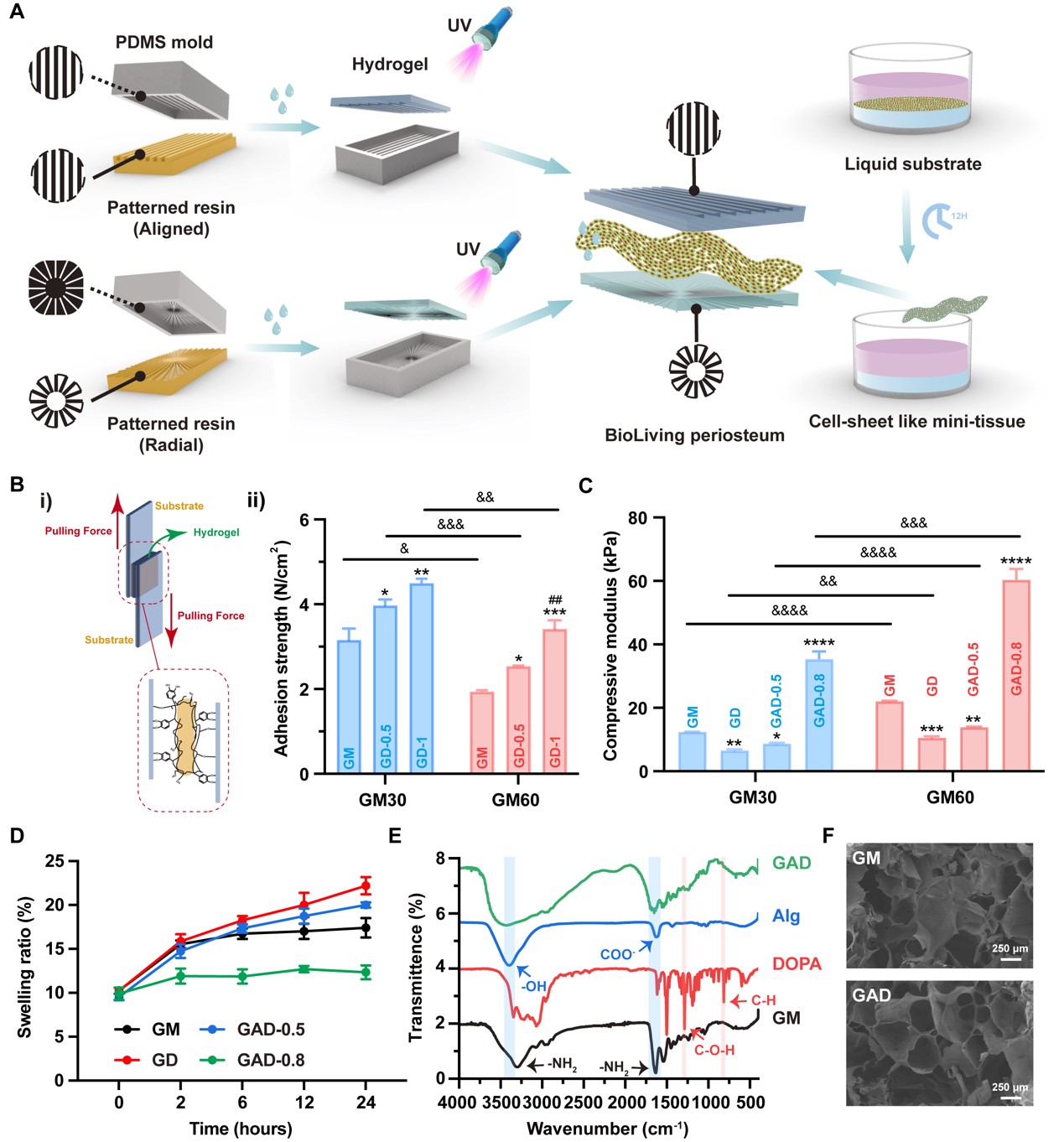
支撑水凝胶:双网络设计兼顾粘附与力学
理想的人工骨膜需具备良好的粘附性与可操作性,研究团队采用甲基丙烯酰化明胶(GelMA)作为水凝胶系统主成分,并引入多巴胺(DOPA)增强粘附性能。实验显示,在低取代度GelMA中,1 wt% DOPA可实现4.5 N/cm²的剪切粘附强度。然而,DOPA的引入会因自由基竞争而降低水凝胶的力学性能。为此,团队进一步引入海藻酸钠构建双网络水凝胶体系,通过离子交联补偿力学损失。优化后的GAD水凝胶压缩模量达60.39 kPa,且在酸性环境中保持稳定,满足骨修复的力学与稳定性需求。
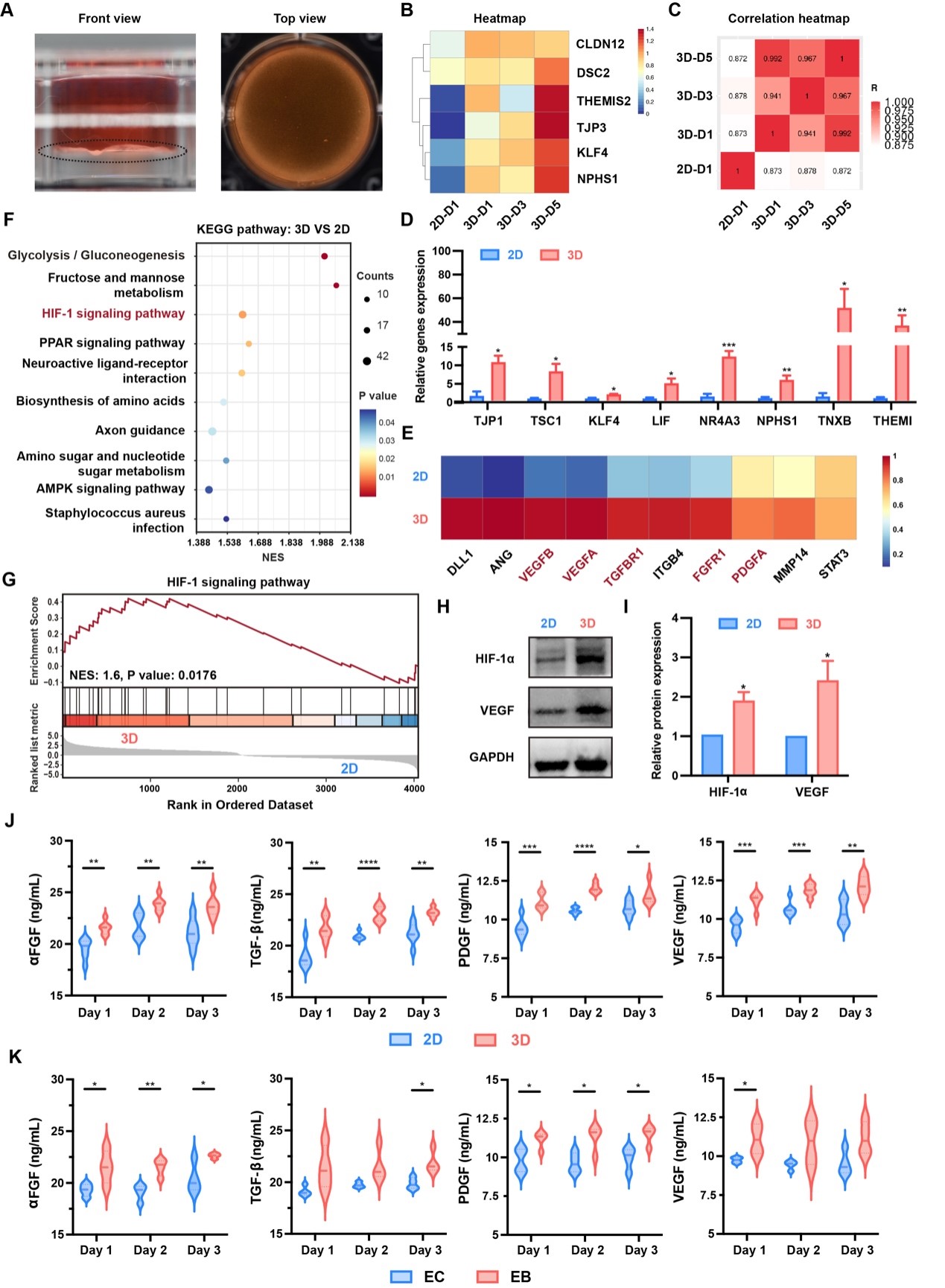
LSC培养法:诱导内皮细胞表型向H型转变
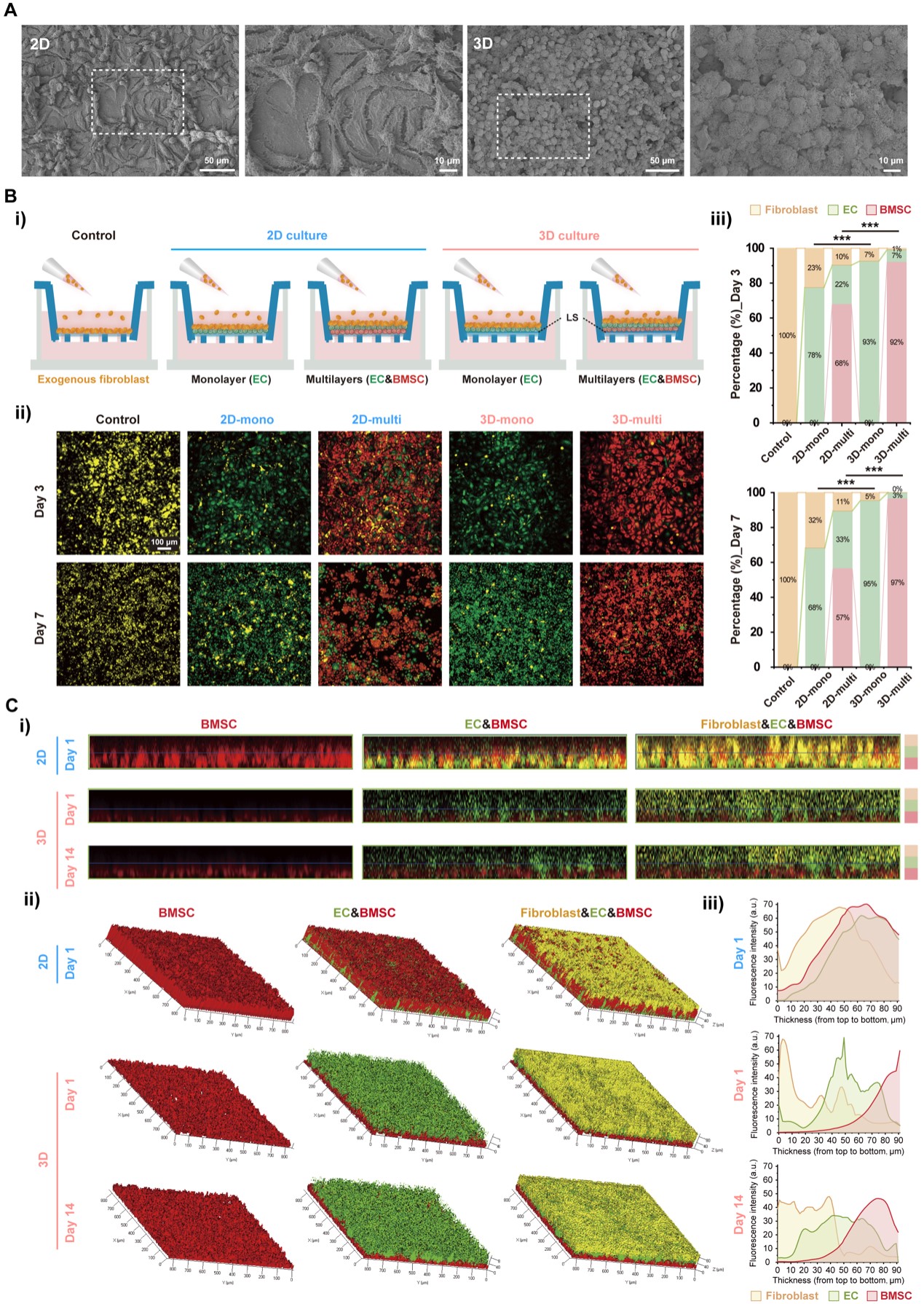
研究团队利用前期研发的液体基底培养(LSC)技术构建活体骨膜的核心结构迷你组织。研究发现,与传统的二维培养法相比,LSC培养法使内皮细胞形成紧密的细胞间连接,并显著上调了血管生成相关基因的表达。转录组测序分析进一步揭示,LSC培养的内皮细胞中,与H型血管(CD31hi EMCNhi)形成密切相关的基因显著上调。KEGG富集分析显示,HIF-1信号通路被显著激活,WB结果也证实LSC培养组中HIF-1α与VEGF蛋白表达水平显著升高。这些结果表明,LSC技术能诱导内皮细胞向H型表型转变,使其具备更强的促血管生成与成骨耦合的能力。
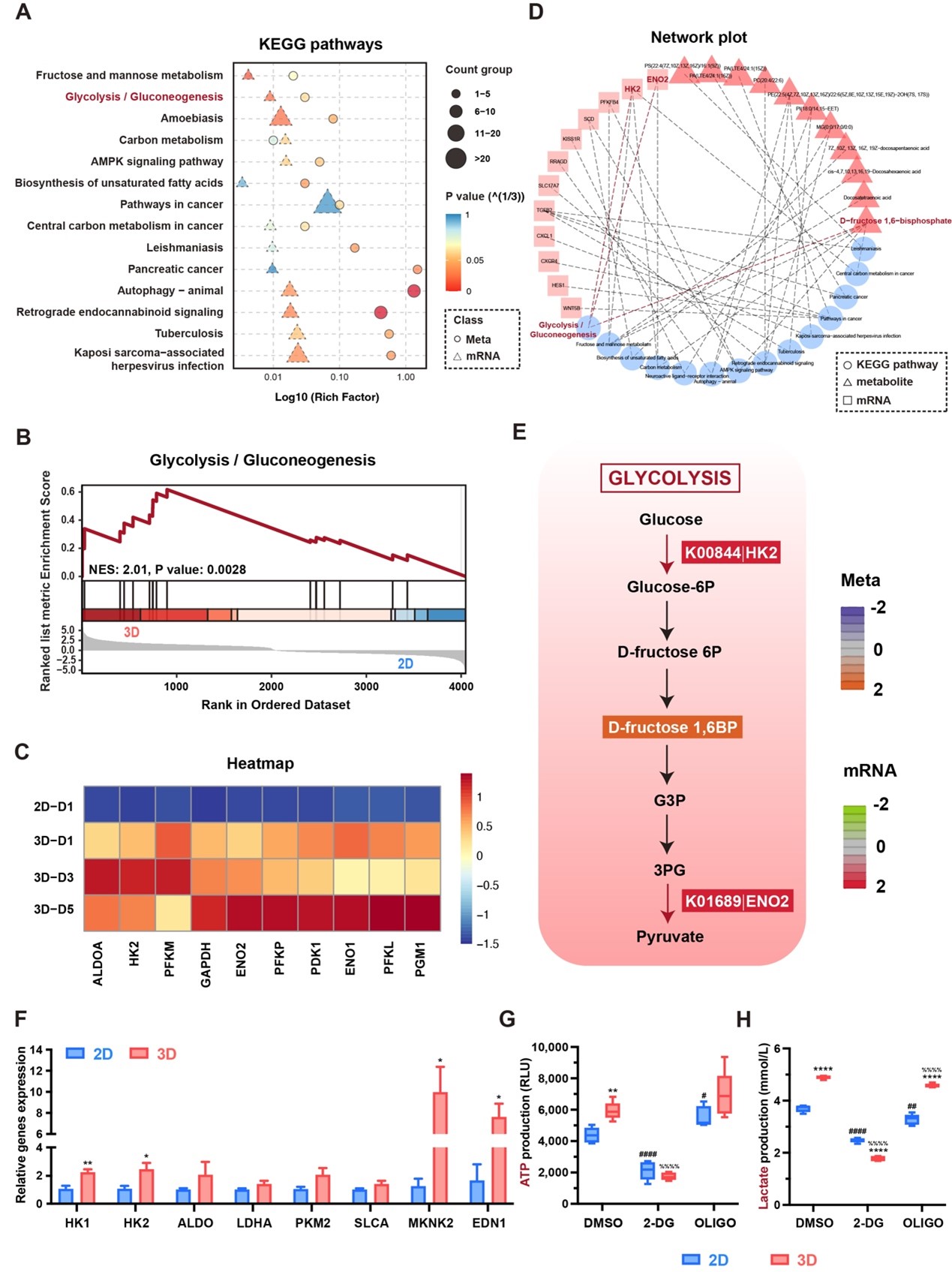
代谢重塑:糖酵解增强驱动H型表型
为进一步探究LSC技术诱导内皮细胞向H型表型转变背后的生物学机理,研究团队进一步进行了转录组与代谢组联合分析,结果发现LSC培养环境下内皮细胞的糖酵解活性显著增强,关键糖酵解酶HK2、ENO2在LSC培养组中显著上调,同时糖酵解核心中间代谢物D-果糖-1,6-二磷酸(F16BP)也呈现显著升高趋势。功能验证实验也进一步显示,LSC培养组中内皮细胞ATP生成量与乳酸产量均显著高于二维培养组,且2-DG处理可显著抑制HIF-1α与VEGF表达。这表明LSC培养通过上调内皮细胞糖酵解代谢为其向H型表型转变提供了能量与生物合成基础。
致密迷你组织:生物活性屏障
在骨愈合过程中形成保护屏障以防止成纤维细胞侵袭至关重要。SEM显示二维培养细胞间存在明显间隙,而LSC培养法构建的三维迷你组织则形成了紧密接触的致密结构。Transwell实验进一步证实单层内皮细胞迷你组织即可显著减少成纤维细胞的跨膜迁移,而内皮细胞与骨髓间充质干细胞构成的多层迷你组织具有更理想的屏障功能。共聚焦图像也显示,在LSC培养环境下不同细胞层在14天后仍保持独立分布,而二维环境下细胞在1天后即发生相互迁移。这些结果验证了LSC培养法构建的迷你组织具备高效的生物活性屏障功能。
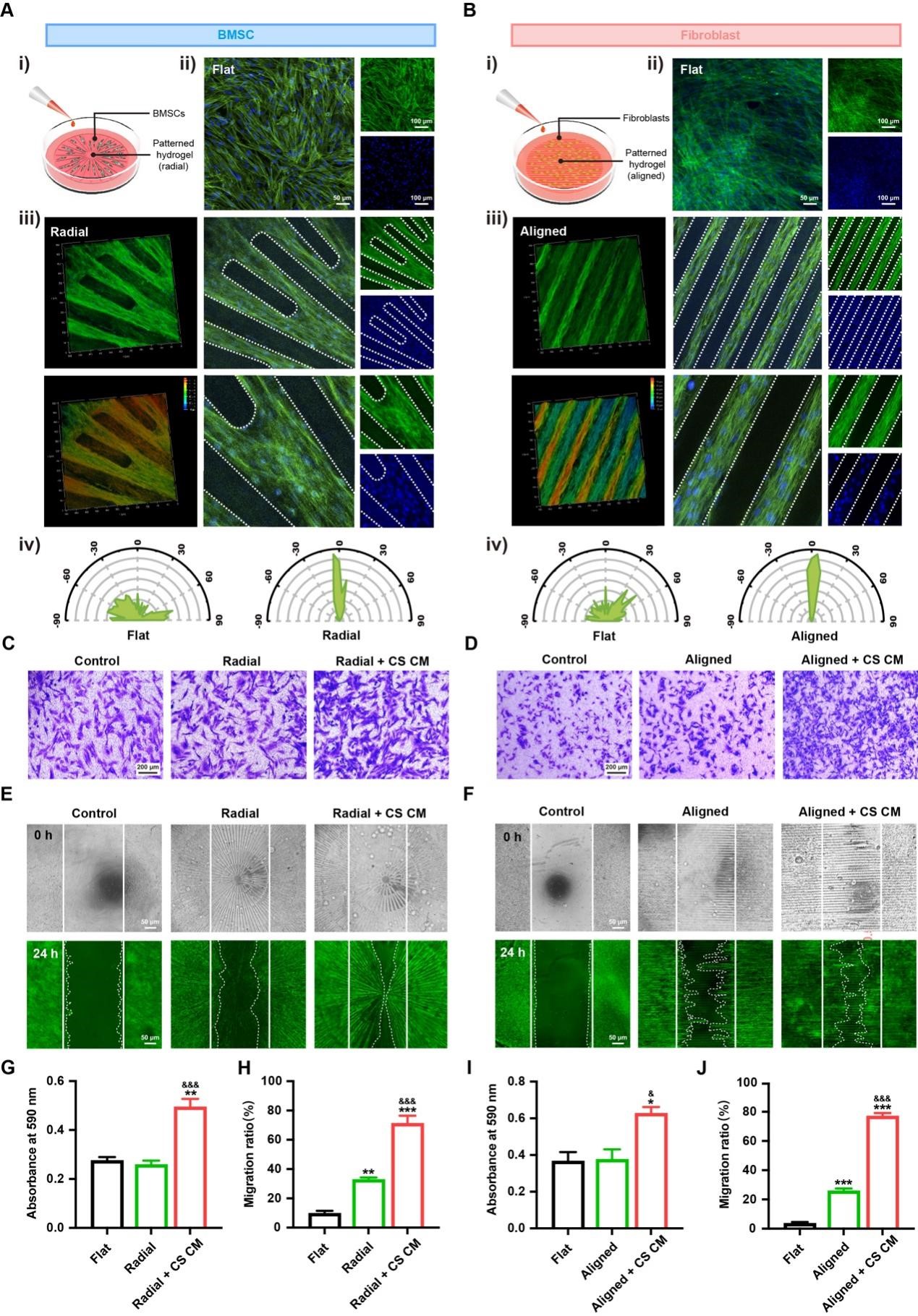
信号接力:物理与化学线索协同调控细胞行为
为模拟体内环境,研究团队将BMSC和成纤维细胞分别接种于不同拓扑结构的水凝胶表面。结果显示,BMSC在放射状结构上呈现定向排列,成纤维细胞则在平行结构中呈现有序取向。通过Transwell迁移实验发现,来自双层迷你组织的条件培养基可显著促进BMSC与成纤维细胞的三维迁移能力。当细胞直接接种于水凝胶表面并与条件培养基共培养时,放射状结构联合共培养组的划痕在24小时内几乎完全闭合。这些结果揭示了化学信号远程招募与物理信号接触引导的信号接力模式,即细胞先响应生化线索迁移至目标区域,随后受拓扑结构引导完成精准空间分布。
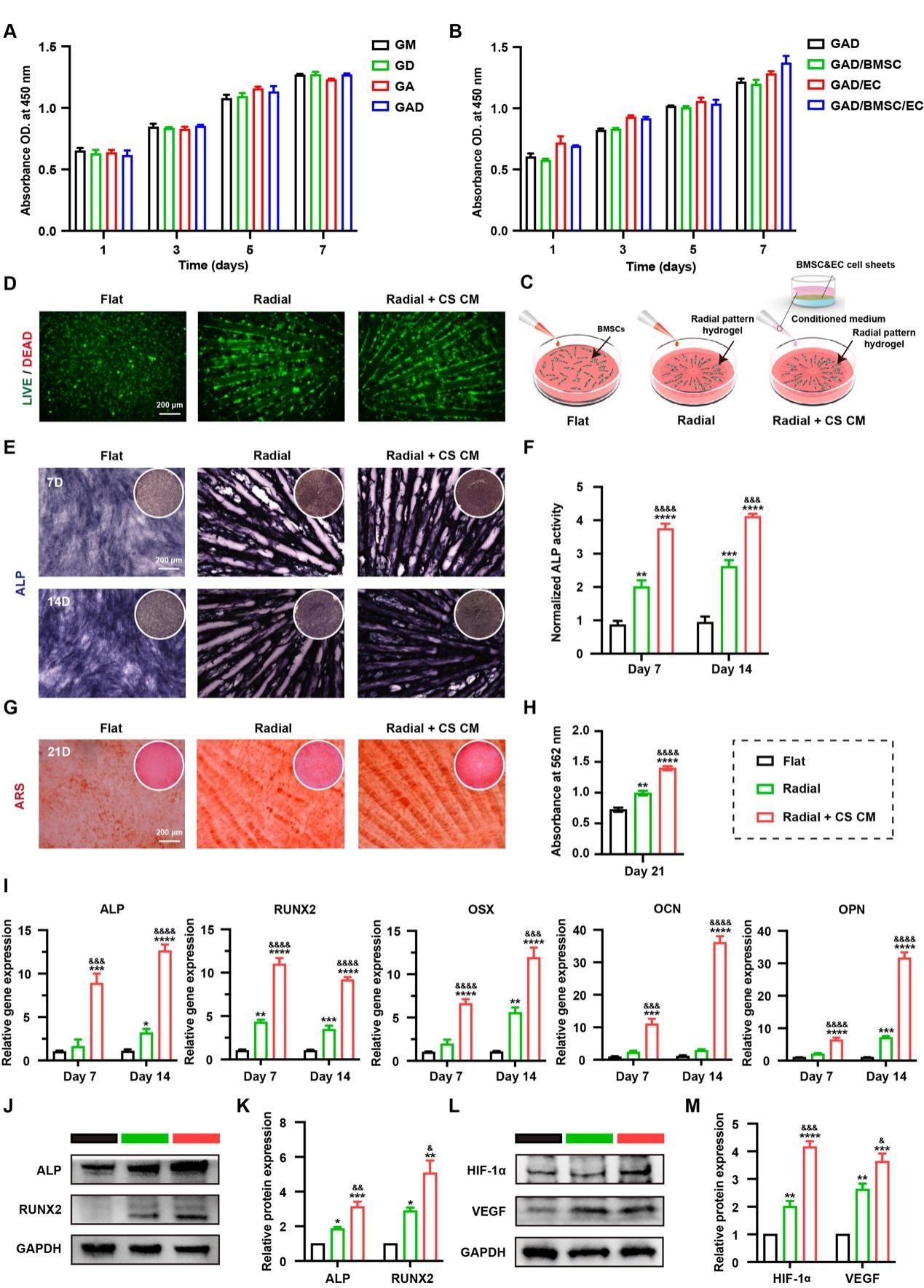
体内外成骨:拓扑结构与生化信号协同
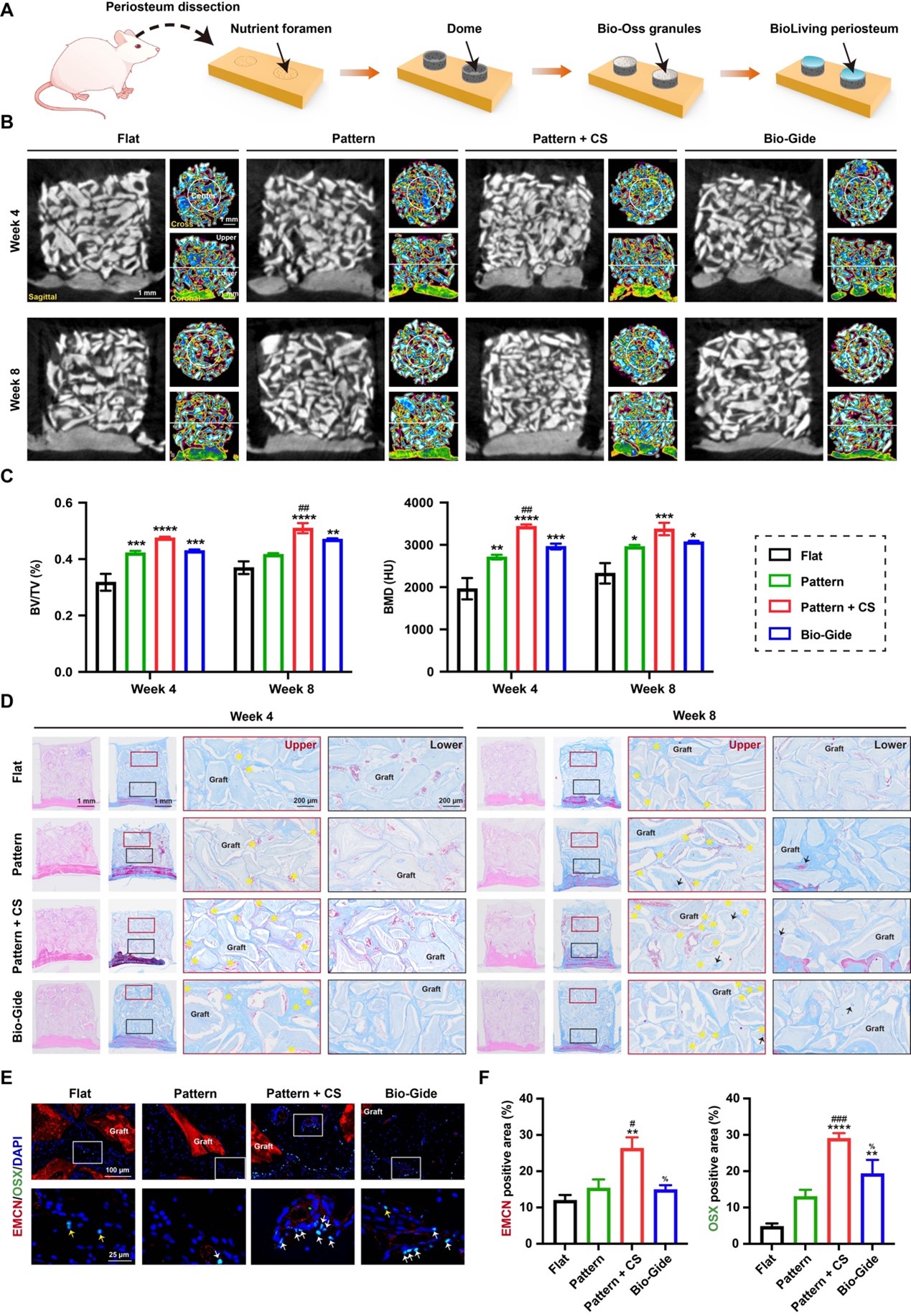
在体外成骨活性评估中,放射状结构显著增强了BMSC的碱性磷酸酶及成骨标志物的表达,联合条件培养基共培养后成骨活性进一步增强。随后研究团队首先在大鼠临界骨缺损模型中评估了活体骨膜的体内修复效果。Micro-CT结果显示,Pattern + CS组骨再生最为显著,BV/TV与BMD均优于临床常用Bio-Gide膜,组织学染色显示,Pattern + CS组在8周时缺损中心区域已接近完全修复,新生骨组织更为致密成熟,而Bio-Gide组新生骨则呈多孔状且蓝染的未成熟胶原纤维较多。免疫组化结果也显示,Pattern + CS组中OSX+成骨祖细胞数量最多,ALP表达也最高。免疫荧光染色进一步证实,该组中CD31hi EMCNhi H型血管数量显著增加,且多数新生血管呈现H型表型。这些结果表明,活体骨膜通过诱导H型血管形成,实现了血管生成与成骨的有效耦合。
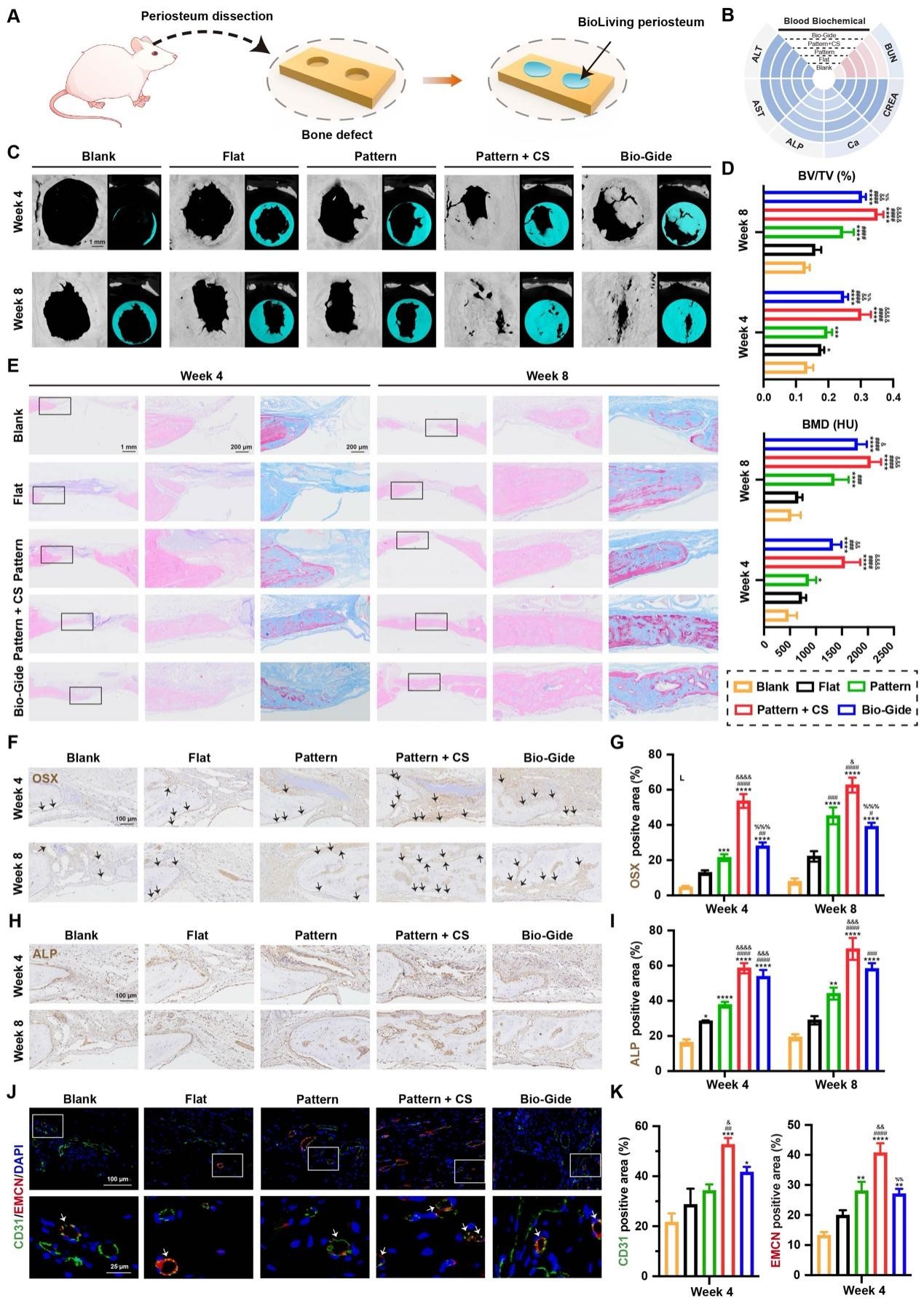
垂直骨增量:向心性骨再生模式
为进一步模拟口腔临床中更具挑战性的垂直骨增量场景(如牙槽嵴缺损),团队建立了大鼠颅骨垂直骨增量模型。该模型中骨环与宿主骨之间仅通过数个营养孔供血,上部的再生区域远离宿主血供来源。Micro-CT结果显示,Pattern + CS组中,增量的中心区域(尤其是远离营养孔的上部)形成了大量新生骨(黄绿色),而其他组则仅在靠近宿主骨的下部区域有少量骨形成。组织学分析进一步显示,Pattern + CS组在术后4周时,增量的上部区域已出现丰富的血管;至8周时,该区域可见明显类骨质沉积。免疫荧光双染显示,Pattern + CS组中CD31hi EMCNhi H型血管数量显著增加,且多数OSX+成骨祖细胞紧密环绕H型血管分布。
本研究开发了兼具生物活性与屏障功能的活性骨膜,通过LSC方法赋予内皮细胞高糖酵解活性,驱使其向H型表型转化,从而分泌大量促血管生成与成骨的生物活性分子,在体内诱导功能性H型血管形成。这些化学信号首先招募OSX+成骨细胞至缺损区域,随后放射状拓扑结构进一步引导这些细胞向中心区域迁移排列。这种理化信号接力新模式有效解决了大面积骨缺损中心区域血供不足、细胞来源匮乏的核心难题。因此,该活性骨膜不仅复制了天然骨膜的屏障功能,更通过主动调控细胞行为,实现了高效的向心性骨再生,为难治性骨缺损的临床治疗提供了新策略。
全文链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202518401
https://blog.sciencenet.cn/blog-2159320-1527960.html
上一篇:Cell Biomater. 神经血管化的工程肌肉
下一篇:高强度与强湿粘附协同的熵驱动氢键重组水凝胶