博文
Cell Biomater. 神经血管化的工程肌肉  精选
精选
||
神经血管化的工程肌肉
容积性肌肉缺失(VML)后的功能恢复仍是当前临床面临的重要挑战。受天然肌肉再生中的“阶段性融合”模式的启发,浙江大学医学院附属口腔医院俞梦飞研究员与浙江大学贺永教授团队,提出了一种将结构引导与电信号调控相结合的重建策略。通过在体外构建包含神经血管组分的定向工程化肌肉,并结合柔性电极递送可控的体内电刺激,该策略协同促进了肌肉组织再生和功能恢复,并有效促进了工程化组分与宿主系统的生物整合。这一进展标志着VML修复从被动结构替代向主动功能重建的转变。该研究以“An electro-responsive functional neurovascularized engineered muscle”为题,发表于《Cell Biomaterials》期刊。
【文章亮点】
1. 提出“结构引导+电信号调控”的双因素协同再生策略:以定向排列的肌纤维作为组织学基础,并通过可控电刺激作为功能性诱导信号,协同促进肌肉的功能化修复。
2. 构建可电响应的功能性神经血管化工程肌肉(EFNEM):通过整合神经-肌肉单元与血管网,促进复合组织再生,为VML修复提供了可行的工程化构建方案。
3. 3D打印的柔性电极与体内精准电刺激递送:通过电信号干预再生微环境,进一步加速神经肌肉整合,显著提升功能恢复质量。
4. 推动修复范式由“被动结构替代”走向“功能导向重建”:以神经-肌肉-血管耦合与电信号调控为核心,强调通过主动干预引导功能恢复,而非仅依赖结构填补。
1. 功能化再生策略
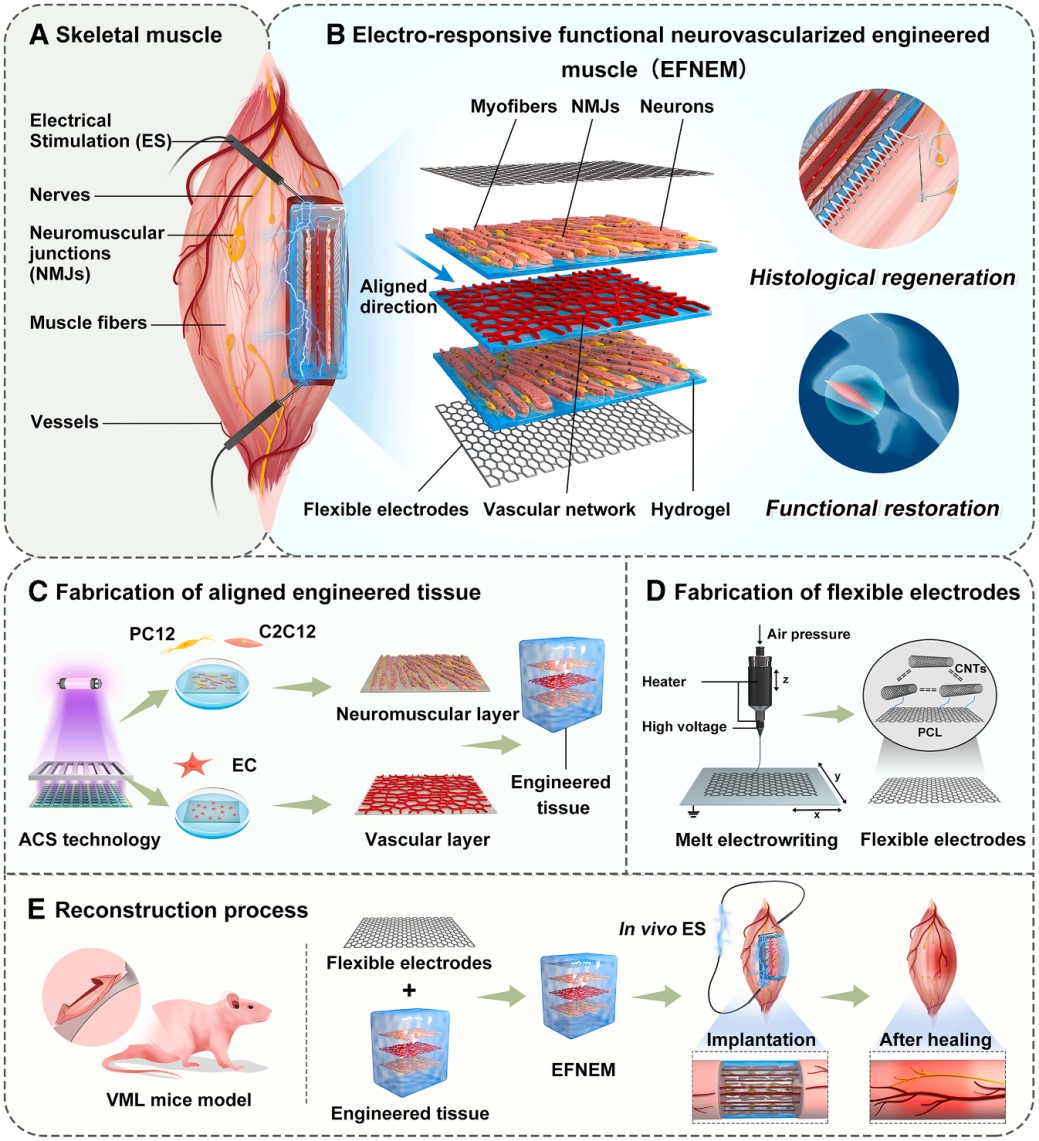
本研究基于天然骨骼肌再生的生物学原理,成功构建了神经血管化的肌肉组织。该构建体以定向微结构为形态学基础,同时实现神经-血管的同步化构建,并通过集成柔性电极实现体内精准电刺激递送,以协同加速工程组织与宿主组织的整合,进而促进肌肉功能恢复。 具体而言,研究采用光控定向细胞片(ACS)技术,模拟天然肌纤维基底膜的空间引导特性,构建了具备定向结构并整合神经血管化的工程肌肉。在此基础上,利用高精度3D打印技术制备超薄柔性电极,支持体内精准电刺激的应用。随后,通过水凝胶辅助的层层组装完成EFNEM的整体构建,并在小鼠VML模型中联合体内电刺激(ES)进行验证。结果表明,该多要素协同的功能化再生策略可加速VML后的神经支配,并显著提升肌肉功能恢复。
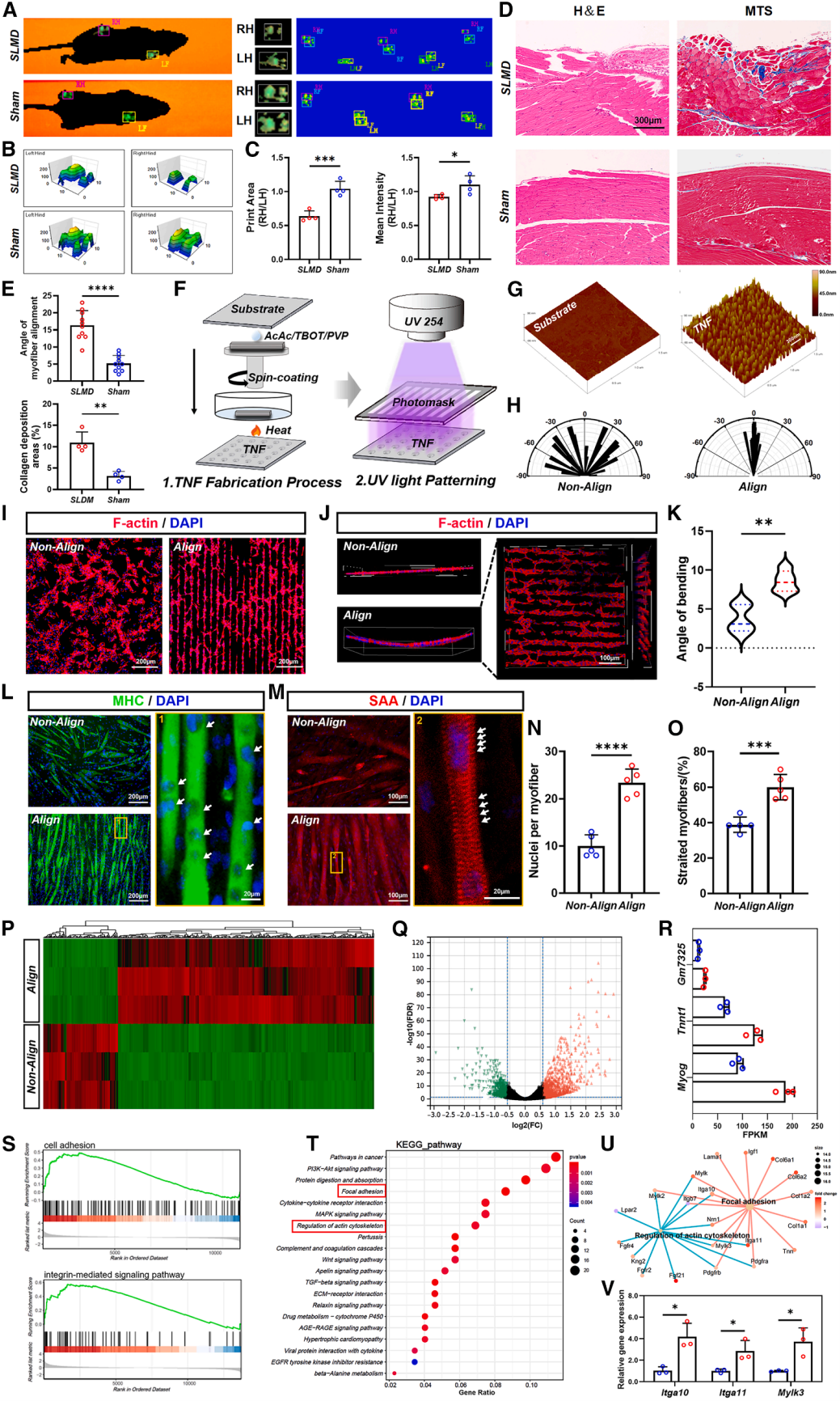
2、定向结构的构建
尽管骨骼肌具有一定的自我再生能力,但损伤后的自然修复往往难以实现功能的充分恢复。在小鼠自限性肌肉缺损(SLMD)模型中,术后4周的步态分析显示,其运动功能水平仍显著低于正常对照。组织学分析显示,新生肌纤维排列松散、取向紊乱,并伴有明显的瘢痕沉积;相比之下,正常组肌纤维结构致密且排列有序,这提示结构失序可能是制约功能恢复的重要因素。基于此,研究引入光控ACS技术调控成肌细胞定向排列。结果显示,定向培养显著增强了细胞排列一致性,并展现出更为协调的功能性表现;在诱导分化后,定向组形成的肌管排列规整、成肌表型增强。上述结果表明,通过工程化手段重建有序、定向的肌纤维结构,有助于促进成肌分化,并为后续功能恢复提供关键的结构基础。
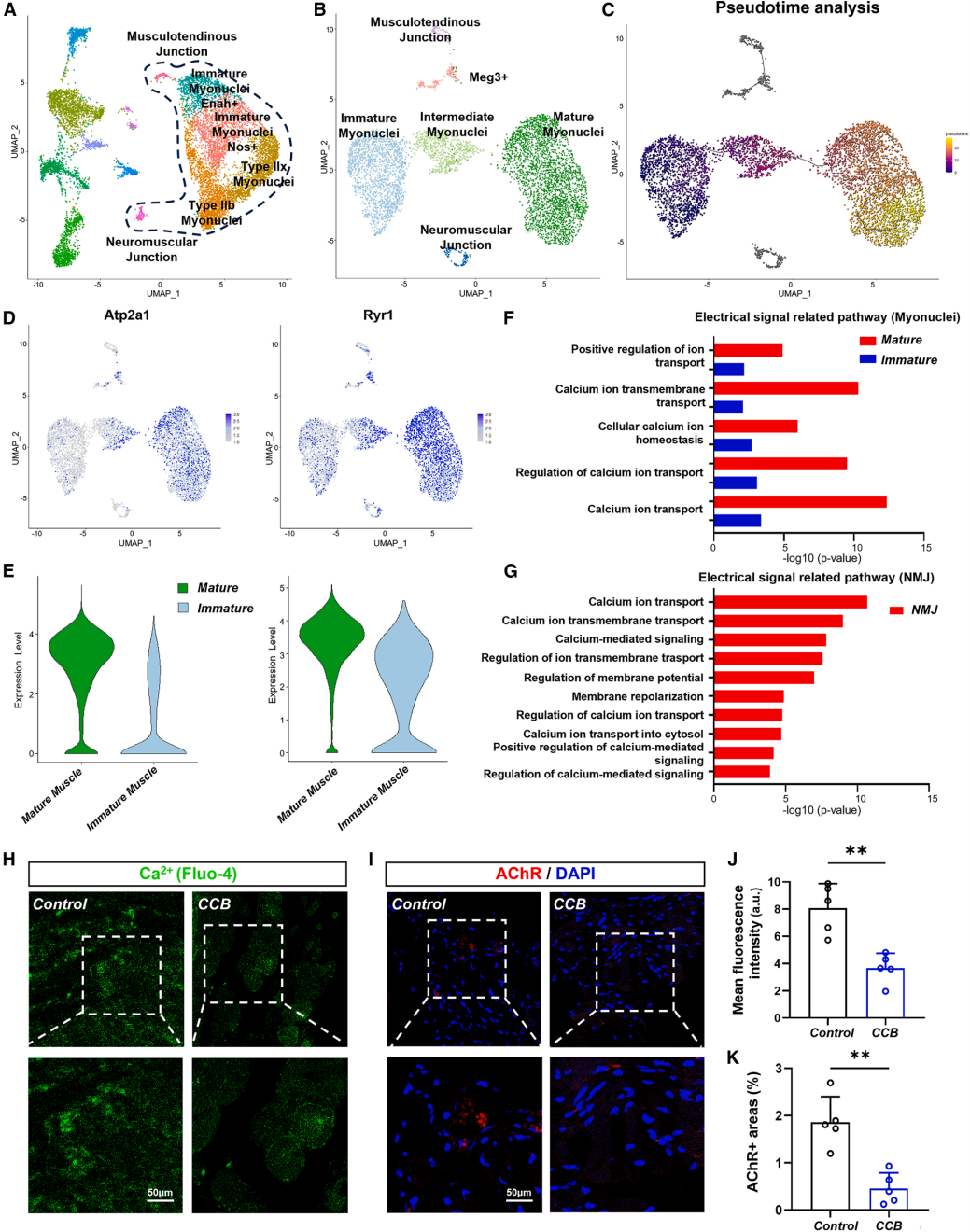
3、电信号的参与
进一步研究发现,仅依靠结构定向尚不足以驱动肌肉的功能成熟。定向肌管虽具备形态特征,但缺乏主动收缩能力;而在施加电刺激后,肌管可展现出协调的收缩反应,提示电信号在功能化过程中具有重要影响。基于这一现象,研究进一步从发育层面解析了生物电信号在骨骼肌成熟过程中的作用。单核转录组数据分析显示,随着肌细胞向成熟状态演进,与电活动相关的信号通路逐渐富集。进一步的体内研究表明,当电信号传导受到干扰时,肌肉成熟及神经肌肉接点(NMJ)的建立均会受到抑制,提示电信号在调控肌肉成熟及NMJ建立过程中发挥着关键作用。
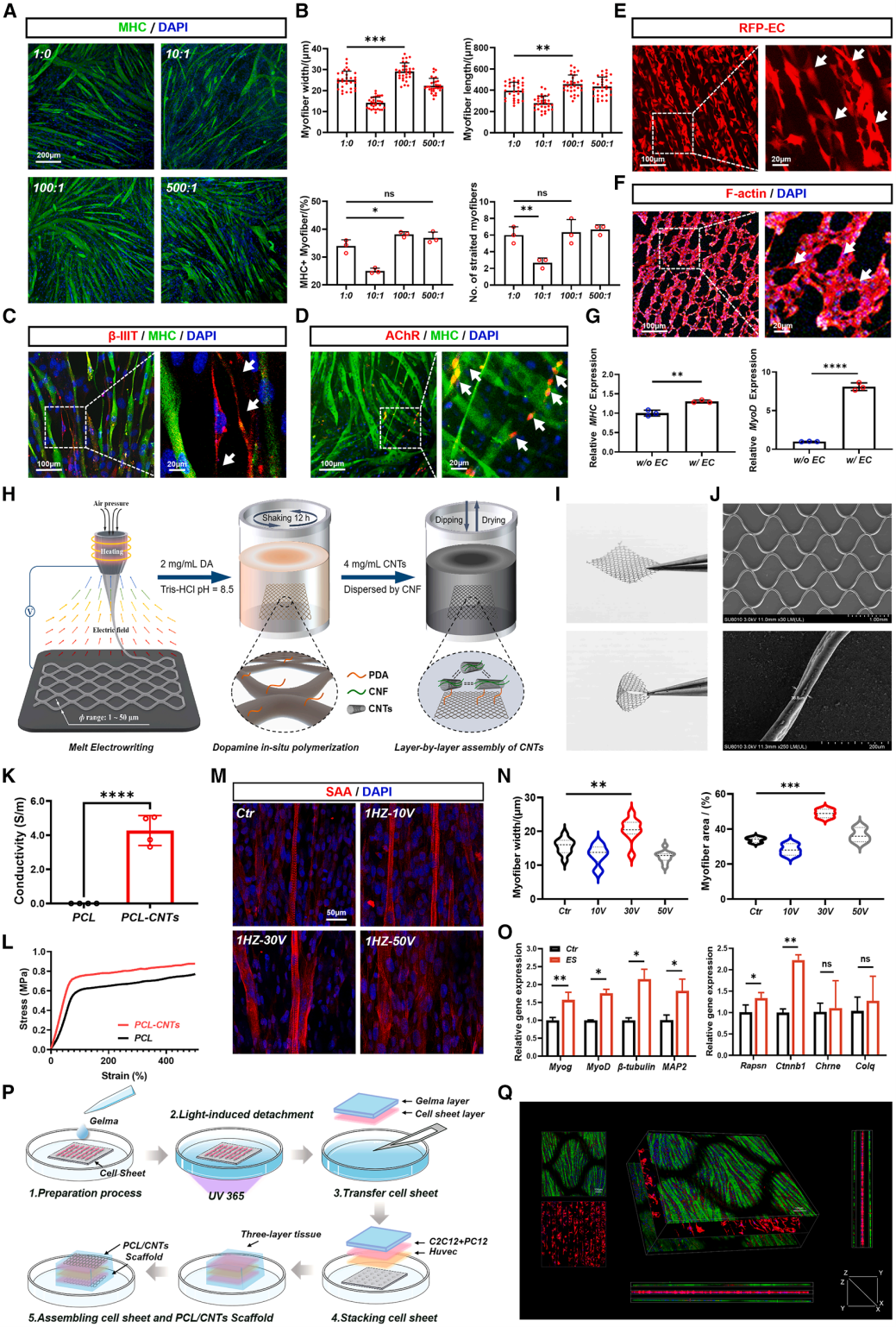
4、EFNEM的构建与应用
基于上述发现,研究团队制备了EFNEM,旨在支持肌肉的结构改善与功能提升。围绕神经血管化的再生目标,研究建立了体外神经–肌肉共培养体系,对不同共培养比例进行系统评估,并据此明确了合适的构建条件,进一步揭示其对NMJ相关结构形成的支持作用。同时,引入血管内皮细胞并采用一致的定向构建策略,形成结构有序的毛细血管样网络,以增强工程肌肉的血管再生能力。 为增强工程组织的导电性能并模拟天然骨骼肌的生理电微环境,研究进一步构建了基于聚己内酯与碳纳米管 (PCL/CNTs) 的柔性电极。该电极通过熔融电写(MEW)技术打印形成结构可控的PCL微纤维支架,并采用CNT层层涂敷工艺在纤维表面构建了连续导电网络。所得电极呈现超薄、网状结构,兼具良好的顺应性与导电性能,可在力学与结构层面与组织实现良好匹配。通过将该柔性电极与上述神经血管化工程组织一体化集成,最终形成兼具神经血管特征与电响应能力的EFNEM。
5、组织学再生
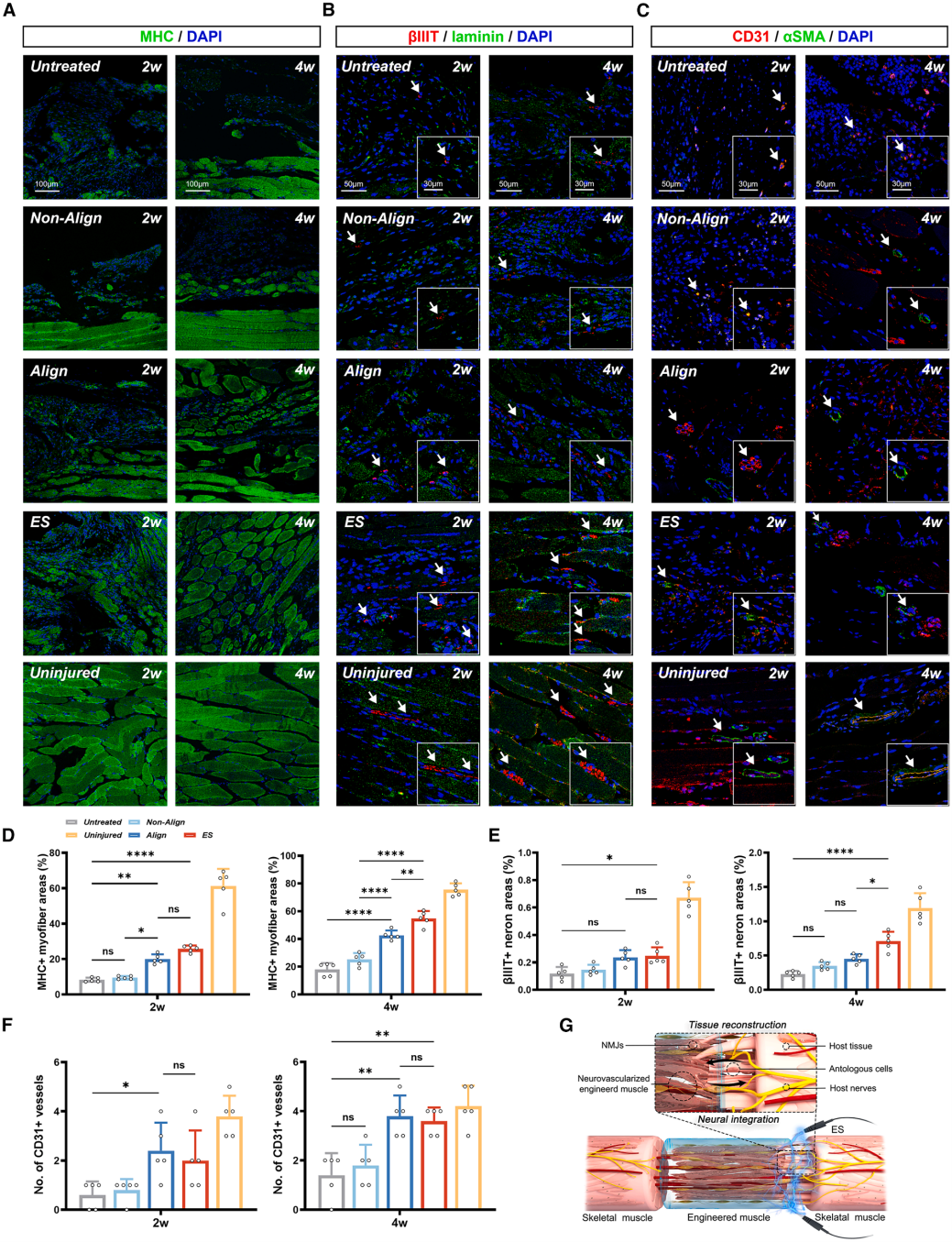
在小鼠VML模型中,采用EFNEM植入联合体内ES的修复策略,对组织学再生效果进行评价。H&E及Masson三色染色结果显示,未治疗缺损组出现明显的肌肉萎缩并伴随广泛纤维化,而接受工程组织植入的各组均表现出不同程度的组织再生。进一步分析提示,定向构建的工程组织可促进新生肌纤维形成并减少瘢痕沉积,在此基础上联合ES干预,可进一步改善肌纤维排列的规则性与整体形态完整性。
免疫荧光分析进一步揭示了神经与血管相关组织的再生情况。MHC染色显示,ES组中新生肌纤维形态更接近正常肌肉组织。βIII-tubulin/laminin共染表明再生区域内神经支配面积增加,Syn与AChR的染色进一步提示NMJ相关结构的重建,且ES组更为显著。血管相关染色显示,CD31+管腔结构在Align组和ES组中均明显增加。激光散斑血流成像则从功能动力学角度证实,ES组再生区域的血流灌注水平得到提升。
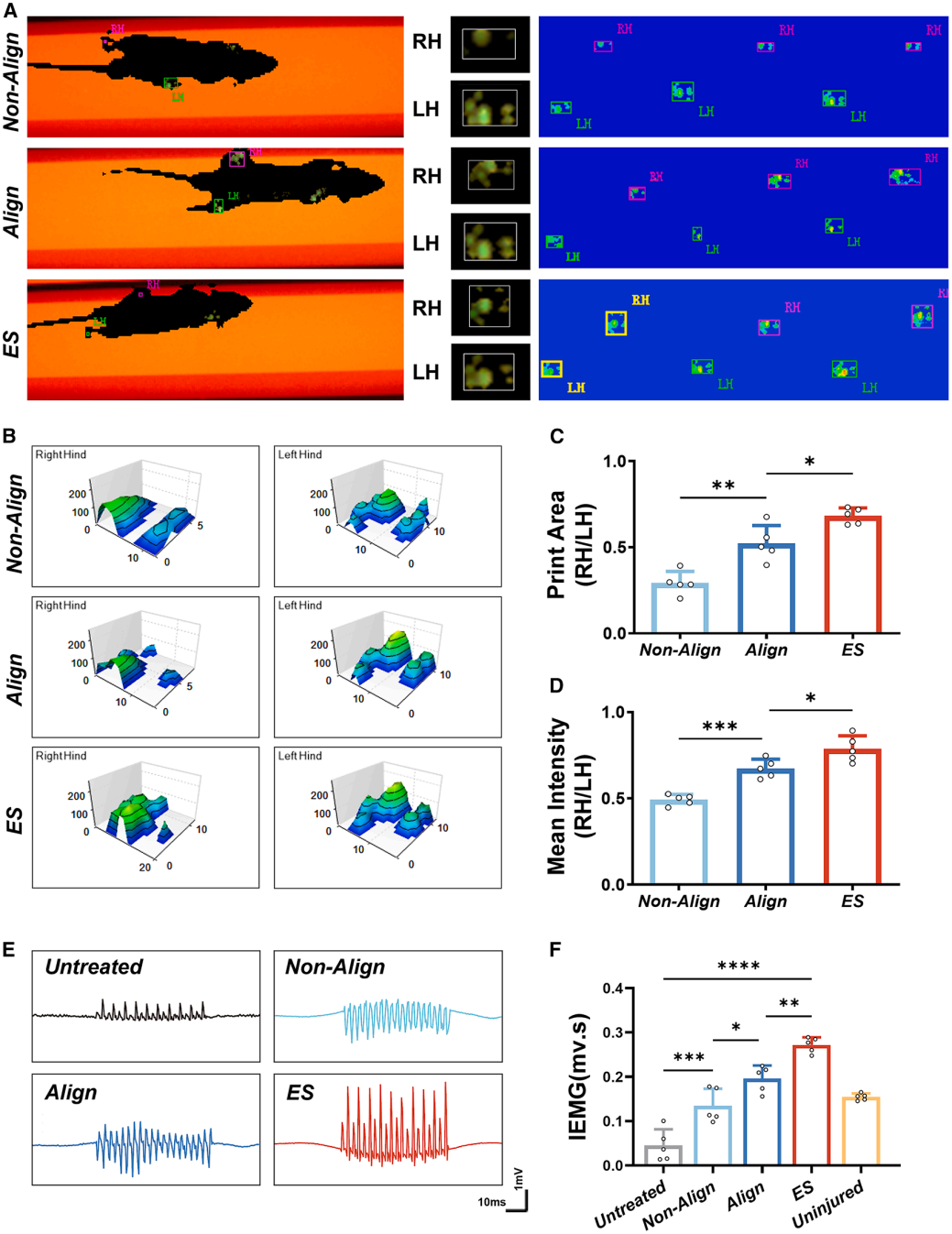
6、功能学恢复
为评估修复后的功能恢复情况,研究采用CatWalk步态分析系统对小鼠的运动能力进行定量评估。结果显示,与对照组相比,接受EFNEM植入联合ES治疗组表现出更接近正常水平的步态特征,其足印面积与步态强度均显著改善,反映出整体运动功能的实质性恢复。相比之下,单独ES而未植入EFNEM的对照组的功能改善幅度有限,表明工程组织与ES之间存在协同效应。 进一步通过肌电图(EMG)检测对神经肌肉兴奋性及信号传导能力进行评估。结果显示,ES组在肌肉收缩过程中表现出更高幅度的电生理响应,其积分肌电(iEMG)值高于其他处理组,提示其神经肌肉功能恢复程度更佳。综上所述,联合EFNEM植入与体内ES的综合治疗策略可有效改善运动性能,促进肌肉生理功能的恢复。
7、结论与展望
本研究围绕骨骼肌功能再生的关键需求,提出了一种融合生物学原理与工程化手段的功能化再生策略。通过将体外构建与体内重塑相结合,该研究验证了工程化组分与宿主系统生物整合的可行性,并揭示了结构引导、神经血管整合与电信号协同作用在推动肌肉功能重建中的潜力。这种多因素协同重建的思路,为功能性组织工程与再生医学的发展提供了新的方向。
原文链接:https://doi.org/10.1016/j.celbio.2025.100305
https://blog.sciencenet.cn/blog-2159320-1520177.html
上一篇:Pa级超软水凝胶的原位结晶3D打印方法
下一篇:“活体骨膜”:“信号接力”攻克难治性骨缺损