博文
超越血糖控制:治疗糖尿病的新目标揭晓  精选
精选
||
超越血糖控制:治疗糖尿病的新目标揭晓
诸平
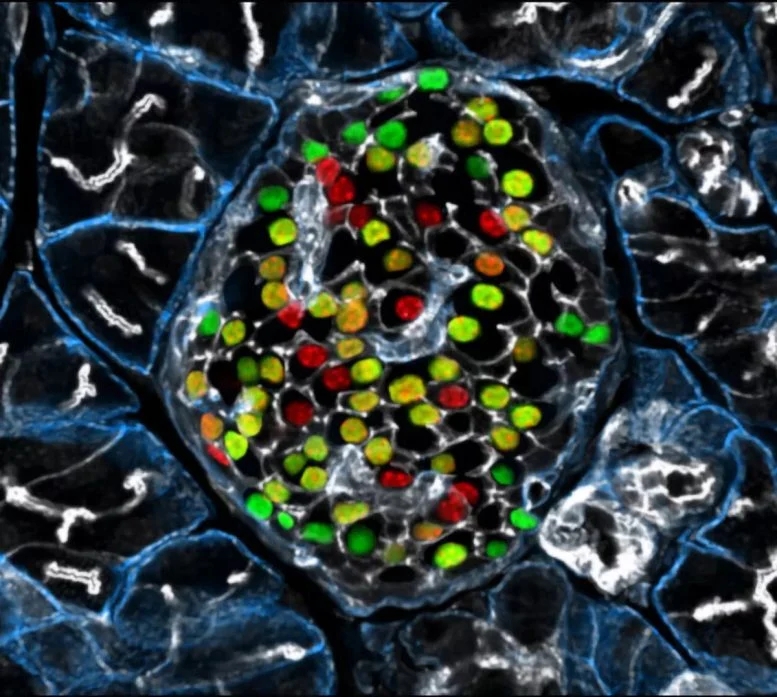
据德国亥姆霍兹慕尼黑中心(Helmholtz Zentrum München)2024年3月22日提供的消息,超越血糖控制:治疗糖尿病的新目标揭晓(Beyond Blood Sugar Control: New Target for Curing Diabetes Unveiled)。以inceptor受体(inceptor receptor)为目标,可以通过保护β细胞和改善血糖控制,为糖尿病的治疗带来突破性的进展,德国的研究机构领导了这一有希望的发现。上述图示是朗格汉斯胰岛(islet of Langerhans)内分泌胰岛素的β细胞。
对胰岛素抑制受体即inceptor (insulin-inhibitory receptor, known as inceptor)的研究揭示了保护β细胞的有希望的途径,为直接治疗糖尿病提供了乐观的希望。一项涉及饮食引起肥胖的小鼠的开创性研究表明,消除胰岛素抑制受体(inceptor)可以改善葡萄糖管理。这一发现鼓励进一步研究inceptor作为治疗2型糖尿病的潜在治疗靶点。相关研究结果于2024年2月28日已经在《自然-代谢》(Nature Metabolism)杂志网站发表——Gerald Grandl, Gustav Collden, Jin Feng, Sreya Bhattacharya, Felix Klingelhuber, Leopold Schomann, Sara Bilekova, Ansarullah, Weiwei Xu, Fataneh Fathi Far, Monica Tost, Tim Gruber, Aimée Bastidas-Ponce, Qian Zhang, Aaron Novikoff, Arkadiusz Liskiewicz, Daniela Liskiewicz, Cristina Garcia-Caceres, Annette Feuchtinger, Matthias H. Tschöp, Natalie Krahmer, Heiko Lickert, Timo D. Müller. Global, neuronal or β cell-specific deletion of inceptor improves glucose homeostasis in male mice with diet-induced obesity. Nature Metabolism, 2024, 6: 448–457. DOI: 10.1038/s42255-024-00991-3. Published: 28 February 2024. https://www.nature.com/articles/s42255-024-00991-3
参与此项研究的有来自德国纽赫伯格的慕尼黑亥姆霍兹中心(Helmholtz Zentrum München, Neuherberg, Germany)、德国慕尼黑亥姆霍兹中心糖尿病和肥胖研究所(Institute of Diabetes and Obesity, Helmholtz Center Munich, Neuherberg, Germany)、德国糖尿病研究中心(German Center for Diabetes Research, Neuherberg, Germany)、德国慕尼黑亥姆霍兹中心糖尿病与再生研究所(Institute of Diabetes and Regeneration Research, Helmholtz Center Munich, Neuherberg, Germany)、德国慕尼黑亥姆霍兹中心病理学及组织分析核心实验室(Core Facility Pathology & Tissue Analytics, Helmholtz Center Munich, Munich, Germany)、德国慕尼黑理工大学(Technische Universität München, Munich, Germany)、德国慕尼黑路德维希·马克西米利安大学医院(Klinikum der Universität, Ludwig-Maximilians-Universität München, Munich, Germany)以及德国慕尼黑大学沃尔特-斯特劳布药理学和毒理学研究所(Walther-Straub Institute of Pharmacology and Toxicology, LMU Munich, Munich, Germany)的研究人员。此研究推动了糖尿病研究的进展。
靶向胰岛素抑制受体对抗β细胞的胰岛素抵抗(Targeting Inceptor to Combat Insulin Resistance in Beta Cells)
胰岛素抵抗通常与腹部肥胖有关,在我们这个时代,这是一个重大的医疗困境。更重要的是,β细胞的胰岛素抵抗导致了它们的功能障碍和从肥胖到显性2型糖尿病的转变。目前,包括胰岛素补充在内的所有药物治疗都侧重于控制高血糖水平,而不是解决糖尿病的根本原因:β细胞衰竭或损失。因此,对β细胞保护和再生的研究至关重要,对于解决糖尿病的根本原因具有很好的前景,为病因治疗(causal treatment)提供了潜在的途径。
随着最近胰岛素抑制受体(Inceptor)的发现,β细胞专家海科·利克特(Heiko Lickert)教授的研究小组发现了一个有趣的分子靶点。在糖尿病中,胰岛素抑制受体(inceptor)的上调可能通过作为该信号通路的负调节因子而促进胰岛素抵抗。相反,抑制inceptor的功能可以增强胰岛素信号传导,这反过来又是β细胞整体功能、生存和应激补偿所必需的。
研究人员与肥胖和糖尿病分子药理学专家蒂莫·米勒教授(Prof. Timo Müller)合作,探索了inceptor敲除对饮食诱导的肥胖小鼠的影响。他们的研究旨在确定抑制inceptor功能是否也能提高饮食引起的肥胖和胰岛素抵抗的葡萄糖耐量,这两个阶段都是糖尿病进展的关键临床前阶段。
去除inceptor可改善肥胖小鼠的血糖水平(Removing Inceptor Improves Blood Sugar Levels in Obese Mice)
研究人员深入研究了从饮食诱导的肥胖小鼠的所有体细胞中去除inceptor的影响。有趣的是,他们发现缺乏inceptor的小鼠在没有体重减轻的情况下表现出更好的葡萄糖调节,这与葡萄糖反应增加的胰岛素分泌有关。接下来,他们研究了中枢神经系统中inceptor的分布,发现它在神经元中广泛存在。从神经细胞中删除inceptor也改善了肥胖小鼠的葡萄糖调节。最终,研究人员选择性地从小鼠的β细胞中去除inceptor,结果改善了葡萄糖控制,β细胞质量略有增加。
Inceptor阻断药物的研究(Research for Inceptor-Blocking Drugs)
蒂莫·米勒教授说:“我们的研究结果支持这样一种观点,即通过靶向inceptor来增强胰岛素敏感性,这是一种有希望的药理学干预,特别是关于β细胞的健康和功能。”与密集的早发性胰岛素治疗不同,利用inceptor增强β细胞功能有望减轻饮食引起的肥胖对血糖和代谢的有害影响。这种方法避免了低血糖相关的无意识风险和强化胰岛素治疗中常见的不必要的体重增加。
海科·利克特解释说:“由于inceptor在胰腺细胞表面表达,它成为一个可接近的药物靶点。目前,我们的实验室正在积极研究几种inceptor阻断药物的潜力,以增强糖尿病前期和糖尿病小鼠的β细胞健康。展望未来,inceptor作为一种新的和有趣的分子靶点出现,不仅在糖尿病前期肥胖个体中,而且在诊断为2型糖尿病的患者中,都可以增强β细胞的健康。”
本研究得到了欧洲研究委员会(European Research Council ERC-CoG trusted no.101044445; ERC, BetaRegeneration-101054564; CGC: STG grant AstroNeuroCrosstalk no. 757393; ERC AdG HypoFlam no. 695054)、德国科学基金会(German Research Foundation / Deutsche Forschungsgemeinschaft缩写DFG, grant nos. TRR296, TRR152, SFB1123 and GRK 2816/1; DFG under Germany’s Excellence Strategy within the framework of the Munich Cluster for Systems Neurology (EXC 2145 SyNergy—ID 390857198)、德国糖尿病研究中心(German Center for Diabetes Research / Deutsches Diabetes-Zentrum简称DDZ)、慕尼黑亥姆霍兹中心、亥姆霍兹协会(Helmholtz Association—Initiative and Networking Fund)、亚历山大·冯·洪堡基金会(Alexander von Humboldt Foundation)、亥姆霍兹联盟ICEMED(Helmholtz Alliance ICEMED)的资助或支持。
上述介绍,仅供参考。欲了解更多信息,敬请注意浏览原文或者相关报道。
Insulin resistance is an early complication of diet-induced obesity (DIO)1, potentially leading to hyperglycaemia and hyperinsulinaemia, accompanied by adaptive β cell hypertrophy and development of type 2 diabetes2. Insulin not only signals via the insulin receptor (INSR), but also promotes β cell survival, growth and function via the insulin-like growth factor 1 receptor (IGF1R)3,4,5,6. We recently identified the insulin inhibitory receptor (inceptor) as the key mediator of IGF1R and INSR desensitization7. But, although β cell-specific loss of inceptor improves β cell function in lean mice7, it warrants clarification whether inceptor signal inhibition also improves glycaemia under conditions of obesity. We assessed the glucometabolic effects of targeted inceptor deletion in either the brain or the pancreatic β cells under conditions of DIO in male mice. In the present study, we show that global and neuronal deletion of inceptor, as well as its adult-onset deletion in the β cells, improves glucose homeostasis by enhancing β cell health and function. Moreover, we demonstrate that inceptor-mediated improvement in glucose control does not depend on inceptor function in agouti-related protein-expressing or pro-opiomelanocortin neurons. Our data demonstrate that inceptor inhibition improves glucose homeostasis in mice with DIO, hence corroborating that inceptor is a crucial regulator of INSR and IGF1R signalling.
https://blog.sciencenet.cn/blog-212210-1427014.html
上一篇:开发世界首个肺癌疫苗的新资金
下一篇:拓扑绝缘体中的奇偶校验异常