博文
好吃货并非对每个人都安全——绿茶提取物的隐藏风险
||
好吃货并非对每个人都安全——绿茶提取物的隐藏风险
诸平
关于绿茶提取物(Green Tea Extract)网络上的介绍很多,主要有效成分为茶多酚,主要包含儿茶素(EGCG),是主要存在于茶叶中的一种多酚成分,占茶叶的8%-20%,它是茶中一种重要的具有保健作用的化学成分。现在,茶多酚已经广泛应用在食品、化妆品和医药工业。绿茶提取物药用功效:降血压、抗血凝、降血脂、减肥、防治动脉粥样硬化和血栓形成等心血管病、降血糖、防治糖尿病、杀菌抗病毒;防治肝炎、脂肪肝、抗衰老和增强免疫机能;抗癌、抗过敏、预防感冒、预防骨折等。关于EGCG的研究,以Dimensions数据库为例,1985年之前每年收录的相关研究在10项以下,之后超过10项;1997年超过200项,2004年979项,2005年超过1100项,之后几乎直线上升,详见图2所示。
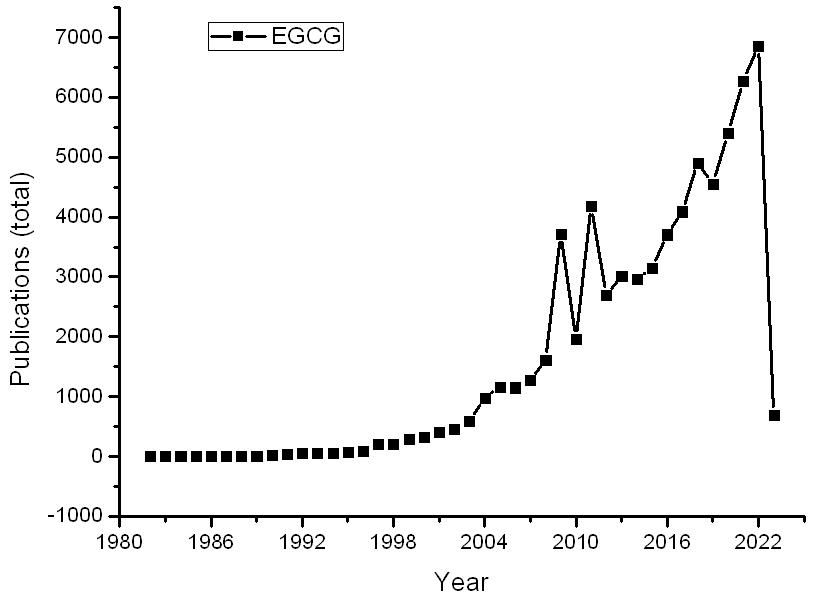
图2 Dimensions数据库收录EGCG相关成果数量之变
但是,美国罗格斯大学(Rutgers University)2023年1月26日的报道,明确指出“并非对每个人都安全:绿茶提取物的隐藏风险”(Not Safe for Everybody: The Hidden Risk of Green Tea Extract),对其报道内容,编译如下,仅供参考。
新研究表明,绿茶提取物会对一小部分人群造成肝损伤。虽然长期服用高剂量绿茶提取物可能对癌症、心血管疾病、肥胖症和2型糖尿病有一定的保护作用,但它也可能对一小部分人造成肝损伤。
究竟是谁有风险?发表在《膳食补充剂杂志》(Journal of Dietary Supplements)上的罗格斯大学的研究提供了第一个可靠线索:预测某些风险的两种遗传变异。详见Laura Acosta, Laura Byham-Gray, Mindy Kurzer, Hamed Samavat. Hepatotoxicity with High-Dose Green Tea Extract: Effect of Catechol-O-Methyltransferase and Uridine 5’-Diphospho-glucuronosyltransferase 1A4 Genotypes. Journal of Dietary Supplements, Published online: 30 Sep 2022. DOI: 10.1080/19390211.2022.2128501. https://www.tandfonline.com/doi/full/10.1080/19390211.2022.2128501
该研究的资深作者、罗格斯大学的注册营养师和助理教授Hamed Samavat说:“学习预测谁会遭受肝损伤可能很重要,因为越来越多的证据表明,高剂量绿茶提取物可能对那些可以安全服用的人有显著的健康益处。”罗格斯大学卫生职业学院(Rutgers School of Health Professions)营养科学专业助理教授Hamed Samavat的研究方向,是饮食因素以及膳食补充剂在癌症和心血管疾病病因学和预防中的作用。
利用来自美国明尼苏达绿茶试验(Minnesota Green Tea Trial)的数据,这是一项关于绿茶对乳腺癌影响的大型研究,研究小组调查了具有某些遗传变异的人在摄入量(843 mg/d)一年后,是否比其他人更容易出现肝脏压力的迹象。摄入物是绿茶中主要的抗氧化剂,一种称为表没食子儿茶素没食子酸酯 (epigallocatechin gallate简称EGCG),也就是儿茶素。
由劳拉·阿科斯塔(Laura Acosta)领导的此项研究,劳拉·阿科斯塔当时还是是一名博士生,现在已经从罗格斯大学完成临床营养学博士学位毕业,在美国佛罗里达大学(University of Florida)担任营养学高级讲师,她也是一名注册营养师。他们小组选择了两个有问题的遗传变异,因为每个变异都控制着一种分解EGCG的酶的合成。他们选择了明尼苏达绿茶试验,因为它是一项针对特定人群的大型、精心设计的研究。这项为期一年的安慰剂对照试验包括1000多名绝经后妇女,并收集了3、6、9和12个月的数据。
研究人员的一项分析表明,在儿茶酚-O-甲基转移酶 (catechol-O-methyltransferase简称COMT) 基因型有一种变异的女性中,肝损伤的早期迹象比正常女性更常见,并且尿苷5'-二磷酸-葡萄糖醛酸转移酶1A4(uridine 5’-diphospho-glucuronosyltransferase 1A4简称UGT1A4)基因型的变异强烈预测了这一点。
平均而言,具有高风险UGT1A4基因型的参与者在服用绿茶补充剂9个月后看到指示肝脏压力的酶上升了近80%,而具有低风险基因型的参与者看到相同的酶上升了30%。
Hamed Samavat说:“我们距离预测谁可以安全地服用高剂量绿茶提取物还有很长的路要走,”他指出,肝毒性风险仅与高水平的绿茶补充剂有关,与饮用绿茶,甚至服用较低剂量的绿茶提取物无关。“这一基因型的变异并不能完全解释研究参与者肝酶变化的变异。完整的解释可能包括许多不同的遗传变异,也可能包括许多非遗传因素。”
Hamed Samavat 继续说道:“尽管如此,我们确实认为我们已经确定了一个重要的难题,并朝着预测谁可以安全地享受高剂量绿茶提取物提供的任何健康益处迈出了一步。”
这项工作由美国国立卫生研究院(National Institutes of Health简称NIH)/国家癌症研究所(National Cancer Institute)资助{NIH/National Cancer Institute under Grant R01 CA127236}。
上述介绍,仅供参考。欲了解更多信息,敬请注意浏览原文或者相关报道。
The predominant catechin in green tea, epigallocatechin gallate (EGCG), may be hepatotoxic in high doses. Our objective was to investigate the influence of catechol-O-methyltransferase (COMT) and uridine 5’-diphospho-glucuronosyltransferase 1A4 (UGT1A4) genotypes on changes in liver injury biomarkers in response to long-term, high-dose green tea extract (GTE) supplementation among postmenopausal women. A secondary analysis was conducted using data from the Minnesota Green Tea Trial (N = 1,075), in which participants were randomized to consume high-dose GTE (843 mg/day EGCG) or placebo capsules for 12 months. Analysis of covariance adjusting for potential confounders was performed to examine changes in aspartate aminotransferase (AST), alanine aminotransferase (ALT), AST: ALT ratio, and alkaline phosphatase from baseline to months 3, 6, 9, and 12 across COMT and UGT1A4 genotypes. Mean age and BMI within the GTE group (n = 400) were 59.8 yrs and 25.1 kg/m2, respectively, and 98% of subjects were white. From baseline to month 3, mean AST: ALT ratio change was +1.0% in the COMT (rs4680) A/G genotype versus −4.8% in the A/A genotype (p = 0.03). From baseline to months 6 and 9, respectively, mean ALT change was +78.1% and +82.1% in the UGT1A4 (rs6755571) A/C genotype versus +28.0% and +30.1% in the C/C genotype (p<0.001 and p=0.004, respectively). The UGT1A4 (rs6755571) A/C genotype may be an important risk factor for clinically-relevant serum transaminase elevations with 6-9 months of high-dose GTE supplementation among postmenopausal women. Understanding the genetic underpinnings of GTE-related hepatotoxicity may allow for a genetically-informed paradigm for therapeutic use of GTE.
https://blog.sciencenet.cn/blog-212210-1374212.html
上一篇:《自然》:材料发现的革命性新方法
下一篇:设计抗癌药物的操作指南
