博文
磁热疗诱导的氢疗法机器人
||
磁热疗诱导的氢疗法用于癌症治疗:基于 PEG 包覆 Mg–Ni 可降解微机器人
作者单位分别是韩国大邱庆北科学技术院(DGIST)机器人与机电一体化工程系,大邱庆北科学技术院(DGIST)DGIST‑ETH 微机器人研究中心,大邱庆北科学技术院(DGIST)新生物学系,美国马萨诸塞大学阿默斯特分校生物医学工程系应用生命科学研究所
亮点
- 镁基微机器人可通过外部磁场进行精确控制。
- 温和热疗可触发氢疗法的激活。
- 磁控制和热疗协同实现局部氢治疗。
- 氢疗法显著提高抗癌治疗效果。
摘要
基于镁的微马达用于氢疗法,为治疗癌症、糖尿病和阿尔茨海默病等与活性氧(ROS)水平升高相关的疾病提供了一种有前景的策略。然而,它们在生理环境中的不可控运动和高反应性限制了其临床应用。为克服这些挑战,我们开发了一种聚合物包覆、磁引导的镁(Mg)微机器人,将氢疗法与磁热疗相结合。聚合物涂层确保其在磷酸盐缓冲液(PBS)中的稳定性,而微机器人在 15 mT、10 Hz 的旋转磁场下可达到 18.63 ± 0.85 μm/s 的速度。温和的磁热(约 43 °C)可部分熔化聚合物外壳,从而触发氢释放。对 HCT 116 细胞的体外研究表明,在磁热疗后,3 mg/mL 的微机器人可显著降低 ROS。小鼠体内实验显示,该微机器人可减轻氧化应激并显著减小肿瘤体积。这些结果表明,Mg 基微机器人是一种可控且有效的 ROS 相关疾病治疗平台。
引言
微/纳米机器人作为靶向药物递送平台,正越来越受到关注,可用于治疗癌症、帕金森病和阿尔茨海默病等多种疾病[[1], [2], [3]]。癌症仍然是全球主要死因之一。尽管化疗被视为癌症治疗的金标准,但其靶向递送困难和严重副作用限制了其疗效[[4], [5], [6], [7]]。先前的研究探索了使用无束缚医疗微/纳米机器人进行高效抗癌药物递送,以克服这些限制[8,9]。尽管这些微机器人表现良好,但它们不可降解,长期暴露可能引起局部炎症[10,11]。
癌细胞与活性氧(ROS)生成增加相关[[12], [13], [14]]。癌细胞中升高的 ROS 不仅具有致癌作用,还能促进异常细胞生长、转移、血管生成和抗凋亡能力[7,15,16]。最近的研究表明,降低癌细胞中升高的 ROS 水平可以破坏氧化还原稳态并诱导凋亡[17,18]。因此,ROS 清除已被提出作为一种新的癌症治疗策略。
气体疗法已成为癌症治疗的替代方法[19,20],其中氢气因其安全性和治疗效果而受到特别关注[[21], [22], [23]]。氢气已被证明是一种强效抗氧化剂,能够清除病变细胞产生的细胞毒性 ROS[[24], [25], [26]]。目前,氢气正被研究用于治疗癌症[27,28]、2 型糖尿病[29,30]、关节炎[31,32]和神经系统疾病[33,34]。尽管其抗炎特性已得到充分证实,但氢的抗肿瘤作用的确切机制仍知之甚少。
最近的研究表明,调节线粒体功能可能是分子氢抗肿瘤作用的机制之一[35]。它通过提高电子传递链效率、维持膜电位和优化细胞能量代谢来帮助恢复线粒体稳态[36,37]。这些改善可抑制异常增殖信号,并增加癌细胞对凋亡的敏感性。
氢通过选择性清除 ROS 而不影响正常细胞,从而抑制肿瘤生长并破坏氧化还原稳态[27,38,39]。它可与羟自由基(·OH)和过氧亚硝酸盐阴离子(ONOO−)反应,从而降低氧化应激。此外,氢通过下调促炎细胞因子发挥抗炎作用。其抗氧化活性归因于清除 ·OH 和 ONOO−,以及上调内源性抗氧化酶和过氧化氢酶[25,40]。然而,氢在生理液体中的固有低溶解度可能限制其治疗潜力。因此,已开发多种氢载体用于靶向、可控和高效递送,例如氢化钯(PdH0.2)、MgB2 纳米片和 Fe 纳米颗粒[[41], [42], [43]]。例如,Xu 等人报道,近红外激活的 PdH0.2 纳米口袋立方体通过增强氢向斑块的扩散来抑制动脉粥样硬化,从而促进脂质外流并抑制疾病进展[44]。Kou 等人开发了羧甲基纤维素包覆的铁颗粒,可在酸性环境中释放氢,用于癌症治疗[41]。然而,这些方法主要依赖于载氢的不可降解微/纳米颗粒,其负载能力、组织穿透性和生物相容性有限。此外,现有的氢递送技术依赖被动扩散,这可能阻碍氢在水溶液中的溶解效率。
可降解金属已被研究作为解决这些问题的替代方案。它们与体液反应可释放高纯度氢气[11,45]。镁(Mg)因其良好的生物相容性、已证实的高饮食耐受性以及在生理溶液中的可降解性而受到广泛关注[[46], [47], [48]]。此外,Mg 还作为约 300 种参与多种代谢过程的酶的辅因子[49,50]。因此,Mg 基 Janus 微马达因其在生理液体中的自推进能力而成为一种有前景的药物递送平台。最近的多项研究证明了 Mg 基微马达在治疗癌症、关节炎和其他疾病方面的潜力[[51], [52], [53]]。然而,这些研究大多依赖气泡反冲推进技术,且缺乏对微马达运动的精确控制。此外,Mg 微马达暴露于体液后会立即释放氢,从而缩短其寿命并阻碍有效的靶向递送。因此,有必要开发策略来延长 Mg 微马达的功能寿命,并实现氢向目标部位的精确递送。
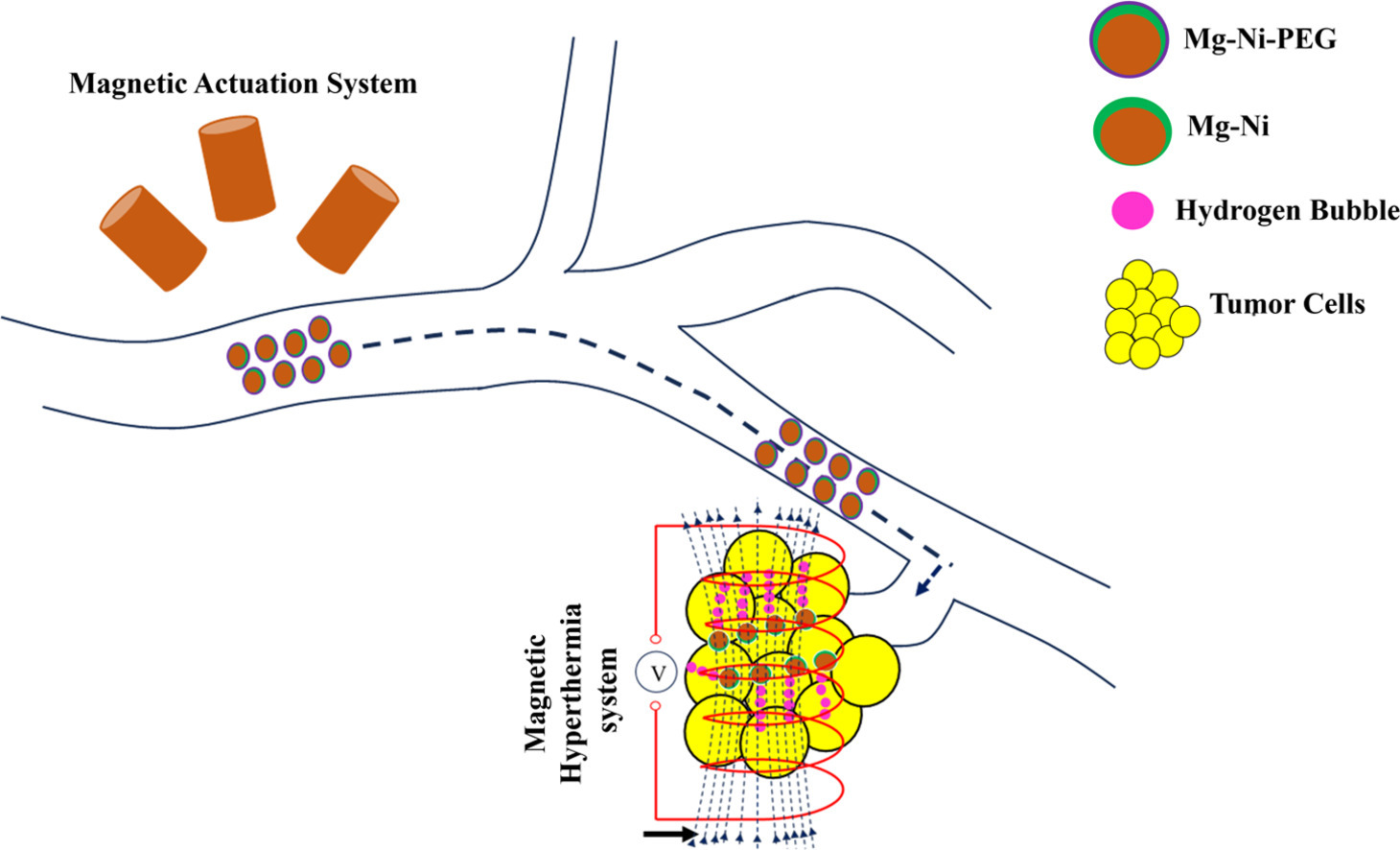
在此,我们开发了一种聚乙二醇(PEG 1500)包覆的磁引导镁‑镍(Mg–Ni)微机器人,用于基于氢的癌症治疗。该微机器人由不对称的 Mg 和 Ni 层组成,并被 PEG 1500 包裹,可通过磁场导航至目标部位。到达后,温和的磁热疗(约 43 °C)可部分熔化 PEG 外壳,使 Mg–Ni 微粒暴露并与生理液体反应生成氢。释放的氢具有增强的扩散能力,可有效清除 ROS。对 HCT 116 细胞的体外研究证实,热疗后 ROS 显著降低。此外,在裸鼠皮下肿瘤模型中的体内研究表明,该微机器人可显著减小肿瘤大小,显示出对氧化应激相关癌症的强大治疗潜力。
https://blog.sciencenet.cn/blog-41174-1518127.html
上一篇:开放科学运动真的如支持者所言那般有益吗?
下一篇:AI 模型竟然会患心理疾病!