博文
代谢健康型肥胖:事实与幻想  精选
精选
|
尽管肥胖通常与代谢功能障碍和心血管代谢疾病相关联,但一些肥胖的人却免受多余体脂肪的许多不良代谢影响,被认为是“代谢健康”。然而,目前还没有一个普遍接受的代谢健康型肥胖(MHO)的定义。大多数研究将MHO定义为具有0、1或2个代谢综合征成分,而许多其他研究使用胰岛素抵抗的稳态模型评估(HOMA-IR)来定义MHO。因此,许多被报告为MHO的人并不是真正的代谢健康,而仅仅是比那些患有代谢不健康型肥胖(MUO)的人拥有更少的代谢异常。尽管如此,一小部分肥胖的人具有正常的HOMA-IR且没有代谢综合征成分。肥胖对代谢健康产生不同影响的机制尚不清楚,但在啮齿动物模型中进行的研究表明,体重增加时脂肪组织的生物学差异可能导致或防止系统性代谢功能障碍。在本文中,我们回顾了MHO的定义、随时间的稳定性以及临床结果,并讨论了可能解释MHO和MUO人群中代谢健康差异的潜在因素——特别是可改变的生活方式因素和脂肪组织生物学。更好地理解区分MHO和MUO人群的因素可以为理解肥胖相关的代谢功能障碍和疾病的机制提供新的洞见。
Smith GI, Mittendorfer B, Klein S. Metabolically healthy obesity: facts and fantasies. J Clin Invest. 2019 Oct 1;129(10):3978-3989.
引言
肥胖经常与一系列代谢异常有关,包括胰岛素抵抗、糖尿病前期、动脉粥样硬化性血脂异常(高血浆甘油三酯[TG]和低高密度脂蛋白胆固醇[HDL-C]浓度)、非酒精性脂肪肝病和代谢综合征,这些都是2型糖尿病(T2D)和心血管疾病(CVDs)的重要风险因素(1, 2)。然而,并非所有肥胖的人都伴有代谢并发症,这就提出了一个问题:那些代谢健康的肥胖者是代表了一个独特的肥胖人群子集,还是仅仅是一个正在向发展成代谢不健康型肥胖(MUO)过渡的群体。在本文中,我们将探讨这样一个前提,即很少有肥胖的人真正代谢健康,并评估潜在的可改变因素(饮食、体育活动和睡眠)和涉及决定过量脂肪沉积代谢效应的脂肪组织因素。为此,我们将首先回顾代谢健康型肥胖(MHO)的定义、流行率、稳定性和临床结果的背景,然后讨论可能解释MHO和MUO人群中代谢健康差异的潜在因素。
代谢健康型肥胖的定义
目前还没有一个普遍接受的标准来定义MHO,不同的研究中使用了超过30种不同的定义(表1)。在大多数研究中,MHO被定义为具有以下五个代谢综合征成分中的≤2个:高收缩压和舒张压、高血浆TG浓度、低HDL-C浓度、高空腹血糖和大腰围;或者排除腰围后具有≤1个异常成分。其他标准,包括高血浆总胆固醇、LDL-胆固醇和C反应蛋白浓度,口服葡萄糖耐量测试期间的2小时血糖浓度,以及基于胰岛素抵抗的稳态模型评估(HOMA-IR)分数、Matsuda指数(全身胰岛素敏感性指数)、高胰岛素-正常血糖钳夹程序(HECP)中的葡萄糖输注速率和胰岛素抑制测试等胰岛素敏感性/抵抗性的指标,也被用来判定MHO。在一些研究中,即使是有糖耐量受损、T2D和CVD病史的人也被视为代谢健康,因为他们没有足够数量的指定代谢异常被识别为MUO。因此,被报告为MHO的人通常并不是真正的健康,而仅仅是比被定义为MUO的人拥有更少的心血管代谢异常。因此,需要一个更严格且普遍接受的MHO定义,以确定MHO的真实流行率和长期后果,并进行研究阐明保护某些肥胖人士免受多余体脂肪不良代谢影响的保护机制。
表1用于识别代谢健康型肥胖的变异性标准示例

我们提出了一套严格的标准来识别MHO人群(表2),基于以下条件:(a)无心血管代谢疾病,(b)健康的心血管代谢血液特征,(c)正常血压,(d)正常的肝内甘油三酯含量,以及(e)正常的胰岛素敏感性。我们将这些标准分为那些在典型的门诊临床设置中可以轻易获得的标准(基本标准)和那些需要更复杂测试的研究设置中可用的标准(高级标准)。我们提出一个比诊断代谢综合征所使用的血浆甘油三酯浓度“切割点”更低的值(即<95 mg/dL vs. <150 mg/dL),这是基于标志着从大型低密度LDL颗粒转变为高致动脉粥样化的小而密集LDL颗粒的血浆甘油三酯浓度。我们还建议包含对胰岛素敏感性的评估,定义为在高胰岛素-正常血糖钳夹程序(HECP)期间维持正常血糖所需的葡萄糖输注速率,因为许多对胰岛素有抵抗的肥胖人士由于血浆胰岛素的代偿性增加,可能会有正常的空腹血浆葡萄糖浓度和正常的口服葡萄糖耐量。我们选择了一个之前用于定义MHO且与BMI为25 kg/m^2且代谢健康的人群中报告的均值相似的葡萄糖输注速率切割值。
表2 代谢健康型肥胖的定义标准

代谢健康型肥胖的流行率
代谢健康型肥胖(MHO)的流行率取决于用于定义代谢健康的准则,是否在研究前排除了患有2型糖尿病(T2D)或心血管疾病(CVD)的人群,以及研究人群的性别、年龄、BMI范围和种族或民族背景。这些变量的差异很可能是造成报告流行率巨大差异的原因,当代谢健康的准则基于测量变量时,成人肥胖的流行率范围从6%到60%(见补充表1-4),而主要基于自报数据时高达75%。一般来说,MHO在女性中比男性更常见,在年轻人中比老年人更常见,在BMI小于35 kg/m^2的人群中比BMI为35 kg/m^2或更高的人群中更常见,在欧洲血统的人中比来自非洲、南美和南亚(印度血统)的人更常见。根据北美和欧洲队列研究中选择标准的严格程度对MHO流行率的估计如图1和补充表1-4所示。将MHO定义为“正常”胰岛素敏感性(基于HOMA-IR分数)且没有任何代谢综合征成分(不包括腰围)的流行率约为7%,而当定义为≤2个代谢综合征成分(包括腰围)时,所有肥胖人士中约有一半可以被归类为MHO。然而,由于许多研究排除了已有心血管代谢疾病的人群,如T2D和CVD,因此这些结果很可能高估了一般人群中MHO的流行率。
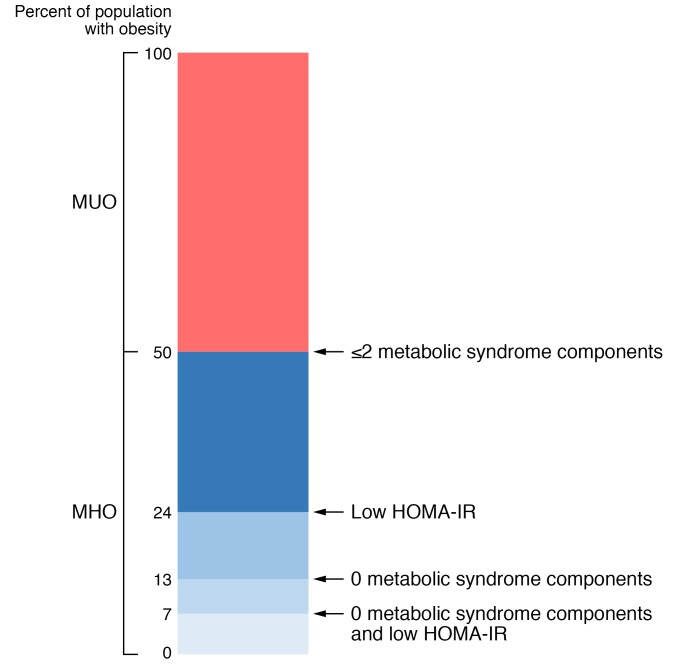
图1基于代谢综合征标准的数量和胰岛素敏感性评估(使用稳态模型评估胰岛素抵抗[HOMA-IR]分数),在北美和欧洲肥胖人群中代谢健康型和代谢不健康型肥胖的估计流行率。
数据来源于33项研究,共涉及123,548名肥胖人群,详细描述见补充材料(本文附带的在线补充材料)。
随时间推移代谢健康型肥胖的稳定性
随着年龄增长代谢健康的正常下降、长期过量脂肪堆积的代谢损害以及中年期间体重增加的趋势很可能影响MHO的稳定性。纵向研究的数据表明,大约30%到50%的MHO人群在随访4到20年后转变为MUO。MHO向MUO转变的主要因素是胰岛素敏感性下降和空腹血糖升高。从MHO转变为MUO的风险在那些BMI较高、年龄较大、有更严重代谢功能障碍证据(即异常代谢标准的数量和接近正常范围上限的值,以及存在肝脂肪变性)、生活方式指数差(饮食成分、休闲时间体育活动和吸烟的综合指标)以及观察期间体重增加的人中更大。
代谢健康型与不健康型肥胖的临床结果
一般来说,MUO人群患T2D、CVD和全因死亡率的风险比MHO人群和代谢健康且体重正常(MHL)的人群都要大,而MHO人群的这些风险又比MHL人群大。此外,这些不良结果的风险与代谢异常的数量和严重程度直接相关。
2型糖尿病
大多数研究的数据显示,与MHL人群相比,MUO人群发展为T2D的风险高出5至20倍。MHO人群发展为T2D的风险远低于MUO人群,但仍比MHL人群高出约4倍,并且与基线时的代谢异常数量直接相关。在为期6年的随访研究中,与MHL个体相比,基线时没有任何代谢综合征成分的MHO人群发展为T2D的风险仍然增加,但如果代谢状态在整个研究期间保持稳定,则风险不会增加。
心血管疾病
MHO人群的CVD事件(新发心绞痛、致命和非致命性心肌梗死、突发心脏死亡、致命和非致命性心力衰竭以及外周血管疾病)风险低于MUO人群,但仍然高于MHL人群。一项汇集了18项研究数据的元分析发现,基线时MHO人群的CVD事件风险比MHL人群高出约50%。发展CVD事件的风险与基线时的代谢异常数量直接相关,以及MHO表型是否保持稳定或转变为MUO。例如,在一项研究中,保持稳定MHO表型的参与者在中位数12年的随访期间的CVD事件风险与MHL参与者没有差异。
全因死亡率
MHO人群的全因死亡率风险低于MUO人群。与MHL人群相比,MHO人群的全因死亡率风险取决于代谢异常的数量和严重程度以及代谢健康的稳定性。五项大型队列研究的合并数据显示,平均随访13年,没有代谢综合征成分(不包括腰围)的MHO人群与MHL组相比,全因死亡率风险没有增加;然而,当将具有一个异常代谢风险因素(不包括腰围)的参与者包括在MHO组中时,与MHL相比,MHO参与者的全因死亡率风险更大。
代谢健康肥胖与代谢不健康肥胖的选定特征
与MUO相关的特征如图2所示。在这些特征中,多器官胰岛素抵抗(损害胰岛素介导的肝脏葡萄糖产生抑制、脂肪组织脂解活性抑制和肌肉葡萄糖摄取刺激)可能是导致心血管代谢疾病发展的最重要潜在因素。在非糖尿病患者中,通过HECP评估的全身胰岛素敏感性与BMI成反比;然而,在任何给定的BMI值上,胰岛素敏感性存在相当大的异质性,以至于一小部分肥胖人群的胰岛素敏感性与瘦人一样。MHO人群的胰岛素敏感性高于MUO人群,许多被识别为MHO的参与者比MHL的人更具胰岛素抵抗性,表现为更高的空腹血浆胰岛素浓度、口服葡萄糖耐量测试中的血糖浓度和HOMA-IR值。与MUO相比,MHO人群中胰岛素作用更大程度保留的因素尚不清楚,但可能与潜在的可改变的生活方式因素和脂肪组织生物学的改变有关。在这一部分中,我们将重点回顾这些领域,主要关注脂肪组织生物学。
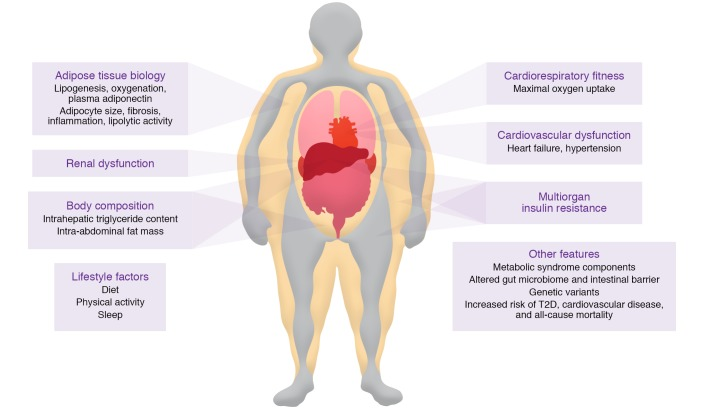
图2 与代谢健康型肥胖人群相比,代谢不健康型肥胖人群具有的独特特征。
然而,由于数据不足或不同研究结果相互矛盾,支持MUO和MHO之间许多特征差异的证据并不确凿。
生活方式因素
饮食。
通过使用食物频率问卷或24小时饮食回忆数据在大型人群研究中评估了饮食摄入与代谢健康之间的关系。这些方法可靠评估饮食摄入的能力受到质疑。大多数研究的结果并未显示MHO和MUO人群之间的总饮食能量摄入或宏量营养素分布有差异。此外,美国国家健康和营养检查调查的数据显示,在采用地中海式和DASH式饮食的消费量评估的饮食质量方面,MHO和MUO人群之间没有差异。在19-44岁的MHO女性中发现了比MUO女性更高的总健康饮食指数得分,该指数根据2005年美国国家饮食指南评估饮食质量,但在45-85岁的MHO和MUO女性或成年男性MHO和MUO中,这一得分没有差异。一些研究(但不是全部)的证据表明,MHO和MUO组之间特定类型食物的消费量存在差异;MHO与较低的糖、含糖饮料和饱和脂肪摄入量以及较高的全果、全谷物和来自蔬菜来源的蛋白质摄入量相关联。
体力活动和心肺健康。
增加的体力活动可改善胰岛素敏感性和代谢综合征异常。通过双标记水法、加速度计和活动问卷研究了MHO和MUO人群中的体力活动量和强度。通过双标记水法测量的总日常能量消耗或体力活动期间的能量消耗在MHO和MUO人群之间未检测到差异。相比之下,使用加速度计或问卷测量体力活动的研究表明,MHO人群在中等到剧烈体力活动上花费的时间比MUO人群多,而在久坐活动上花费的时间较少。一项汇集了15项研究数据的元分析结果显示,以运动期间最大氧气消耗量评估的心肺健康在MHO人群中比在MUO人群中更好,但两组之间的平均差异非常小(1-2 mL/kg/min)。
睡眠。
睡眠时间不足和睡眠质量差对代谢功能有不利影响,并与肥胖有关。几乎所有评估MHO和MUO人群中睡眠时间和质量的研究结果都不足以可靠评估MHO和MUO之间的潜在差异,因为这些数据来源于问卷而非直接评估睡眠时间和质量。一般来说,MHO人群和MUO人群中的睡眠时长和短睡眠者(每天少于7小时)的比例没有显著差异。
脂肪组织生物学
随着体重增加,脂肪组织的扩张和TG质量(a)在不同脂肪组织库和肝脏之间的分布并不均匀;(b)是由于脂肪细胞大小或数量的增加,或两者兼有;(c)需要充足的血液供应来维持组织氧化;(d)促进细胞外基质(ECM)重塑,以提供支撑扩张的脂肪细胞质量所需的支架;(e)导致脂肪组织驻留免疫细胞的增加以及脂肪组织和全身炎症标志物的增加;(f)影响脂肪细胞脂解活性和脂肪酸释放入循环的速率;(g)改变主要脂肪细胞分泌蛋白脂联素的产生,该蛋白参与调节胰岛素敏感性。
身体组成。
百分比体脂在BMI和性别相匹配的MHO与MUO人群中没有差异。然而,在MHO和MUO队列之间,脂肪组织分布和肝内TG含量存在显著差异。与MUO人群相比,MHO人群的内脏脂肪组织(IAAT)较少,但仍比代谢健康的体重正常(MHL)人群多出两到三倍。尽管MHO女性往往比MUO女性的下半身(大腿或腿部皮下)脂肪量更多,但男性MHO和MUO之间的下半身脂肪量却没有差异。MUO人群的肝内TG含量高于MHO人群,且患有脂肪肝的人群比肝内TG含量正常的人在多器官胰岛素抵抗和血浆TG浓度上更高,即使BMI、体脂百分比和IAAT体积相匹配也是如此。总的来说,这些数据显示,过多的脂肪本身并不是导致MHO与MUO人群间代谢健康差异的原因,但脂肪组织的分布差异却能区分MHO和MUO表型。
脂肪生成和脂质生成。
评估MHO和MUO人群脂肪生成/脂质生成的研究主要集中在腹部皮下脂肪组织(SAAT)库。SAAT中的脂肪生成(即前脂肪细胞的增殖和分化)与代谢健康之间的关系尚不清楚。通过体外分化测定和涉及前脂肪细胞增殖与分化的基因表达来评估,SAAT中的脂肪生成能力在MHO人群中比MUO人群中更高。然而,通过测量从SAAT分离的脂肪细胞中摄入的氘并入DNA来确定的脂肪细胞增殖率,被报告为在超重/肥胖且胰岛素敏感的人群与超重/肥胖且胰岛素抵抗的人群中要么没有差异,要么更低。SAAT中脂质生成能力的评估,作为涉及脂质生成途径的基因(CD36、GLUT4、ChREBP、FASN和MOGAT1)的表达,在MHO人群中比MUO人群中更高。此外,这些基因的表达与胰岛素敏感性正相关,并且在MHO人群中比MUO人群中在适度体重增加后增加得更多。总的来说,这些数据反驳了受损的脂肪生成会导致MUO人群中胰岛素抵抗的观点,但证明增加的脂肪组织脂质生成途径基因表达与代谢健康有关。
脂肪细胞大小。
脂肪细胞的大小通常通过三种方法之一来测量:(a)脂肪组织的组织学分析;(b)用胶原酶消化脂肪组织以产生通过显微镜测量的自由脂肪细胞;以及(c)用四氧化锇固定脂肪组织和使用显微镜或Multisizer Coulter Counter进行细胞大小分析。通过这些方法中的每一种测量的SAAT中脂肪细胞的中位直径与全身脂肪量相关。然而,这三种方法中小细胞(20-50微米范围)的频率差异很大。当通过四氧化锇固定法评估细胞大小时,观察到这些小细胞的最高频率,这些小细胞被认为是未成熟或正在分化的脂肪细胞,但可能是大型含脂巨噬细胞。几项研究的结果显示,皮下腹部脂肪细胞的平均或峰值大小与胰岛素敏感性呈负相关,并且MUO人群中的脂肪细胞大小比代谢更健康的人群更大。然而,其他研究并未在MHO和MUO参与者中检测到平均皮下脂肪细胞大小的差异。两项研究基于大小识别了两个不同的脂肪细胞群体,并发现在胰岛素抵抗的人群中,小脂肪细胞与大脂肪细胞的比例高于胰岛素敏感的人群。总之,大多数研究表明,MHO人群的平均脂肪细胞大小比MUO人群小。然而,脂肪组织包含具有可变细胞数的不同小细胞和大细胞群体的观察结果,使得对整体平均细胞大小的解读变得复杂。因此,需要更复杂的分析方法来量化脂肪细胞的大小和数量。
氧气供应。
脂肪组织的氧合取决于氧气输送到脂肪组织细胞(脂肪细胞、前脂肪细胞、间充质干细胞、成纤维细胞、血管内皮细胞和免疫细胞)的速率与其消耗氧气的速率之间的平衡。由于与肺部功能障碍相关的全身动脉血氧含量降低、脂肪组织毛细血管密度和灌注减少、间质免疫细胞数量增加以及可能由于脂肪细胞肥大和ECM含量增加而导致的氧气扩散距离增大,肥胖人群的脂肪组织氧气输送可能低于瘦人。然而,肥胖人群的脂肪组织氧合是否充足尚不清楚,因为测量的是间质脂肪组织氧分压(pO2),而不是细胞内pO2,并且根据使用的方法不同,不同研究的数据相互矛盾。使用Clark型电极或光纤系统在原地评估SAAT间质pO2的研究中发现,肥胖人群的pO2低于瘦人。相比之下,使用光化学传感器在体外通过微透析提取的SAAT间质液中测量pO2的研究发现,尽管肥胖人群中脂肪组织血流减少,但pO2高于瘦人,这表明肥胖组的脂肪组织氧气消耗减少。直接评估SAAT动脉-静脉氧气平衡显示,与瘦人或超重人群相比,肥胖人群的氧气输送和消耗均降低;然而,肥胖与脂肪组织缺氧的证据无关,这是通过SAAT的氧气净平衡和血浆乳酸-丙酮酸比例来评估的。我们了解到三项研究评估了MHO和MUO人群中SAAT间质pO2。两项研究在原地测量了pO2,并发现与MUO组相比,MHO组的pO2更高或没有差异。第三项研究在体外通过微透析提取的SAAT间质液中测量了pO2,并发现MHO组比MUO组低。我们不知道有任何研究评估了MHO和MUO人群中代谢指示脂肪组织缺氧的指标,即脂肪组织HIF1α蛋白含量。总之,目前没有足够证据得出MUO人群与MHO人群相比,脂肪组织的氧合有生理上重要的降低的结论。
细胞外基质重塑和间质纤维化。
脂肪组织的细胞外基质由结构蛋白(主要是I型、III型、IV型、V型和VI型胶原)和粘附蛋白(纤维连接蛋白、弹性蛋白、层粘连蛋白和蛋白多糖)组成。与瘦人相比,肥胖人群中I型、IV型、V型和VI型胶原的基因表达增加,并且有组织学证据表明,特别是在网膜脂肪组织和皮下腹部脂肪组织中,纤维化程度增加,特别是细胞周围纤维化。此外,我们最近发现,脂肪组织中结缔组织生长因子(CTGF)的表达与体脂肪量正相关,与全身、肝脏和骨骼肌胰岛素敏感性的指标负相关(136)。肥胖人群中脂肪组织胶原基因的表达和胶原含量也与胰岛素敏感性负相关,并随着体重减轻而减少。这些数据支持了脂肪组织纤维化与MUO相关的观点,如在啮齿动物模型中所证明的。
免疫细胞和炎症。
肥胖通常与慢性、低度、非感染性炎症有关,这被认为是胰岛素抵抗的一个原因。人们提出,脂肪组织免疫细胞的变化是与肥胖相关的慢性炎症和胰岛素抵抗的一个重要原因。巨噬细胞是脂肪组织中最丰富的免疫细胞,与瘦人相比,肥胖人群的脂肪组织中巨噬细胞含量增加。而且,MUO人群的SAAT和IAAT中的脂肪组织巨噬细胞含量和冠状结构(巨噬细胞围绕一个细胞外脂滴)比MHO人群更多;巨噬细胞含量的增加主要是由于M1样(促炎)巨噬细胞的增加。还报告了MHO和MUO人群之间脂肪组织促炎CD4+ T淋巴细胞的差异。在SAAT和IAAT中,具有促炎作用的Th17和Th22细胞占CD4+ T细胞总数的百分比在MHO人群中比MUO人群低。此外,在一项研究中,SAAT和IAAT中的抗炎症CD4+ Th2细胞直接与通过胰岛素抑制试验评估的胰岛素敏感性相关。
与脂肪组织免疫细胞的变化相一致,MUO人群的脂肪组织炎症相关基因表达也高于MHO人群,但在不同研究中上调的具体基因存在不一致性,而且MUO组和MHO组之间的基因表达标记差异往往很小。血浆中炎症标志物的浓度,主要是C反应蛋白、纤溶酶原激活物抑制剂-1(PAI-1)、IL-6和TNF-α,在MUO人群中要么高于MHO人群,要么在两组之间没有差异。结果的变异性很可能与用于识别MUO和MHO的定义、不同研究中评估的具体炎症标志物以及因为组间血浆浓度均值差异小所需的足够统计力的样本量有关。
MHO和MUO人群脂肪组织炎症标志物的表达差异及其变化性和MUO与MHO人群之间血浆炎症标志物的差异及其变化性质疑了脂肪组织产生和分泌炎症细胞因子在介导MUO和MHO人群观察到的全身胰岛素抵抗差异中的重要性。尽管如此,其他免疫细胞相关的介质,如脂肪组织巨噬细胞衍生的外泌体,可能参与代谢功能障碍的发病机制。
脂肪分解活性。
急性实验性增加血浆游离脂肪酸(FFA)浓度,通过输注脂质乳剂诱导,以剂量依赖性方式损害胰岛素介导的对肝葡萄糖产生的抑制和胰岛素介导的葡萄糖处置的刺激。然而,内源性脂肪组织脂肪分解活性和血浆FFA浓度对肥胖人群胰岛素敏感性的影响尚不清楚,因为不同研究的结果相互矛盾。具体来说,与胰岛素敏感的人相比,超重/肥胖且胰岛素抵抗的人的FFA释放到全身循环的基础速率和血浆FFA浓度被报告为更高或没有差异。MUO中循环FFA作为胰岛素抵抗原因的重要性进一步受到质疑,因为研究发现,与瘦人和胰岛素敏感性更高的人相比,肥胖人群的基础、餐后和24小时血浆FFA浓度没有差异。研究之间差异的原因尚不清楚,但可能与FFA动力学和血浆FFA浓度的日常个体差异大以及胰岛素抵抗人群中胰岛素介导的脂肪组织脂肪分解速率的补偿性高胰岛素血症和抑制差异有关。研究队列中女性比例的差异也会影响MHO和MUO组之间FFA动力学和浓度的比较,因为与去脂体重或静息能量消耗相关的血液中FFA出现率在女性中比男性更高,然而肌肉和肝脏的胰岛素敏感性在女性中更高。总的来说,这些研究表明,皮下脂肪组织脂肪分解活性的差异不能解释MHO和MUO人群之间胰岛素敏感性的差异。然而,IAAT的脂肪分解差异和门静脉FFA浓度的差异,或者FFA对组织(肌肉或肝脏)胰岛素作用的影响差异,仍然可能导致两组之间胰岛素抵抗的差异。
脂联素。
脂联素,脂肪组织分泌的最丰富的蛋白质,与男女的体脂肪百分比成反比,与胰岛素敏感性成正比。在MHO人群中,血浆脂联素浓度通常高于MUO人群。MUO与MHO相比,脂联素浓度较低的原因尚不清楚,但可能与MUO人群中的慢性高胰岛素血症有关,这抑制了脂肪组织脂联素的产生,从而形成了一个由胰岛素抵抗引起的脂联素分泌减少和由脂联素分泌减少引起的胰岛素抵抗增加的正反馈循环。
结论
与肥胖相关的代谢并发症存在相当大的异质性。当健康被定义为没有代谢综合征时,约50%的肥胖人群是代谢健康的,而当健康被定义为没有任何代谢综合征成分和通过HOMA-IR评估的正常胰岛素敏感性时,只有大约5%是代谢健康的。肥胖人群发展为心血管代谢疾病的风险与代谢异常的数量和严重程度直接相关。因此,与MUO人群相比,MHO人群未来患T2D和CVD的风险较低,但大多数MHO人群的风险比MHL人群要高。然而,没有任何代谢异常并且随时间保持MHO状态的人群可能不会比MHL人群有更高的发展为心血管代谢疾病的风险。这些发现支持需要对MHO进行严格和普遍的定义(如表2所提议),以允许可靠地整合不同研究的数据,并促进识别保护一些肥胖人群免受过量脂肪积累不良代谢影响的因素所需的研究。
目前还不知道保持MHO人群代谢健康状态的确切机制。迄今为止的研究并未显示出MHO和MUO之间在生活方式因素(饮食组成、体力活动和睡眠)上的重要差异。然而,这并不意味着生活方式不是代谢健康的重要调节因素,而是强调了当前研究中对生活方式因素评估和MHO定义的局限性。很可能肥胖人群的代谢表型有一个重要遗传因素。尽管全基因组关联研究已经鉴定出与健康代谢特征相结合的增加肥胖倾向的遗传变异,但更好地理解MHO的遗传方面可能会为负责代谢疾病的机制提供新的见解。肠道微生物组对代谢健康的影响是一个迅速涌现的研究领域。肠道微生物组对代谢健康的不利和有益影响可能与微生物群的组成和多样性以及肠道屏障功能防止细菌及其产物穿过肠道泄漏的能力有关。此外,在人类受试者中进行的研究显示,与MUO相比,MUO人群的脂肪组织中炎症和间质纤维化的标志物增加。然而,这些研究无法确定这些异常是胰岛素抵抗和相关代谢功能障碍的原因还是结果。
肥胖相关代谢并发症的异质性具有重要的临床意义,特别是在当前的精准医疗和成本效益时代。仅根据BMI状态对肥胖进行分类并不能充分洞察当前的健康状况、未来不良临床结果的潜在风险,或谁最有可能从减重治疗中受益。现有数据表明,应该优先考虑为MUO而非MHO人群提供更密集、可能也更昂贵的体重管理治疗。然而,这种方法需要一个更强大的MHO诊断和额外数据来理解MHO与其他肥胖相关并发症风险之间的关系,而不仅仅是代谢结果本身。
https://blog.sciencenet.cn/blog-41174-1441743.html
上一篇:博士生们如何应对职业心理健康危机
下一篇:健康型肥胖的秘密