博文
氢气生物学效应的目标分子  精选
精选
|
氢气直接生物靶标的探索
氢气具有广泛生物学效应,这种作用是如何实现的,特别是氢气如何和具体生物分子的作用,这是理解和解释氢气生物学效应的重要问题。本文主要从氢气具体作用分子方面对当前的学术研究进行了全面总结。
氢分子(H2),无论是以气体形式还是溶液形式提供,作为一种治疗多种疾病和病状的方法越来越受欢迎。例如,它被认为对神经退行性疾病有益,有助于缓解恢复血流至先前缺血组织所造成的伤害,甚至能够减轻COVID-19的症状。它还被提议作为增强运动表现的体育补充剂。然而,H2的确切作用机制尚未明确揭示。有研究表明,H2可能作为一种抗氧化剂,特别是作为羟基自由基(·OH)的清除剂。情况可能是这样,但这不太可能是H2在生物系统中唯一的作用方式。在这里,我们将讨论H2可能发挥作用的一些机制,这可能解释它在医学背景下的作用方式。
这是《氢气在疾病健康中作用》书内第二章内容的摘要。该内容对氢气生物体内直接目标效应分子的研究进行了总结和回顾,并对目前存在的问题进行了探讨。这篇内容对于理解氢气医学机制研究现状有帮助,是从事氢气医学研究和氢气产品开发人员需要了解的最基本知识。
Hancock, J.T., May, J.E., LeBaron, T.W., Punampalam, R., Russell, G. (2024). An Exploration of the Direct Biological Targets of Molecular Hydrogen. In: Slezak, J., Kura, B. (eds) Molecular Hydrogen in Health and Disease. Advances in Biochemistry in Health and Disease, vol 27. Springer, Cham.
前言2007年,《自然医学》杂志发表了一篇论文,提出了将分子氢(H2)引入医学领域的可能性[1]。这不是第一次将氢气作为药物进行研究,至少可以追溯到18世纪末的作品。在亨利·卡文迪什于1766年发现氢气后不久[2],托马斯·贝多斯、汉弗莱·戴维和提伯留斯·卡瓦洛就进行了相关研究[3]。Dole等人也提出,氢气可以作为癌症的高压氧疗法[4],尽管当时这一提议并未被广泛采纳或深入研究[5]。在Ohsawa等人的论文中[1],作者研究了H2在细胞培养和动物模型中的效果。他们通过使用荧光探针或电子顺磁共振(ESR)和自旋捕获技术,评估了活性氧(ROS)和一氧化氮(NO·)的积累。特别是,因为H2的作用机制一直存在争议,作者通过2-[6-(4’-羟基)苯氧基-3H-呫吨-3-酮-9-基]安息香酸酯(HPF)的荧光和自旋捕获剂5,5-二甲基-1-吡咯啉N-氧化物(DMPO)来评估羟基自由基(·OH)的存在。作者得出结论,H2能够减少·OH,并且在一定程度上也能减少过氧亚硝酸盐(ONOO−)。他们指出,即使在细胞核区域,H2也能通过荧光探针和标记物降低·OH水平。然而,重要的是,H2并不与一些重要的内源性信号分子反应,例如一氧化氮(NO·)、超氧阴离子(O2·−)或过氧化氢(H2O2)。氢气在医学上的用途被其他人接受并提出,认为它对人类各种疾病都有益[6]。这包括治疗神经退行性疾病[7]、缺血再灌注损伤[8]和COVID-19[9]。也有建议将氢气用于体育运动以增强表现[10,11,12,13]。氢气在医疗治疗中的使用已经被其他人回顾[14,15,16]。甚至有人提出氢气对农业实践有益[17],以及对农作物的收获后储存有益[18, 19]。尽管这些工作可能与其临床效果不直接相关,但在植物细胞中的基础机制可能与在动物中揭示的类似。氢气可以通过多种方式给予生物体,包括人类。由于氢气是一种气体,可以以其气态形式使用,直接吸入。显然需要有一定比例的氧气存在,但已经证明吸入相对较高浓度的氢气是安全的,正如深海潜水所用的气体混合物所证明的那样。这种气体混合物最早在1940年代提出[20],并已被广泛使用。最近,一种含有66%氢气和33%氧气的气体混合物被称为含氧气体(也常被称为布朗气、羟基气、HHO气,通常带有负面含义)。含氧气体被认为对医疗治疗有益[21],而且它们被认为是对人类消费安全的,尽管这种气体非常易燃。或者,可以制备富含氢气的溶液。最常用的含氢溶液被称为富氢水(HRW)。这只需将氢气注入水中即可简单制备。氢气会迅速从水相转变为气相,从溶液中消散,因此HRW需要相对快速使用,其半衰期约为2小时。另一种方法是将H2气体溶解在盐水中,称为富氢盐水(HRS)。除了可以饮用外,HRW还可以用于局部治疗,如用于减少皱纹[22]。如果你没有现成的氢气罐,可以通过电解产生氢气,或者使用现在常见的产氢片剂。这些通常由镁组成,与水反应产生H2气体,然后部分溶解,形成HRW的现成来源。这样的治疗现在可以通过互联网轻松获得。因此,氢气是一种容易获得、有用、安全且易于使用的辅助治疗,适用于一系列人类疾病。然而,如果它有任何效果,它必须作用于细胞并在这些细胞内引发生化机制。这里存在一个问题。虽然有人提出了氢气对细胞的直接作用,但几乎没有具体的证据。这里,将对一些提出的建议进行回顾并总结在表2.1中,但迫切需要更多的工作集中在这一领域,而不仅仅是报告表面效应。除非揭示了潜在的机制,否则使用H2进行治疗可能会继续边缘化,未来的一个重要机会可能会丧失。正如最近几篇关于氢气在生物系统中历史的论文所示[3, 5],使用H2作为治疗(特别是消费,即结核病)的想法在两百多年前就被提出并研究过,但氢气用于人类治疗的历史一直是断断续续的[5]。这一次它需要坚持下去并被认真对待,理解H2的生物作用将极大地有助于实现这一点。
Table 2.1 Potential mechanisms by which H2 may directly interact with cells
Action suggested | Comments | Ref(s) |
Direct covalent modification of proteins | Extremely unlikely as H2 is relatively biologically inert and will not have action akin to phosphorylation | – |
Direct action on DNA/RNA | Extremely unlikely as H2 is relatively inert | – |
Modification of life-time of proteins, i.e. ubiquitination | Some evidence that H2 alters this | |
Antioxidant | Many oxidant molecules shown not to be directly scavenged, including O2·−, H2O2 and NO· | [1] |
Scavenger of hydroxyl radicals | Most commonly mooted action. Likely to take place but does it account for all of the actions seen? | [1] |
Redox modulator | Precedent in bacterial systems, so could happen. Likely targets are haem-containing proteins, such as cytochromes | [25] |
Altering spin states | Theoretically possible, but never investigated | [26] |
Acting on xenon pockets | Precedent in other proteins with other inert gases, so theoretically possible. May alter structural stability of proteins? | [27] |
氢气的直接作用
因为氢气(H2)对生物系统有作用,所以它必须与细胞成分发生相互作用。所见的变化必然涉及蛋白质活性的改变。这种控制可能在多个层面上进行。蛋白质的活性可能会因其结构直接改变而增加或减少,从而调节功能。蛋白质的改变可能涉及共价修饰,例如氧化和磷酸化。如下文进一步讨论的,这里有许多先例,其他小的、相对活跃的化合物可以通过修饰氨基酸侧链来改变蛋白质的结构。这包括一氧化氮(NO·)的S-亚硝基化(S-亚硝酰化)[28],氢过氧化物(H2O2)的氧化[29],以及硫化氢(H2S)的S-过硫化[30]。可以看出,这些分子中的一些是气体(NO·和H2S),就像H2一样,但H2并不是非常活跃,通常被认为是生物学上惰性的。因此,H2通过共价修饰氨基酸的可能性非常小。
或者,为了增加蛋白质活性,细胞可能简单地制造更多活跃的蛋白质,这将需要改变基因表达。这要么意味着mRNA的不同表达,要么意味着mRNA的不同处理。通过转录因子Nrf2介导的H2的作用在这里可能相关[31]。在一些研究中,报告了抗氧化活性的增加,例如,这可能涉及去除氧化剂的酶的整体活性的增加[32, 33],但并没有解决如何存在更多活跃酶的确切机制。
最后,蛋白质活性可能通过允许蛋白质工作或存在更长时间而增加。蛋白质可能会被降解并从细胞中移除,在这样的机制中如泛素化[34]。有一些证据表明这是H2作用的范围之一,Lio等人[23]和Ren等人[24]都提出H2的存在可能会影响蛋白质的泛素化水平。
如果H2不通过共价改变蛋白质、直接调节它们的活性或让它们持续更长时间,那么H2在细胞中的作用机制是什么?下面讨论了一些更可能的机制。
抗氧化剂和羟基自由基
毫无疑问,小的活跃分子在控制细胞中蛋白质的作用方面有着深远的影响。通过对细胞信号传导机制的改变,许多小分子可以对细胞活性产生深远的影响。这些机制可以直接作用于蛋白质,如表2.2所概述。尽管不是通过同一种类型的机制介导的,磷酸化被视为蛋白质可以被共价修饰的经典方式[35]。磷酸化可以增加蛋白质的活性,例如磷酸化酶激酶,或减少蛋白质活性,如糖原合成酶——在这种情况下防止无效循环。在许多情况下,磷酸化是可逆的,磷酸基团的添加由激酶催化,其去除由磷酸酶催化。通过这种方式,蛋白质的活性可以被开启和关闭。参与磷酸化的蛋白质包括转录因子和那些参与RNA代谢的蛋白质,因此基因表达和多肽水平可能会改变,表现为细胞活性的改变。这种蛋白质共价修饰和活性改变的模式被许多细胞信号传导机制复制,其中许多涉及小的、相对活跃的分子,有些是气体,如上所述。因此,任何对磷酸化或类似机制的影响,都会对蛋白质的细胞活性产生深远的影响。
1987年发表的一篇论文将小的活跃分子在细胞信号传导机制中的作用带到了前台,该论文显示内皮舒张因子(EDRF)实际上是气体一氧化氮(NO·)[36]。NO·部分通过修饰蛋白质中的半胱氨酸侧链产生-SNO加合物来发挥作用。这可以改变蛋白质活性,并且可以逆转,就像磷酸化一样。现在已知,NO·的作用,无论是由细胞本身产生的,还是来自外源的,都是细胞控制其行为的重要方式,并且涉及许多疾病状态[37]。
Palmer等人的工作[36]为许多其他人打开了大门,他们开始研究可能参与细胞信号传导的活性化合物。工作转向了活性氧物种(ROS),如超氧阴离子(O2·−)、H2O2和羟基自由基(·OH)。这些分子被认为是相对有毒的,就像NO·一样,并且参与病原体反应的过程,如呼吸爆发[38]。这些化合物也会导致细胞内环境变得氧化,这一过程被称为氧化应激,相反的是还原应激[39]。然而,同时,对这些分子在细胞信号传导中也具有积极作用的兴趣也在增加,即在控制细胞功能方面发挥积极作用,工作开始接受其他化合物。例如,超氧阴离子可以与NO·反应生成过氧亚硝酸盐(ONOO−),从而降低ROS和NO·的水平,但创造了一个新的潜在信号分子[40]。H2O2和H2S可以制成亚硝硫醇,降低ROS和H2S的水平,但又制造了另一个信号组分[41]。H2S本身已被证明可以引起血管舒张并具有细胞信号传导作用。对抗氧化应激的主要细胞成分之一是谷胱甘肽,它也已被证明可以在共价改变蛋白质方面发挥作用[42]。因此,人们了解到有一系列方式可以控制蛋白质功能,并且很快就明白这些都不是独立的过程。这些途径之间有大量的交叉通话。
随后,更多的参与者出现了。一氧化碳[43]和甲烷[44]也可能被混合进来,尤其是氢气。因此,人们提出的问题是,如果这些“新”的信号分子要对细胞的信号传递过程产生影响,它们将如何融入其中?或许可以合理地明确,H2不会通过直接共价修饰蛋白质来发挥作用,但很快也有报告称,H2与许多这类重要的小型活性分子也几乎没有直接相互作用。一个重要的例外是,分子氢可以与羟基自由基反应,因此这至少可以解释所观察到的一些效果[1]。这将在下一节中讨论。然而,应该注意的是,没有证据表明H2可以反应,因此清除和移除NO·或H2O2,这两者都是已知可以通过共价修饰蛋白质并改变基因表达的。如果这些分子的作用被改变了,那么必然存在一些机制来修改它们的产生或清除,从而通过对蛋白质活性的适应来发挥作用,而不是与H2直接化学反应。因此,如果修饰后的蛋白质结构可能影响NO·或H2O2的产生或清除机制,可以推测H2通过间接的蛋白质结构修饰来调节机制,而不是直接的化学反应。由于没有直接反应的证据,必然存在另一种机制。如果NO·和ROS的代谢都没有被H2直接改变,那么很难想象H2在细胞中有如此深远的影响。有报告称H2改变了NO·的代谢,但确切的机制需要阐明[45, 46],关于ROS代谢也有类似的报告[47]。因此,直接作用于信号分子似乎被排除了,但下面讨论了H2可能如何发挥作用的一些可能解释。有许多论文讨论了氢气(H2)如何作为抗氧化剂,或至少改变细胞的抗氧化能力。例如,Dong等人[48]报道,由于细胞中抗氧化剂的变化,水果通过H2处理得以保存,而Gu等人[49]报道了水稻中抗氧化剂的变化。其他食品产品也有类似的反应,例如苜蓿[50]、韭菜[51]和小白菜[52]。然而,正如上文所讨论的,很难想象H2如何直接改变抗氧化酶的活性或增加它们在细胞中的产生。众所周知,许多ROS和NO·并不直接与H2反应。然而,这里的一个例外是羟基自由基。在Ohsawa等人2007年的论文[1]中,报告称H2抑制了细胞中的·OH积累。通过这一机制,人们认为细胞的氧化应激减少了,氧化反应减少了,因此细胞可以缓解一系列压力。这种氧化还原机制被认为可以通过抑制有害自由基引起的氧化损伤来减轻细胞的氧化应激,作者甚至说:“H2可能足够温和,不会干扰代谢的氧化还原反应或破坏参与细胞信号传导的ROS。”另一方面,这样的机制被认为是H2在一系列疾病治疗中作用的基础,这些疾病很多都是由ROS/NO代谢紊乱所支撑的。这里值得一提的一个可能是,类似的机制在其他模型生物中也可能发生,不仅仅是在人类中。因此,H2的响应机制应该在其他脊椎动物中也能观察到,包括人类和哺乳动物,以及更低等的动物和植物。最近有几篇论文尝试解释氢气(H2)和羟基自由基(·OH)相互作用的机制。Kim等人[53]使用计算机模拟来评估H2与蛋白质中的血红素辅基相互作用的方式。研究表明,根据相互作用的方向,氢气可以转化为氢自由基(·H),然后有能力与·OH相互作用。这种机制确实可以解释H2和羟基自由基如何在细胞中以显著的速率相互作用,从而减少细胞中·OH的积累。然而,这也可能取决于适当的血红素团的细胞位置,以及与可能在细胞其他部位起作用的·OH的距离。正如其他地方讨论的[27],除了任何·OH清除作用外,还会对含有血红素的酶的原始作用产生影响。Jin等人[54]也提出了类似的机制。他们也专注于H2与血红素辅基的相互作用,提出了一种可以解释H2的·OH清除活性的机制。他们认为,由于高激活能,·OH和H2之间直接相互作用是不太可能的,然后引用了Gong等人[55]的工作,他们研究了用于实时成像活体内氢分子的荧光探针。然而,他们展示了H2可以与过氧化亚硝酸盐缓慢反应(血红素不会显著增强),但如果存在血红素,H2也可以与H2O2反应,尽管速度慢。此外,H2与血红素的相互作用允许将二氧化碳(CO2)还原为一氧化碳(CO)。因此,这样的反应允许进一步的下游作用,这将由H2的存在(或如果内源性的话,积累)启动。当然,看来H2与血红素的相互作用及其理解这些相互作用的任何后果是H2生物学及其与·OH相互作用的一个重要方面。最近,有人提出这样的涉及H2和血红素的机制参与了转录因子Nrf2的控制[31]。因此,似乎毫无疑问H2和·OH可以发生反应,当然H2很可能会清除·OH。问题仍然是,在复杂的多方面细胞信号传递过程中,这种机制在多大程度上有助于其生理益处?如果这里有一个重要的作用,它应该在信号传递中扮演重要角色,这将在下面讨论。Table 2.2 Possible mechanisms for altering protein action through covalent modifications
Reactive molecule mediating effect | Mechanism | Comment |
Catalysed from ATP | Phosphorylation | Not mediated by a small reactive compound, but seen as a classical model |
Nitric oxide (NO·) | S-nitrosylation | Sometimes referred to as S-nitrosation. Cys target. Protein activity can be toggled on and off |
Hydrogen peroxide (H2O2) | Oxidation | Lower oxidation states can be reversed. Cys often the target |
Hydrogen sulfide (H2S) | S-persulfidation | Can be reversed. Cys often the target |
Glutathione | Glutathionation | Can be reversed. Cys often the target |
Hydrogen | – | No mechanism reported |
细胞内羟基自由基的作用
似乎毫无疑问,即使有一些关于动力学的争论[56],H2和·OH确实可以发生反应。尽管关于血红素和H2的工作表明动力学问题已经解决,如上所述。H2/·OH相互作用在生理上可能是相关的,并且很可能在某种程度上在细胞内发生。这里需要提出的问题是:H2与·OH的作用能否解释细胞中看到的所有效应,无论它们是来自人类还是植物?
这里的一个问题是·OH自由基是否能控制细胞功能,即它是否能参与细胞信号传导过程?对此的答案几乎是肯定的。早期的工作似乎集中在·OH在介导细胞损伤中的作用,有报道称蛋白质是·OH的主要靶标,而不是脂质,或导致DNA断裂[57]。羟基自由基的存在已被证明与疾病机制相关。例如,通过测定由·OH介导机制产生的间位和邻位酪氨酸,有人提出·OH参与了胰岛素抵抗[58]。然而,有充分的证据表明·OH在控制一系列细胞活动中具有互动作用。例如,cAMP信号传导被认为在·OH的产生中具有矛盾的作用,既可能刺激它也可能抑制它,这取决于效应是由cAMP直接激活的交换蛋白(Epac)还是蛋白激酶A(PKA)介导的[59]。
羟基自由基已被牵涉到对CO的反应中,CO不仅是一种有毒气体,还可以具有治疗效果[60]。在脑组织中,发现·OH的含量会随着氧气张力的变化而增加或减少。这一点很有趣,因为H2已被证明可以通过调节血红素加氧酶(HO-1)的活性来发挥作用[61,62,63],而血红素加氧酶本身已被证明参与CO和血红素的代谢[64]。此外,如上所述,H2可能与血红素发生相互作用,对CO的产生和代谢可能产生影响[54]。因此,在这里,我们有H2、CO、血红素和特征明确的信号组分(即cAMP)都在同一个机制中,并且都参与细胞中的调节过程。
这里的第二个问题是细胞内区域化的问题。如果·OH是介导H2所降低效应的活性化合物,那么·OH是否在细胞中正确的位置产生?为了产生实际响应,·OH、H2和效应都需要处于同一位置。正如cAMP信号传导所示,区域化是重要的考虑因素[65]。为了让行动发生,信号分子必须能够迁移到作用点,否则无法发生响应。活性信号必须在正确的位置产生,并在不需要时被移除。人们不禁要问,也许H2作为·OH的区域化调节剂,但鉴于H2可以在水溶液中以及通过膜等疏水空间扩散,很难看出它如何能有基于位置的效应。它肯定会从所有地方移除·OH。然而,围绕·OH信号传导的区域化的主要问题是,这种自由基不太可能扩散。它会与它接触的第一物质发生反应,无论是蛋白质、脂质还是核酸,尽管蛋白质被认为是它的主要靶标[57]。它的行动很可能是由质子抽象驱动的[66],它的行动将没有什么微妙之处。它是否会像cAMP那样作为一个特定目标驱动的信号分子行动,cAMP将通过基于受体(锁和钥匙)类型的机制进行相互作用,或者像NO·那样可能与水性可接近的巯基团发生相互作用?·OH会有如此明确的作用吗?这似乎不太可能,因此·OH是否是H2的一个好靶标,以解释H2被赋予的所有行动?如果不是,那么替代方案是什么?
当讨论参与控制细胞功能的小活性分子时,主要候选者是O2·−、H2O2和NO·。然而,Ohsawa等人的论文[1]强调,H2没有能力直接与这些分子中的任何一个发生反应。因此,H2不能直接影响由O2·−、H2O2或NO·介导的信号传导,如图2.1所总结,尽管如上所述,ROS/NO代谢的变化已被注意到会受到H2存在的影响。
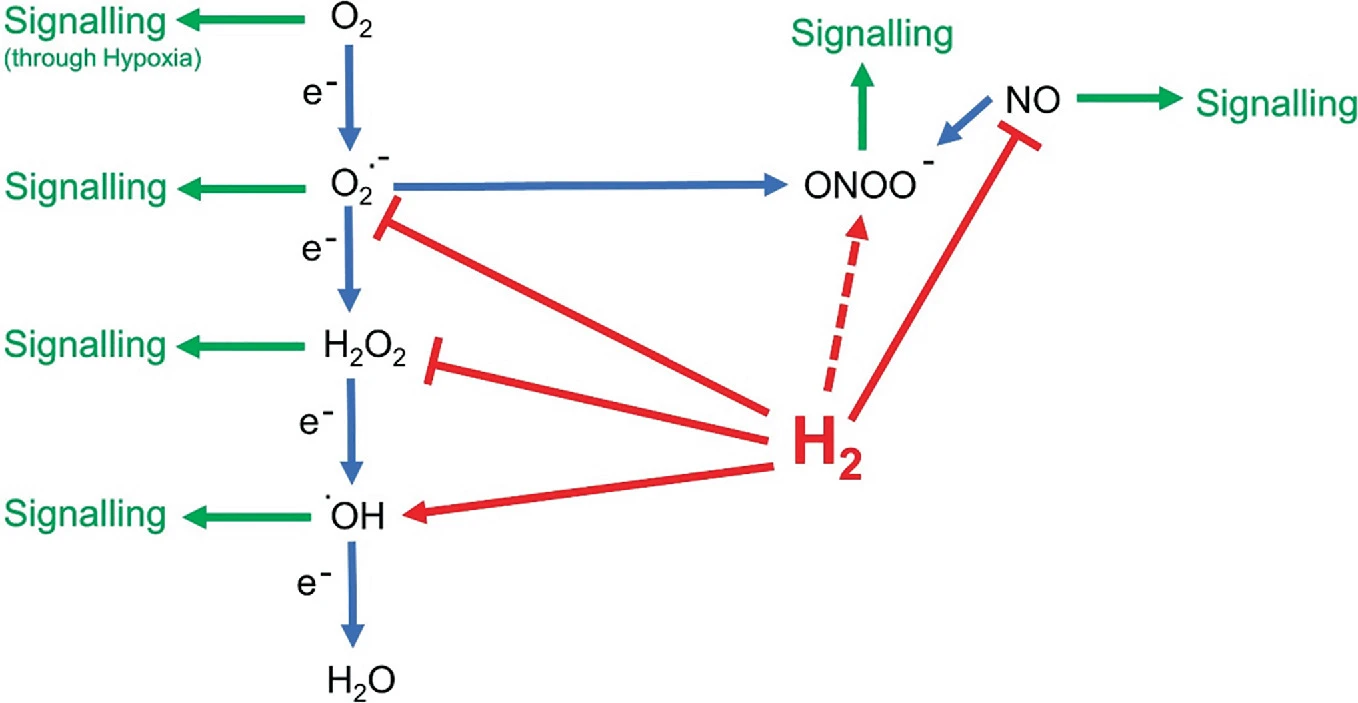
图2.1 氢气的直接作用目标分子
尽管通过判断生物组分对生理系统影响的方式非常朴素,表2.3显示了使用不同术语在PubMed数据库中的文献数量(截至2023年3月)。可以看出,关于羟基自由基(signalling)的文章比例非常少。这可能简单地表明了像NO· (27,294条目)和H2O2 (9793条目)这样的小活性分子在信号传导中的重要性,与·OH (634条目)相比。然而,目前的观点是H2通过·OH信号传导起作用,并且不对NO·、O2·−或H2O2产生任何直接影响。如果这能说明H2的作用方式,那么很难调和H2通过·OH信号传导的所有作用。实际上,Ohsawa等人[1]认为,H2不与反应性较低的物种如NO·、O2·−或H2O2反应,对于维持氧化还原平衡是一种有益的作用。
这里值得强调一个附加说明。尽管与NO·和H2O2相比,针对·OH自由基信号传导的研究相对较少,但这并不排除·OH作为H2益处的重要介质。如果·OH能间接影响其他ROS/RNS如O2·−、H2O2和NO·的信号传导,通过影响它们的产生和/或中和,可能会影响重大的信号事件。此外,·OH自由基可能诱导细胞膜的脂质过氧化,进而导致信号转导途径的许多变化,正如Iuchi等人[67]所建议的。即便如此,探索H2的其他可能作用机制也是值得的,以便完全理解H2在细胞中如何产生如此广泛的影响。
H2的氧化还原作用
改变蛋白质作用的方法之一,特别是那些具有辅基的蛋白质,是通过改变蛋白质活性部分的氧化还原状态。例如,在血红蛋白中,位于卟啉中心的Fe可以作为Fe2+或Fe3+存在,这改变了其功能和结合氧的能力。另一个例子是细胞色素c。细胞色素c在电子从线粒体复合体III传递到复合体IV的过程中扮演着重要角色——一次传递一个电子。这对于电子传递链的完全功能性以及跨膜电化学梯度的形成和随后的ATP产生至关重要。然而,线粒体可以驱动凋亡[68],在这种情况下,细胞色素c离开线粒体并形成凋亡复合体,激活caspases并导致细胞死亡。这类具有双重且通常截然不同功能的蛋白质被称为兼职蛋白[69]。然而,凋亡是由氧化应激触发的,人们质疑细胞色素c的氧化还原状态是否在允许这一机制进行中起到关键作用[70],或许作为一种安全机制,只有在细胞氧化还原状态足够氧化时才允许凋亡进行。同样,细胞色素c中的Fe可以以2+或3+状态存在,这可能会影响细胞色素c的作用。
氢气可以作为一对氧化还原对。在生理条件下,H2的中点氧化还原电位(Em)比标准氢电极更负,低于-400 mV。这是显著的还原性。例如,NAD+/NADH的氧化还原对的Em为-320 mV。NAPDH氧化酶中的细胞色素b的中点电位约为-245 mV(它通常被称为Cyt b-245,尽管它有两个不同电位的血红素组[71])。该细胞色素被认为具有非常低的氧化还原电位,但不像H2那样低。因此,理论上,H2对具有热力学能力减少人类细胞中蛋白质的血红素组和其他辅基。在细菌中有这样的先例,Cyt c3可以通过H2的存在而被还原[72]。
然而,并没有证据表明这是一种在真核细胞中发生的机制。一些目标已经被调查并排除,例如烟酰胺腺嘌呤二核苷酸(NAD)、黄素腺嘌呤二核苷酸(FAD)和细胞色素c[1],但还有许多可能受H2这种影响的系统。已经提到的一个是NADPH氧化酶[73],因此可能会改变细胞中ROS的产生。超氧化物的产生可能会改变,随后可能会导致细胞内H2O2水平和任何下游化合物的波动。NO合酶含有血红素组,因此NO·的产生可能以类似方式改变,从而调节下游NO·代谢。鸟苷酸环化酶是NO·的一个靶标,也有一个血红素组。线粒体辅基可能是潜在的目标,在植物中还有叶绿体的细胞色素、叶绿素和黄素。尽管一些H2的氧化还原目标可能被认为是无关的,但对这里一些可能的参与者进行广泛搜索将是一个值得的练习。
H2调节自旋态
氢气(H2)可以存在于不同的自旋状态中,并且有可能在状态之间切换,这些不同的状态可能能够与其他分子进行差异性交互。这已经被提出[26],但还没有证据支持。然而,就像其他提议一样,探索这种可能性也许是值得的。
H2与蛋白质中的氙气口袋相互作用
氢气(H2)是一种相对惰性的气体。然而,生物系统受到各种惰性气体的影响。其中最著名的是氙气(Xe),但也包括氩气(Ar)。因此,如果氢气是通过其惰性本质起作用的,那么这种作用方式是否可能,是否可以解释细胞中观察到的一些效应。
惰性原子与蛋白质相互作用的经典系统之一就是氙气,由于其已知的生物效应,氙气被建议作为医疗气体使用[74]。实际上,蛋白质中参与结合惰性原子或分子的区域通常被称为氙气结合位点(简称Xe口袋)。蛋白质具有三维结构,那些亲水性的蛋白质,可能位于细胞质中,可以被看作是一个松散的线团,因此在这样的结构中存在间隙、裂缝、空腔和口袋。这些地方可以让水分子进入,并且这样的水合可能有助于稳定结构,或者如果蛋白质发生别构变化,则稳定结构。然而,这些口袋也对其他小分子和原子的进入开放,例如氙气。如果这些滑入空腔,它们也可能起到稳定甚至诱导多肽链的一些微妙拓扑变化的作用。一个很好的例子是氙气和血红蛋白[75]。Turan等人[76]提出,氙气能够在肌红蛋白等蛋白质的空腔中迁移,因此氢气也有可能做到这一点。有趣的是,这样的机制已经被提出用于酶胃蛋白酶[77]。
还有其他惰性气体可以与蛋白质相互作用。一个好的例子是氩气。氩气被发现通过激酶[78]和Toll样受体信号传导[79]发挥作用,并被建议作为脑部创伤的治疗[80]以及具有神经保护作用[81]。因此,可以将关于氩气和氙气等气体的已知信息转化为理解氢气的作用吗?
这里和其他地方[27]提出的问题是,氢气是否能以同样的方式起作用。主要问题是氢气分子的大小,它太小了。也许太小了吗?然而,这并不意味着应该排除这个想法,尤其是已经发表了有关胃蛋白酶的先例[77],而是这是氢气可能与蛋白质相互作用的一种方式,应该探索。
结论和未来
毫无疑问,氢气在人类中具有深远的效果,并可用作一系列疾病的治疗[82]。它也在其他生物体,如植物中显示出显著效果。因此,氢气被认为是医学和农业未来的治疗手段[83,84,85]。它已被提议作为运动医学[10,11,12, 86]和放射损伤的治疗[87]。
氢气安全、相对便宜且易于管理。过去八十年来,氢气在潜水中的使用表明,人类可以耐受吸入气体中高浓度的氢气[20]。早期对动物和人类的实验都显示出类似的结果[3],尽管在十八和十九世纪之交,人们对所使用的气体的成分有很大的不确定性。
尽管已经有关于氢气在细胞中如何作用的建议,但仍存在一些争议。一些人提出了特定的机制,可能是氢气与血红素相互作用,可能是作为蛋白质中的辅基[31, 53, 54],但这些机制是基于至少部分·OH媒介了氢气在细胞中的效果的前提,并且这些机制还开启了许多额外的下游效应和目标的可能性,除了·OH清除之外。
非常有可能的是,氢气对细胞有多种作用。在某些情况下,它的效果可能是通过清除羟基自由基来介导的,但这一机制不太可能解释在所有报道过效果的生物体中看到的所有反应,包括人类和植物。它可能通过其氧化还原中点电位起作用,并对含有血红素或黄素辅基的一系列蛋白质产生影响。它可能通过自旋态起作用,但更有可能是它以一种在其他惰性气体中看到的方式起作用,即通过进入蛋白质的空腔并影响蛋白质结构的稳定。当然,后一种机制可以解释氢气广泛的效果。这不依赖于局部化学反应,并且由于氢气可以自由地通过水性和疏水性环境扩散,不会受到隔室化的限制。在未来,基于Cheng等人的工作[77],对氢气对胃蛋白酶活性的影响进行了彻底的研究,这将是值得深入研究的。
从上述讨论中可以清楚地看出,这里有很多值得探索的地方。一些想法可能被证明是错误的,或者意义不大,但现在正是揭开分子氢作用的分子机制的最佳时机,无论是在植物、低等动物还是人类中。
https://blog.sciencenet.cn/blog-41174-1422870.html
上一篇:生成式AI脖子竟卡在能源
下一篇:红光照降血糖临床试验