博文
Green Carbon文章 | 中国科学院植物所杨文强研究员:揭示莱茵衣藻高效固碳机制,赋能作物增产
||

作者:Ruizi Li, Junting Pan, Jiale Xing, Wenqiang Yang*
01 论文信息
论文信息
Ruizi Li, Junting Pan, Jiale Xing and Wenqiang Yang. The Secret of High Carbon Fixation Efficiency in Chlamydomonas and Its Potential to Boost Yields in Land Plants,[J].Green Carbon, 2025.
论文网址
https://doi.org/10.1016/j.greenca.2025.02.005
论文下载
中文解读原链接
Green Carbon文章 | 中国科学院植物所杨文强研究员:揭示莱茵衣藻高效固碳机制,赋能作物增产
02 背景简介
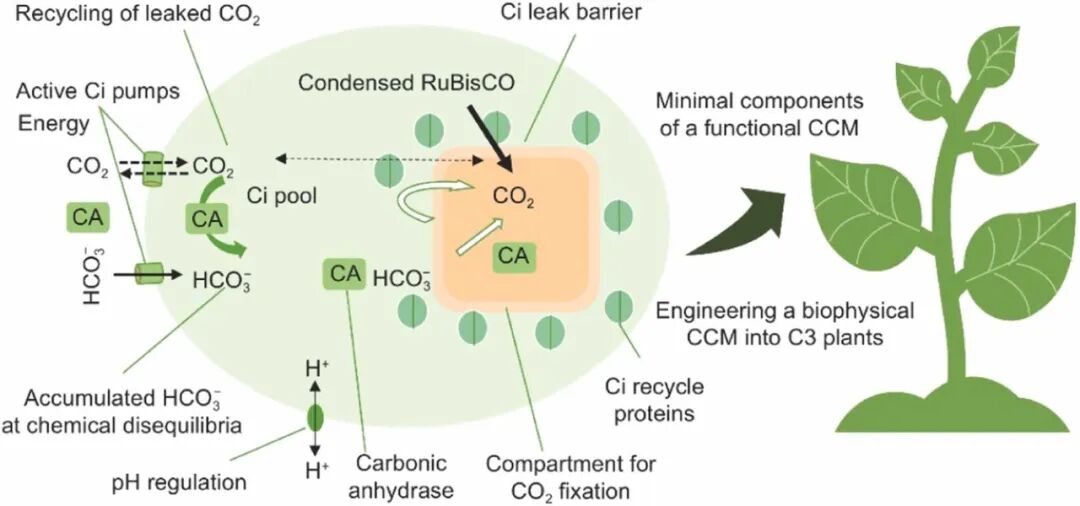
微藻作为光合生物,以其高效的碳固定效率而闻名。尽管它们仅占初级生产者总生物量的一小部分,其CO₂固定量却约占地球固碳总量一半。这种非凡能力主要归功于它们的生物物理性的二氧化碳浓缩机制(CO₂-concentrating mechanisms, CCMs)。CCM通过实现CO₂在固碳酶RuBisCO周围的富集,增强了其羧化活性,从而实现了CO₂的高效固定。此外,微藻还表现出高效的光捕获能力、强大的光保护能力以及较强的适应性和广泛分布性,这些特性进一步促成了它们高效的碳固定能力。解析微藻高效固碳的秘密,并将其转移到高等植物中,是提高作物产量和适应能力非常有前景的一种方法。
中国科学院植物研究所杨文强研究员团队于Green Carbon发表题为“The secret of high carbon fixation efficiency in chlamydomonas and its potential to boost yields in land plants”综述论文。论文以莱茵衣藻(Chlamydomonas reinhardtii)为例,系统的回顾了CCMs的发现过程、工作原理、构成的分子机制的研究成果和最新进展,并深入讨论了将基于蛋白核的CCM机制引入陆生植物以增强其光合性能的潜在应用和面临的挑战。
03 文章简介
简要介绍
地球上所有能接触到的有机碳均被认为是在某一时刻由核糖-1,5-二磷酸羧化酶/加氧酶(RuBisCO)固定CO₂产生的。尽管RuBisCO在固碳过程中发挥关键作用,但它的催化速率相对较慢,并且容易发生竞争性的加氧反应,导致能量浪费和固定CO₂的损失,尤其在C₃作物中,以成为限制光合固碳效率的关键因素。CCM是莱茵衣藻为克服RuBisCO的缺陷以及水生环境CO₂扩散速率慢的限制进化出来的特殊机制,它能将RuBisCO周围的CO₂浓度提升至环境浓度的1000倍以上,从而大大提高了RuBisCO的羧化活性。
CCM的运行依赖于不同膜定位的Ci转运蛋白和不同亚细胞定位的碳酸酐酶(carbonic anhydrase, CA)。莱茵衣藻中,这一高度有序且依赖光的过程可在外部Ci水平不足以维持高效光合作用的条件下被诱导激活,蛋白核是其核心组成部分(图1)。CCM的第一步是Ci的富集浓缩。衣藻通过膜定位的Ci转运蛋白以HCO₃⁻的形式主动摄取无机碳。由于HCO₃⁻不能自由穿过膜,因此可以更有效地积累在细胞内形成Ci库。第二步是利用蛋白核类囊体腔中定位的CA将HCO₃⁻转化为CO₂,释放在RuBisCO周围。此时的RuBisCO在支架蛋白EPYC1的帮助下发生相变,高度聚集,穿过蛋白核的类囊体形成网状结构。类囊体腔内的微管结构加速了光合固碳过程中的能量和物质交换,使得固碳效率大大提升。
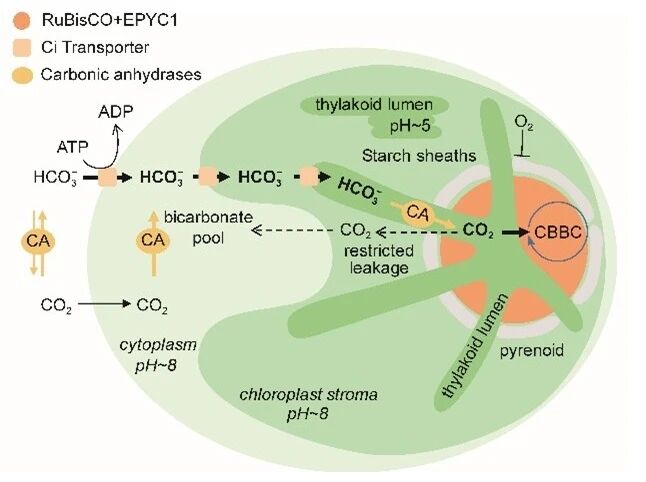
图1. 莱茵衣藻CCM的组分和过程
莱茵衣藻对Ci的吸收和富集涉及多种Ci转运蛋白,已经发现的有位于质膜上的HLA3和LCI1,位于叶绿体被膜上的LCIA、CCP1和CCP2,位于类囊体膜上的BST1–3。这些Ci转运蛋白的表达除受低CO₂条件的诱导外,还受到转录因子CIA5和LCR1以及CAS蛋白的调节。Ci的主动吸收是一个能量依赖的过程,需要消耗ATP,光合电子传递的各个途径和呼吸作用电子传递链均在其中发挥了重要作用。此外,研究表明,在CO₂限制条件下,微藻中PSI较PSII活性的比值会增强(图2)。
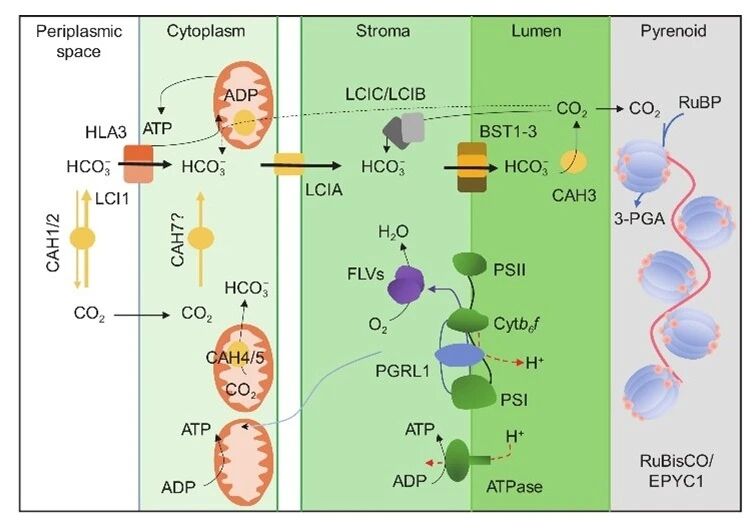
图2. 驱动CCM无机碳吸收和固定的能量来源
莱茵衣藻CCM机制的存在,使得其固碳效率高达5%~7%,远高于C3(~3.5%)和C4(~4.3%)植物。基于蛋白核的CCM在高等植物中的应用,理论上可以将其光合固碳效率提升60%。这一过程的成功实现大致可以分为五个步骤:第一步是将RuBisCO聚集到类似蛋白核的相分离液滴中;第二步涉及类囊体与RuBisCO聚集物的结合;第三步包括将CA引入到聚集体内的类囊体腔中;第四步涉及将HCO₃⁻转运蛋白定位于不同膜结构上;第五步围绕蛋白核体建立CO₂扩散屏障,并回收泄漏的CO₂。经过研究人员的不断努力,尽管存在诸多挑战,从简单的遗传操作扩展到综合的合成生物学策略,使得基于蛋白核的CCM在高等植物中的应用取得了初步的进展。
总结与展望
莱茵衣藻通过进化出基于蛋白核的生物物理型CCM,有效克服了低CO₂环境限制及RuBisCO酶固有的催化缺陷。相较于受限于复杂解剖结构(花环结构)的C4植物生化型CCM,衣藻的CCM策略更易于在异源系统中重构。本文综述了该机制的运行原理、关键元件及分子基础,并探讨了其在高等植物中应用的难点与挑战。这一工作为通过基因工程将CCM核心组件导入C3作物、大幅提升光合固碳效率提供了理论支撑,并在一定程度上指明了未来的研究方向。
04 作者简介

杨文强 教授
杨文强,国家级海外人才,国家植物园、中国科学院植物研究所研究员,中国科学院大学岗位教授。饲草种植高效设计与利用全国重点实验室课题组长,博士生导师。现任中国科学院植物所副所长、党委委员、中国科学院植物研究所光生物学重点实验室主任、中国科学院大学现代农学院作物生理与高效农业教研室主任。主要从事光合作用调控和豆科作物高光效相关研究。主持基金委、科技部、中国科学院和农业部多个项目。在Molecular Plant,PNAS,Plant Cell等期刊发表论文40余篇,参编著作5本。荣获中国科学院大学优秀教师、北京市教工委大中小幼教书育人特等奖和中国科学院“朱李月华”优秀教师奖。兼任中国植物学会和藻类学会理事、中国植物生理与分子生物学学会常务理事、中国空间生命科学与生物技术科学工作委员会委员等多个专委会委员。
中国科学院植物研究所杨文强研究员为论文的通讯作者,中国科学院植物研究所2024届博士李瑞姿(现已入职连云港市农业科学院)和博士后潘俊廷为论文共同第一作者。邢家乐博士为该论文撰写和修改提供了帮助和宝贵建议。该研究得到了国家重点研发计划(2021YFA0909600)、国家自然科学基金(U22A20445和32300220)、山东省自然科学基金(ZR2023ZD30)、黄河三角洲农业高新技术产业示范区的科技专项项目(2022SZX12)的资助。
05 Green Carbon
期刊官网:Green Carbon官网
投稿网址:Green Carbon投稿
公众号:Green Carbon公众号

https://blog.sciencenet.cn/blog-3620330-1530366.html
上一篇:Green Carbon文章 | 宁夏大学/天津大学王智文教授:利用甘油非平衡发酵的希瓦氏菌底盘适应性实验室进化
下一篇:Green Carbon文章 | 上海理工大学顾阳教授:工程化永达尔梭菌实现一碳气体高效合成乙醇