ВЉЮФ
ЙњздШЛШШЕу Ѓќ ЁАОВЯЂЁБЪЧЮѓНт ЁАM1M2ЁБ вбЙ§ЪБ зюШШЕФаЁНКжЪЯИАћКФНп, ФуБиаыСЫНт Ѓќ MCE
|
аЁНКжЪЯИАћЁЊЁЊФдЪЕжЪФкЮЈвЛЕФУтвпЯИАћЁЃЫцзХГЩЯёММЪѕНјВНЃЌШЫУЧЖдЦфШЯжЊДгЁАОВЯЂзДЬЌЁБзЊБфЮЊЁАМЋЖШЛюдОЕФЯИАћЁБЃЌЬиБ№ЪЧЦфЮшЖЏЕФЗжжІЁАУВЫЦЁБдкЬНВтжмЮЇзщжЏЁЂМрПиЩёОдЊЛюЖЏЃЌЪЙЕУаЁНКжЪЯИАћГЩЮЊЩёОПЦбЇСьгђбаОПШШЕуЁЃБОЦкдлУЧОЭРДпыпыаЁНКжЪЯИАћ~
Section.01
ШЯЪЖаЁНКжЪЯИАћ

ЯШРДНјаавЛВЈжЊЪЖИќаТ~
ЃЈвбеЦЮеЃЌЧыТдЙ§ЃЉ
ЪзЯШЃЁ
аЁНКжЪЯИАћВЂЗЧНіДцдкгкжаЪрЩёОЯЕЭГ

ЦфДЮЃЌ
вдЭљЪЙгУЕФвЛаЉЙуЗКЪѕгяКЭУќУћЃЌ
ЛђаэашвЊБЛжиаТЖЈвх......
аЁНКжЪЯИАћЃК ЁАОВЯЂЁБгыЁАМЄЛюЁБ
20 ЪРМЭ 70 ФъДњжаЦкЃЌЁАОВЯЂЁБКЭЁАМЄЛюЁБаЁНКжЪЯИАћетСНИіЪѕгяЪзДЮГіЯждкЮФЯзжаЃЌгУгкдкаЮЬЌбЇЩЯУшЪідкЩњРэ ("ОВЯЂ") КЭВЁРэ ("МЄЛю") ЬѕМўЯТЙлВьЕНЕФЖдвјШОгаЧзКЭСІЕФЯИАћЁЃетжжУќУћЗЈдк 20 ЪРМЭ 90 ФъДњЕУЕНЙуЗКЪЙгУЁЃ
ШЛЖјЃЌЫцзХНќаЉФъЫЋЙтзгЯдЮЂГЩЯёММЪѕЕФЗЂеЙЃЌШЫУЧж№НЅЗЂЯжаЁНКжЪЯИАћЪМжеЛюдОЃЌВЛЛсвђДДЩЫЁЂЫ№ЩЫЁЂИаШОЁЂМВВЁЕШЬєеНДгЁАОВЯЂЁБзЊБфЮЊЁАЛюЛЏЁБзДЬЌЁЃЯрЗДЃЌЫќГжајЛюдОЃЌЛсИљОнЩњУќНзЖЮЁЂжаЪрЩёОЯЕЭГЧјгђЁЂЮяжжЁЂадБ№МАНЁПЕЛђМВВЁЛЗОГВЩШЁВЛЭЌзДЬЌЁЂжДааВЛЭЌЙІФм (ЭМ 1)ЁЃЫљвдЃЌОЁЙмЁАОВЯЂЁБКЭЁАЛюЛЏЁБаЁНКжЪЯИАћШдБЛЙуЗКЪЙгУЃЌПЦбЇМвдНРДдНЖрЕФГЩЯёЪ§ОнЖдЁАМЄЛюЁБаЁНКжЪЯИАћИХФюЬсГіжЪвЩ[2]ЁЃ
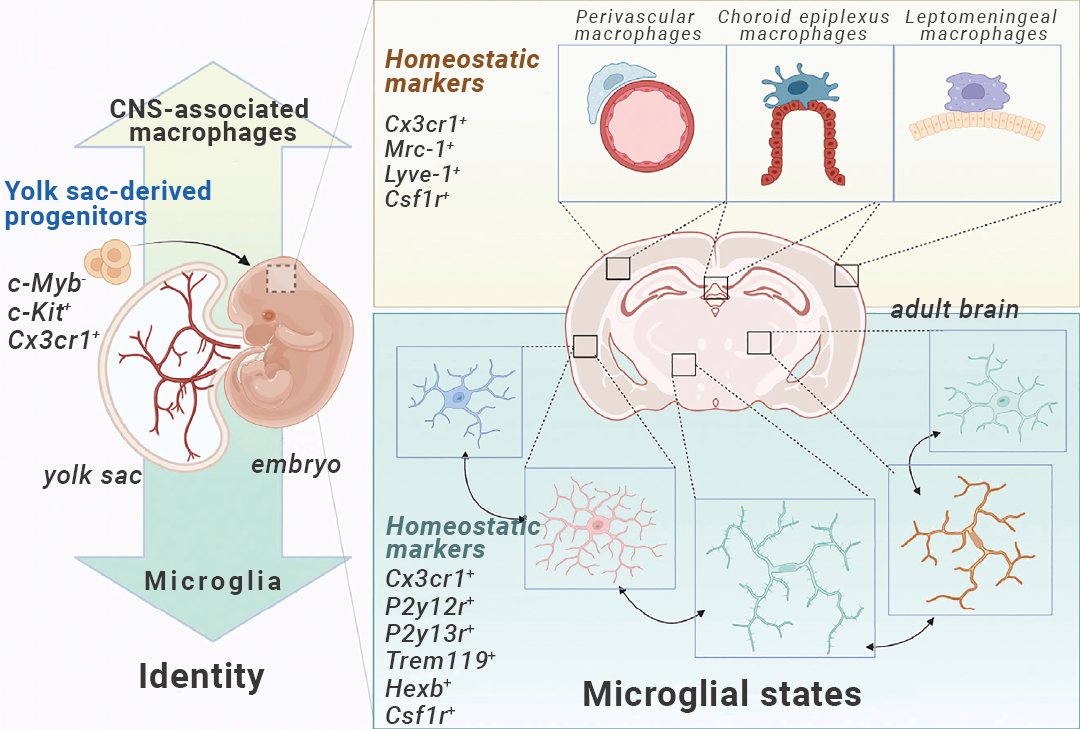
ЭМ 1. аЁНКжЪЯИАћЕФЩэЗнКЭзДЬЌ[2]ЁЃ
гыбЊЙмжмЮЇМфЯЖЁЂТіТчДдКЭШэФдФЄжаЕФЦфЫћжаЪрЩёОЯЕЭГЯрЙиОоЪЩЯИАћЯрБШЃЌаЁНКжЪЯИАћЕФЩэЗндкдчЦкОЭгЩТбЛЦФвРДдДЕФзцЯИАћШЗЖЈЁЃвЛЕЉЫќУЧдкФдЪЕжЪжаЖЈжВВЂЗжЛЏЃЌЫќУЧОЭПЩвдИљОнЬиЖЈЕФЪБПеЛЗОГГЪЯжЖржжзДЬЌЁЃ
аЁНКжЪЯИАћЃКM1 гы M2
21 ЪРМЭГѕЃЌУтвпбЇМвИљОнЬхЭтФЃаЭЕФбаОПНсЙћЖдОоЪЩЯИАћНјааЗжРрЃЌВЂЬсГіСЫСэвЛИіЪѕгяЃКЁАM1ЁБЃЌМДОЕфМЄЛюЃЌБЛШЯЮЊОпгаДйбзКЭЩёОЖОадЃЌгыЁАМЄЛюЁБаЁНКжЪЯИАћЕФИХФюУмЧаЯрЙиЃЌЖјЁАM2ЁБМДЬцДњМЄЛюЃЌБЛШЯЮЊОпгаПЙбзКЭЩёОБЃЛЄзїгУЁЃетаЉЪѕгядкаЁНКжЪЯИАћбаОПжаБЛЙуЗКВЩгУЁЃ
ШЛЖјЃЌКмПьЗЂЯжОоЪЩЯИАћЕФЗДгІБШМђЕЅЕФЁАM1ЁБКЭЁАM2ЁБИќИДдг (ЭМ 2)ЁЃОЭаЁНКжЪЯИАћЖјбдЃЌЕЅЯИАћММЪѕЕФГіЯжЬсЙЉСЫУїШЗЕФжЄОнЃЌБэУїЛюЬхФджаЕФаЁНКжЪЯИАћВЛЛсМЋЛЏЮЊетСНжжРрБ№жаЕФШЮКЮвЛжжЃЌЭЈГЃЭЌЪББэДя M1 КЭ M2 БъМЧЮяЁЃПЩвдДгБэЙлвХДЋбЇЁЂзЊТМзщбЇЁЂДњаЛзщбЇКЭЕААзжЪзщбЇЪ§ОнЕШЖрИіЮЌЖШећКЯаЁНКжЪЯИАћЕФЙВДцзДЬЌ[2]ЁЃ
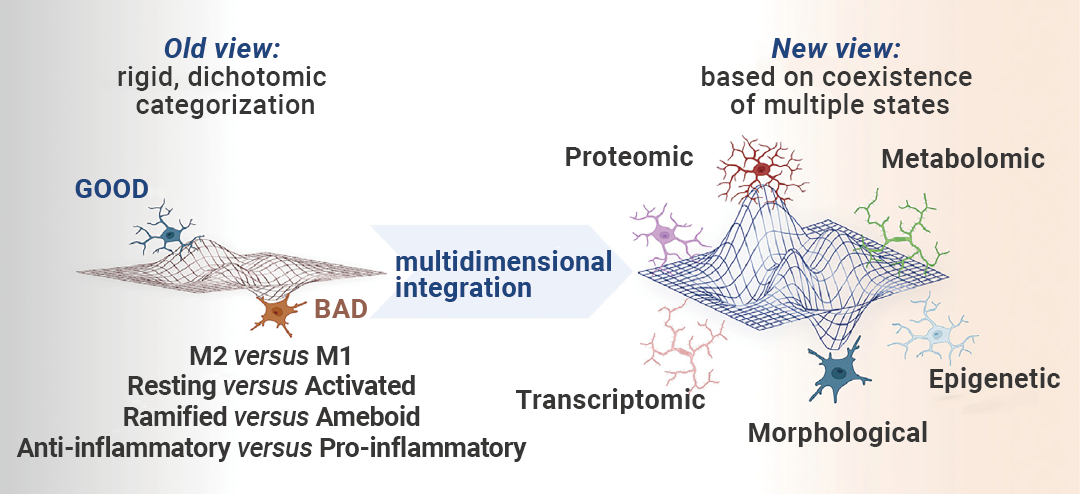
ЭМ 2. аЁНКжЪЯИАћУќУћЗЈЃКЙ§ШЅКЭЮДРД[2]ЁЃ
ОЁЙмФПЧАШдДцдкељвщЃЌЕЋЯраХдкВЛОУЕФНЋРДЃЌжеНЋЖдаЁНКжЪЯИАћЕФвЛаЉУќУћДяГЩЙВЪЖЁЃ
МђЕЅСЫНтКѓЃЌдлУЧбдЙще§ДЋЃКзїЮЊжаЪрЩёОЯЕЭГЕФГЃзЄУтвпЯИАћЃЌаЁНКжЪЯИАћЪЧДѓФдНЁПЕЕФЕквЛЕРЗРЯпЃЁ
ДѓФдЕФЁАЫЋУцЮРЪПЁБ
УтвпЯИАћЪЧУтвпЯЕЭГЕФживЊВПЗжЃЌЗжВМгкЩэЬхЕФИїИізщжЏЦїЙйЁЃCNS вВВЛР§ЭтЃЌаЁНКжЪЯИАћЪЧжаЪрЩёОЯЕЭГФкЙЬгаЕФЯШЬьУтвпЯИАћ[3]ЁЃ
ПДЕНетРяЃЌФуЪЧВЛЪЧЦШВЛМАД§ЯыЮЊаЁНКжЪЯИАћЬљЩЯЁАGoodЁББъЧЉЃП
ЕФШЗЃЌЩњРэзДЬЌЯТЕФаЁНКжЪЯИАћдк CNS ЗЂг§ЁЂЬхФкЦНКтКЭМВВЁжаЗЂЛгзХживЊзїгУЁЃЫќУЧФмДйНјЭЛДЅЕФЗЂг§КЭПЩЫмадЃЌЭЈЙ§ГжајМрВтЁЂЭЬЪЩЕђЭіЩёОдЊЛђЪмЫ№ЯИАћЫщЦЌЁЃаЁНКжЪЯИАћЛЙПЩдкЪмЕНДЬМЄЪБДЅЗЂУтвпЗДгІЃЌРДЮЌГжЩёОЯЕЭГЕФНЁПЕКЭЮШЬЌ (ЭМ 3)ЁЃ
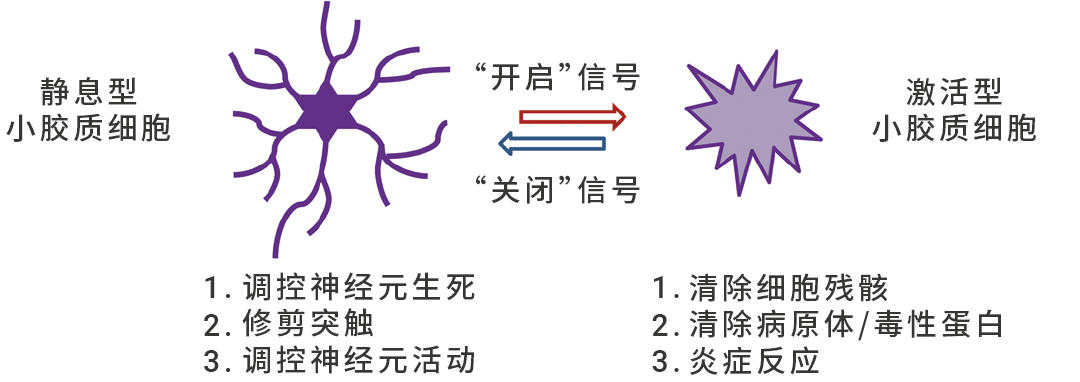
ЭМ 3. аЁНКжЪЯИАћЕФЛюЛЏ[4]ЁЃ
Section.02
аЁНКжЪЯИАћКФНп: CSF1Ri
ЭљЦкаЁ M вбИјДѓМвНщЩмЙ§ВЛЭЌЕФаЁНКжЪЯИАћЧхГ§ММЪѕЃЌШчРћгУЖОЫиЁЂCSF1R вЉРэадвжжЦМС (CSF1Ri)ЁЂТШьЂЫсбЮжЌжЪЬхКЭЙЙНЈвХДЋФЃаЭЕШЃЌУПжжММЪѕЖМгаЦфздЩэЕФгХЪЦКЭОжЯоад(ЯъМћ ДђПЊЩёОЯЕЭГЁАКкЯЛзгЁБ----ВйзнаЁНКжЪЯИАћвдЬНОПДѓФдЙІФм)ЁЃ
ЦфжаЃЌCSF1Ri (ДњБэадЛЏКЯЮяАќРЈPLX3397 КЭ PLX5622) ЦОНшЦфЖРЬигХЪЦЃЌБЛЙуЗКгІгУгкЩњРэЛђВЁРэЬѕМўЯТаЁНКжЪЯИАћЕФКФНп[6]ЁЃ
CSF1Ri ЧхГ§аЁНКжЪЯИАћЕФдРэЪЧЪВУДЃПЪЧЗёПЩФцЃПPLX5622 КЭ PLX3397 ЧјБ№ЪЧЪВУД...... Б№МББ№МБЃЌД№ЭъФуЕФД№ФуЕФЃЌД№ЭъФуЕФД№Ы§ЕФЃЌдлУЧНгзХПД~
CSF1Ri ЧхГ§ЛњжЦ
дРэЃКЮоХфЬхЪБЃЌCSF1R ДІгкЗЧЛюадзДЬЌЃЌЭЈЙ§здЮввжжЦЮЌГжЛюадЁЃЕБвЛжжХфЬхгыжЎНсКЯЃЌв§ЗЂ CSF1R ЭЌдДЖўОлЛЏЁЂЙЙЯѓзЊБфМАНќФЄНсЙЙгђ (JMD) ФкРвАБЫсВаЛљСзЫсЛЏЃЌНтГ§здЮввжжЦЃЌЪЙИќЖр ATP НјШыЁЃетДйЪЙИќЖрРвАБЫсВаЛљСзЫсЛЏЃЌЪЙ CSF1R ЭъШЋМЄЛюЃЌМЄЛюЯТгЮаХКХЭЈТЗЃЈШч PI3K/AktЁЂJNKЁЂERK1/2 КЭ JAK - STAT аХКХЭЈТЗЃЉЃЌДйНјАаЯИАћЃЈШчОоЪЩЯИАћЁЂаЁНКжЪЯИАћЁЂЕЅКЫЯИАћЕШЃЉдіжГЁЂЗжЛЏЁЂДцЛюгыЛюЛЏ[5][10][11]ЁЃ
CSF1RiЃЈШч PLX3397ЁЂPLX5622ЁЂBLZ945ЁЂJNJ-40346527ЁЂKi20227 КЭ GW2580ЃЉФмЙЛзшЖЯ CSF1R ЪмЬхЕФНсЙЙИФБфгыздСзЫсЛЏЃЌвжжЦаХКХДЋЕМЃЌжТЪЙаЁНКжЪЯИАћЩЅЪЇЩњДцаХКХЃЌНјЖјж№ВНБЛЧхГ§ЁЃЖјЧвЃЌЭЃгУетаЉвжжЦМСКѓЃЌаЁНКжЪЯИАћЛсбИЫйжиаТдіжГЁЊЁЊвВОЭЪЧЫЕЃЌCSF1Ri ЧхГ§ЪЧПЩФцЕФЁЃ
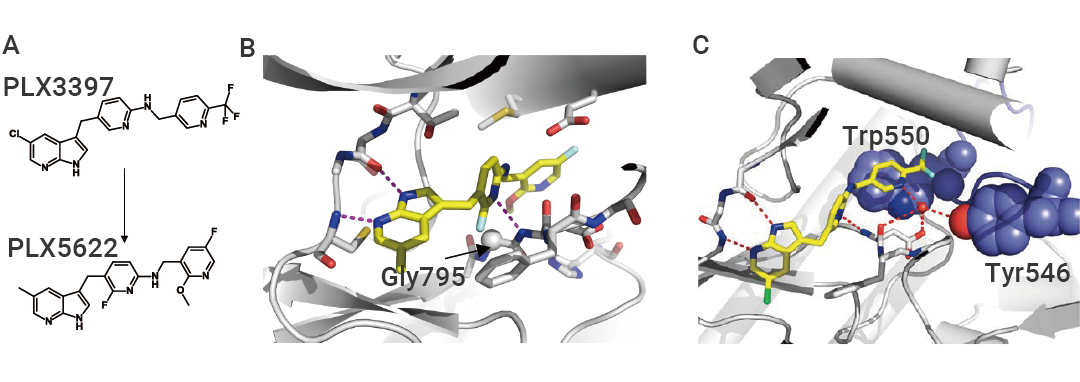
ЭМ 4. PLX3397 КЭ PLX5622 гы CSF1R ЕФНсКЯЮЛЕу[12][13]ЁЃ
A. PLX3397 КЭ PLX5622ЕФЛЏбЇНсЙЙЪНЁЃB. CSF1R-PLX5622 ИДКЯЮяЕФ X ЩфЯпОЇЬхНсЙЙЁЃC. CSF1R-PLX3397 ИДКЯЮяЕФ X ЩфЯпОЇЬхНсЙЙЁЃНсКЯЮЛЕуБэУїЃЌPLX3397 ФмЙЛгыНќФЄНсЙЙгђ (JMD) НсКЯЃЌЖј PLX5622 ФмЙЛЮШЖЈНсКЯдкБЛНќФЄНсЙЙгђ (JMD) ХХГтзпКѓаЮГЩЕФ CSF1R БфЙЙПкДќжаЃЌЧв PLX5622 ЩЯЕФ 2-ЗњШЁДњЛљЩьШы CSF1R ЬигаЕФ Gly795 ИННќПеМфЃЌЖј Gly795 дк KIT КЭ FLT3 ЖдгІЮЛжУЮЊНЯДѓЬхЛ§ЕФАыызАБЫсЃЌДгЖјЕМжТПеМфХХГтЃЌгАЯьећЬхНсКЯЮШЖЈадЃЌДгЖјБмУтСЫЖд KIT КЭ FLT3 ЕФЗЧЬивьНсКЯЁЃ
Бэ 1. PLX5622 КЭ PLX3397 ЩњЛЏаджЪКЭЯИАћФкЕФЛюадВювь (ІЬM)[12]ЁЃ
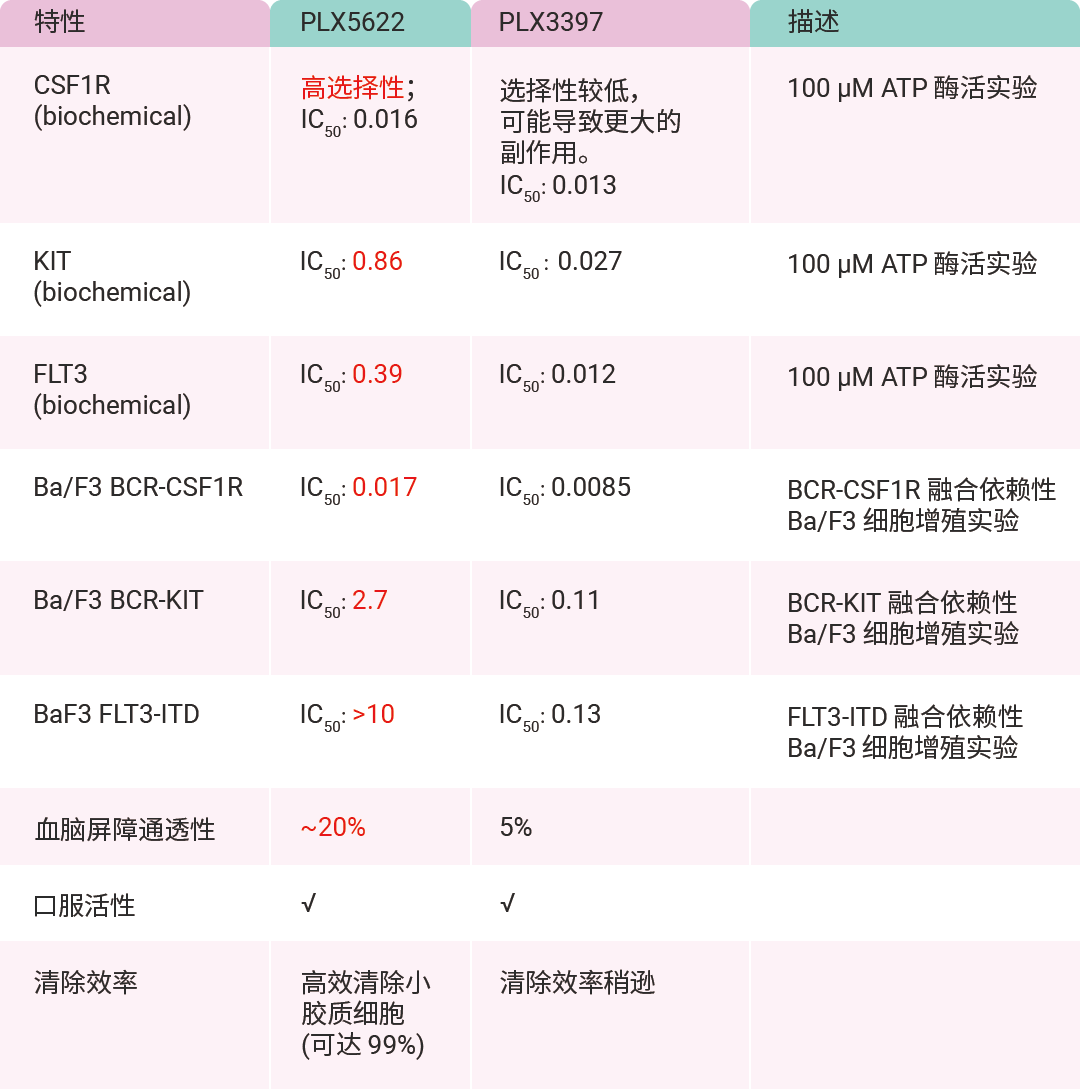
змЬхЖјбдЃЌЯрНЯгк PLX3397ЃЌ PLX5622 Жд CSF1R ЕФбЁдёадИќЧПЃЌЖд KIT КЭ FLT3 ЕФвжжЦЛюадвВИќШѕЁЃдк CSF1R вРРЕадЪдбщжаЃЌPLX5622 еЙЯжГігы PLX3397 ЯрНќЕФаЇСІЁЃШЛЖјЃЌдк KIT вРРЕадЪдбщжаЃЌPLX5622 ЕФаЇСІБШ PLX3397 ЕЭдМ 30 БЖЁЃ
MCE бщжЄЃКPLX5622
MCE ПЩЬсЙЉИпДПЖШЃЌИпаЁНКжЪЯИАћЧхГ§аЇТЪЃЌХњДЮМфЮШЖЈЕФ PLX5622ЃЌВњЦЗвбОЙ§ MCE ЪЕбщЪвзЈвЕЕФЩњЮябщжЄЃК7 ЬьаЁНКжЪЯИАћЧхГ§ТЪПЩДя 87%ЃЌ 14 ЬьПЩДя 90% (ЭМ 5)ЁЃ
? ЪЕбщЖЏЮяЃКалад C57BL/6 аЁЪѓ (11-12 жм)
? МССПЃКздгЩЩуШЁКЌ 1,200 ppm PLX5622 ЕФ AIN-76A ЫЧСЯ 7 ЬьЛђ 14 Ьь
? МьВтжИБъЃКФдзщжЏжа IBA1+ (аЁНКжЪЯИАћБъжОЮя) ЯИАћЪ§ФП
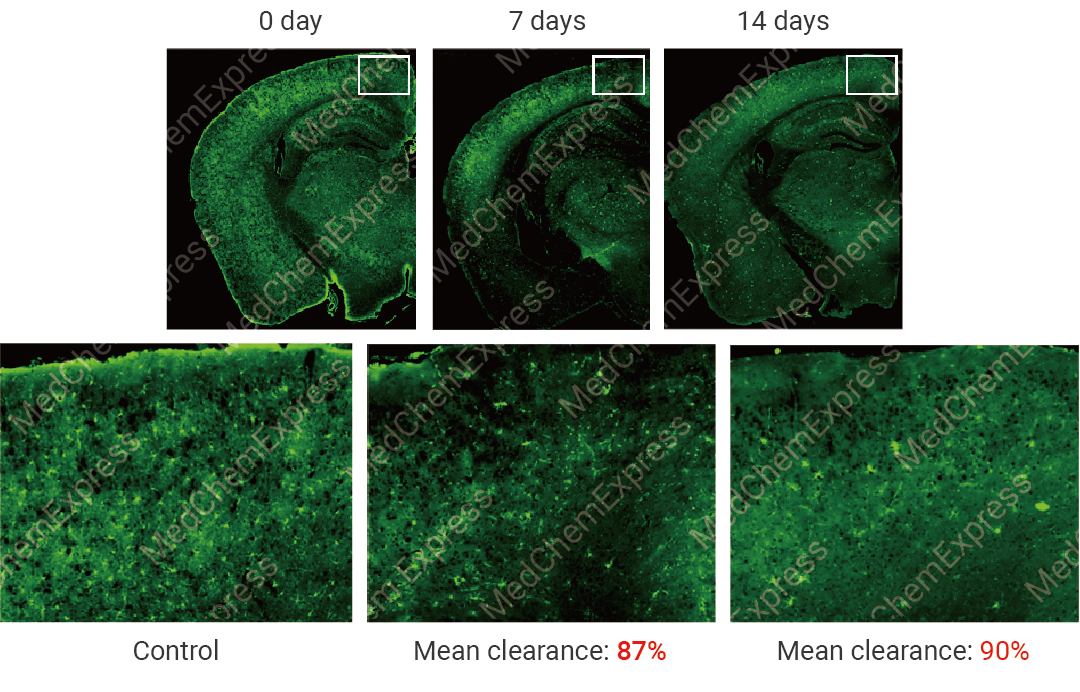
ЭМ 5. MCE ЪЕбщЪвЖд PLX5622 ЧхГ§ФдВПаЁНКжЪЯИАћЕФаЇЙћбщжЄЁЃ
ВњЦЗЭЦМі |
ПкЗў CSF1R вжжЦМСЃЌФмЭИЙ§бЊФдЦСеЯЕФЁЂаЁНКжЪЯИАћЧхГ§ЛЏКЯЮяЁЃ |
PLX5622 ЫЧСЯаЮЪНЃЌ1,200 ppmЁЃдљЫЭПеАзЖдееЫЧСЯЃЌЬсЙЉЗјеежЄУїЁЃ |
бЁдёадКЭФдЩјЭИадЕФ CSF1R вжжЦМСЃЌIC50 ЮЊ 1 nMЁЃ |
бЁдёадЕФЁЂОпгабЊФдЭЈЭИадКЭПкЗўЛюад CSF1R вжжЦМСЃЌIC50 ЮЊ 3.2 nMЁЃ |
ПкЗўгааЇЃЌИпбЁдёад CSF1R вжжЦМСЃЌIC50 ЮЊ 2 nMЁЃ |
ПкЗўгааЇЕФЃЌбЁдёадЕФ c-Fms МЄУИвжжЦМСЁЃ |
ЭУРДдДЁЂЮоХМСЊБъМЧЁЂПЙ IBA1 (аЁНКжЪЯИАћБъжОЮя) ЕФ IgG ЕЅПЫТЁПЙЬхЁЃ |
HY-AF0005ЃЌгеЕМЗЪХжЁЂЬЧФђВЁФЃаЭДПЛЏаЭЫЧСЯЁЃ |

[1] Wang Z, et al. An immune cell atlas reveals the dynamics of human macrophage specification during prenatal development. Cell. 2023 Sep 28;186(20):4454-4471.e19.
[2] Paolicelli RC, et al. Microglia states and nomenclature: A field at its crossroads. Neuron. 2022 Nov 2;110(21):3458-3483.
[3] Angiulli F, et al. Blood-Based Biomarkers of Neuroinflammation in Alzheimer's Disease: A Central Role for Periphery? Diagnostics (Basel). 2021 Aug 24;11(9):1525.
[4] LI Hui-Quan, et al. The multiple roles played by microglia. Chinese Bulletin of Life Sciences. 1004-0374(2014)06-0620-06.
[5] Elmore MR, et al. Colony-stimulating factor 1 receptor signaling is necessary for microglia viability, unmasking a microglia progenitor cell in the adult brain. Neuron. 2014 Apr 16;82(2):380-97.
[6] Kim N Green, et al. To Kill a Microglia: A Case for CSF1R Inhibitors. Trends Immunol. 2020 Sep;41(9):771-784.
[7] Sara Bachiller, et al. Microglia in Neurological Diseases: A Road Map to Brain-Disease Dependent-Inflammatory Response. Front Cell Neurosci. 2018 Dec 18;12:488.
[8] Gao, C, et al. Microglia in neurodegenerative diseases: mechanism and potential therapeutic targets. Sig Transduct Target Ther 8, 359 (2023).
[9] Tahmasebi F, et al. The Role of Microglial Depletion Approaches in Pathological Condition of CNS. Cell Mol Neurobiol. 2023 Aug;43(6):2459-2471.
[10] Weyer MP, et al. Repurposing of pexidartinib for microglia depletion and renewal. Pharmacol Ther. 2024 Jan;253:108565.
[11] Xiang C, et al. Targeting CSF-1R represents an effective strategy in modulating inflammatory diseases. Pharmacol Res. 2023 Jan;187:106566.
[12] Spangenberg E, et al. Sustained microglial depletion with CSF1R inhibitor impairs parenchymal plaque development in an Alzheimer's disease model. Nat Commun. 2019 Aug 21;10(1):3758.
[13] Tap WD, et al. Structure-Guided Blockade of CSF1R Kinase in Tenosynovial Giant-Cell Tumor. N Engl J Med. 2015 Jul 30;373(5):428-37.
[14] Han J, et al. Inhibition of colony stimulating factor-1 receptor (CSF-1R) as a potential therapeutic strategy for neurodegenerative diseases: opportunities and challenges. Cell Mol Life Sci. 2022 Apr 2;79(4):219.
[15] Wu Z, et al. Peripheral nervous system microglia-like cells regulate neuronal soma size throughout evolution. Cell. 2025 Apr 17;188(8):2159-2174.e15.
https://blog.sciencenet.cn/blog-3536222-1507133.html
ЩЯвЛЦЊЃКCisplatinЫГВЌЩіЫ№ЩЫФЃаЭЙЙНЈЃќCisplatinЫГВЌШмНтЗНАИЃќMCE
ЯТвЛЦЊЃК(S)-AMPAЃЌ83643-88-3ЃЌЁн99.0%_MedChemExpress
ШЋВПзїепЕФЦфЫћзюаТВЉЮФ
- • AI ЩИбЁ + ащФтЩИбЁЃКаТвЉбаЗЂЕФ ЁАЫЋв§ЧцЁБ ЕФКЫаФТпМ_MCE(MedChemExpress)
- • AACR ТфФЛЃЌaiвЉЮяЩИбЁЁЂаЁЗжзгвЉЮяЁЂЩњЮявЉЁЂПЙЬхХМСЊвЉЮяADC МЏССЯр_MCE
- • Neuron | TEE ЭЈЙ§ ReExc-BLAInh ЛиТЗФцзЊЧщаїеЯА_MCE(MedChemExpress)
- • ВЛжЙЛљвђгыЕААзЃЌЬЧДњТые§ГЩЮЊМВВЁеяСЦаТУмдП_MCE(MedChemExpress)
- • РрЦїЙйЖрЮЌМјЖЈЃЈЛљвђВтађЕШЃЉ__ MCE (MedChemExpress)
- • ПЙЬхХМСЊвЉЮя ADC КЭздЩэУтвпадМВВЁ_MCE(MedChemExpress)