博文
Viruses:新型RSV minigenome平台提升抗病毒药物筛选效率
||
研究背景
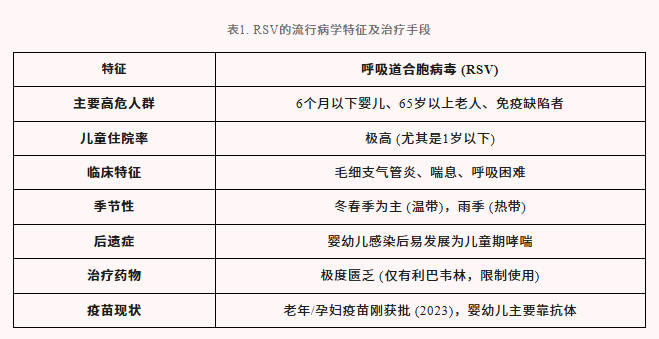
呼吸道合胞病毒 (RSV) 是导致全球婴幼儿严重下呼吸道感染的重要病原,也对老年人和免疫功能低下人群构成显著威胁。当前RSV防治手段仍较有限,而药物研发又长期受制于活病毒筛选带来的高生物安全风险、低通量和长周期等瓶颈,因此建立安全高效的替代筛选体系已成为抗RSV新药研发的关键需求。
近日,深圳湾实验室吴超研究员团队提出一种区别于传统活病毒策略的创新方案:构建基于NanoLuc与sfGFP的“双报告微型基因组系统”,在不产生完整感染性病毒颗粒的前提下,真实模拟RSV在细胞内的复制与转录过程,为聚合酶抑制剂的高通量筛选提供了更安全、可靠且高效的平台。
工作原理与优势
图1展示了RSV双报告微型基因组系统的基本原理:研究人员将微型基因组与辅助质粒共同转入细胞后,可在无活病毒参与的情况下重建RSV的转录与复制过程,并同步产生sfGFP绿色荧光与NanoLuc发光两种报告信号,从而实现对病毒复制活性的可视化和高灵敏定量检测。相比传统体系,该系统兼具高灵敏度、原位可视化和高通量筛选三大优势,为抗RSV药物发现提供了更安全、可靠且高效的实验平台。
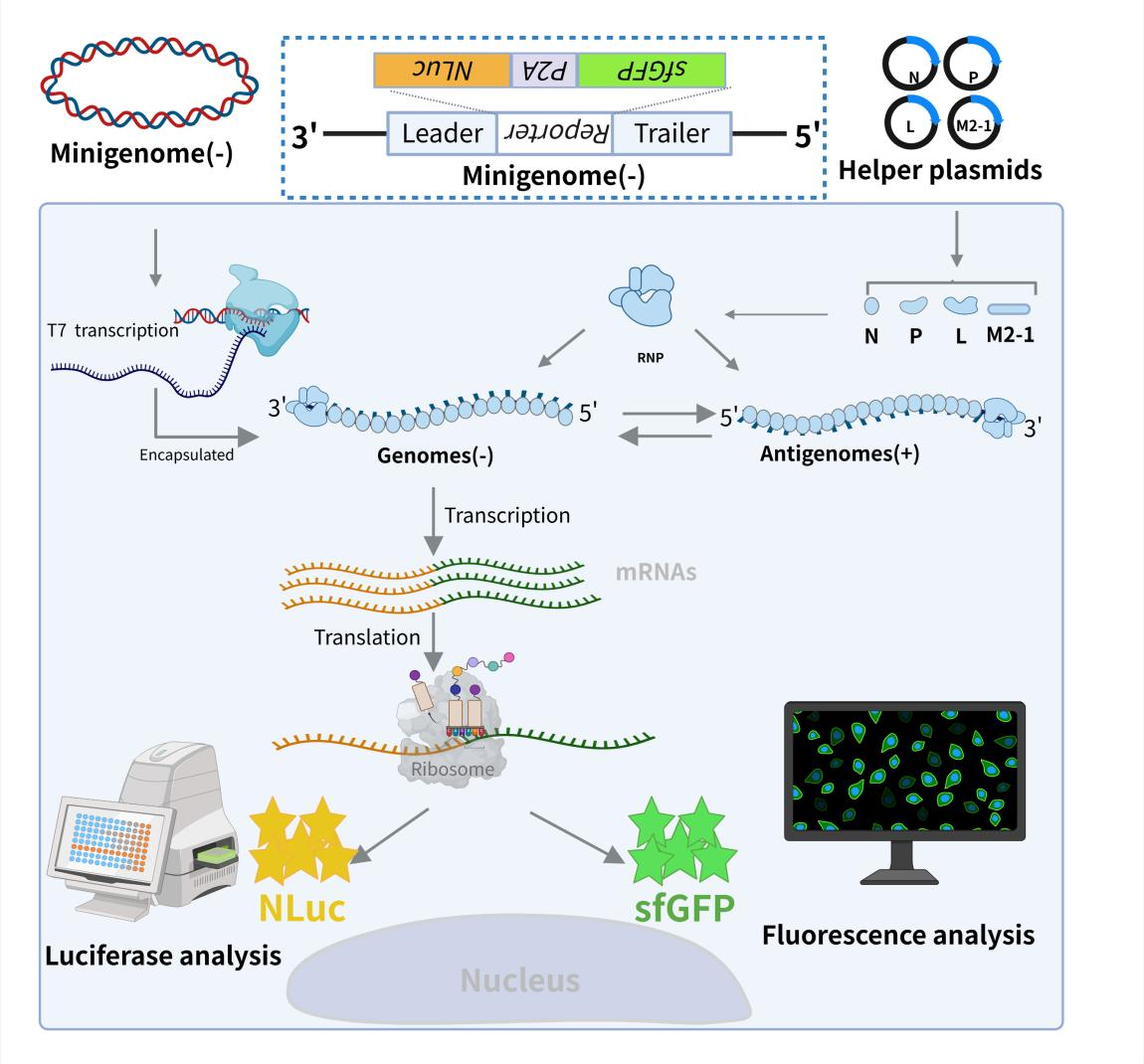
图1. RSV微型基因组工作原理示意图
研究结果
研究团队利用两种已知靶向RSV L蛋白的小分子抑制剂对该系统进行了验证。结果表明,随着药物浓度升高,sfGFP荧光与NanoLuc发光信号均同步呈剂量依赖性下降,且两者始终保持良好线性相关,说明该双报告系统能够通过双重信号一致性可靠反映病毒复制抑制效应,显著降低筛选中的假阳性和假阴性风险
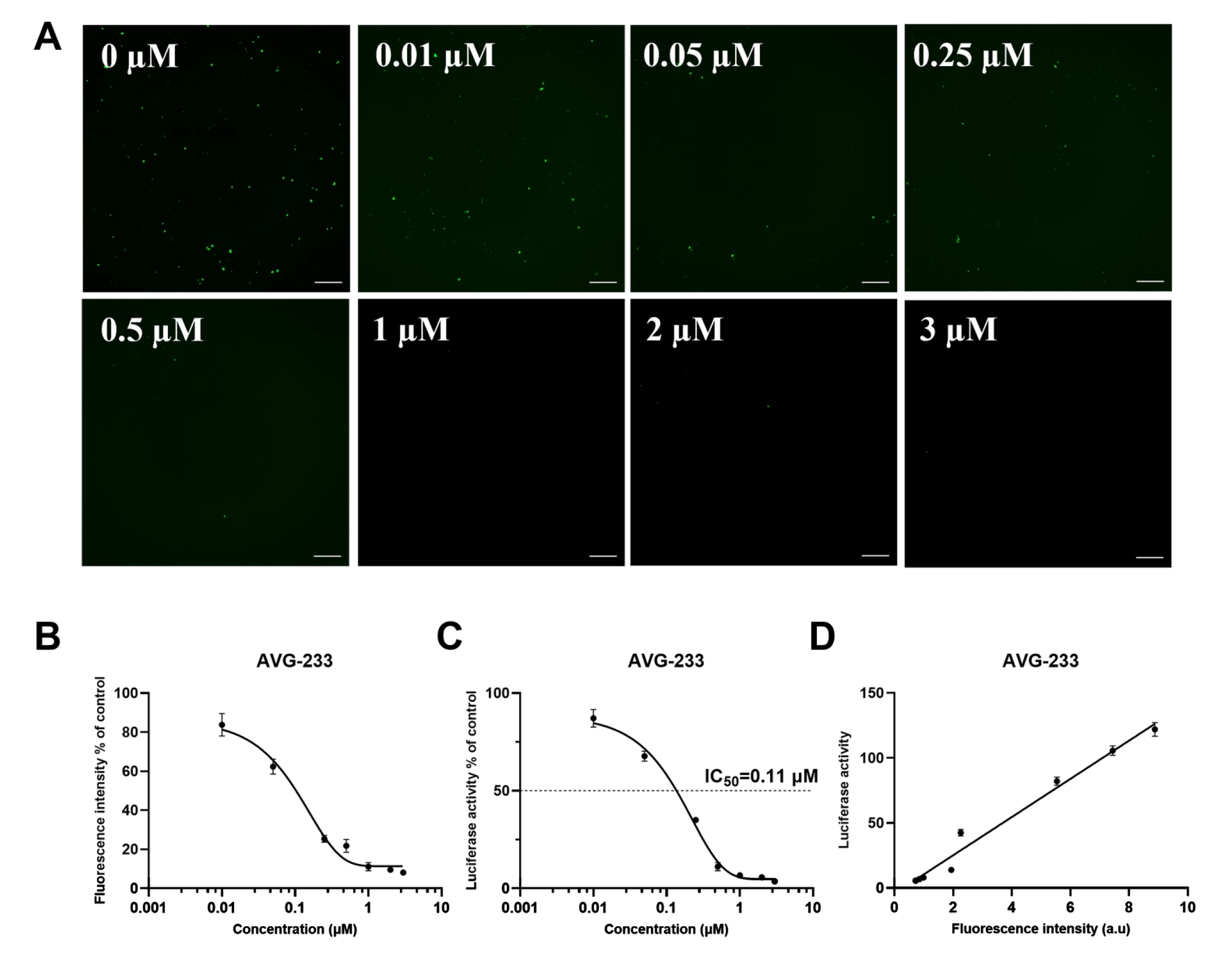
图2. AVG-233处理下Mini-NLuc-sfGFP系统中报告基因信号分析
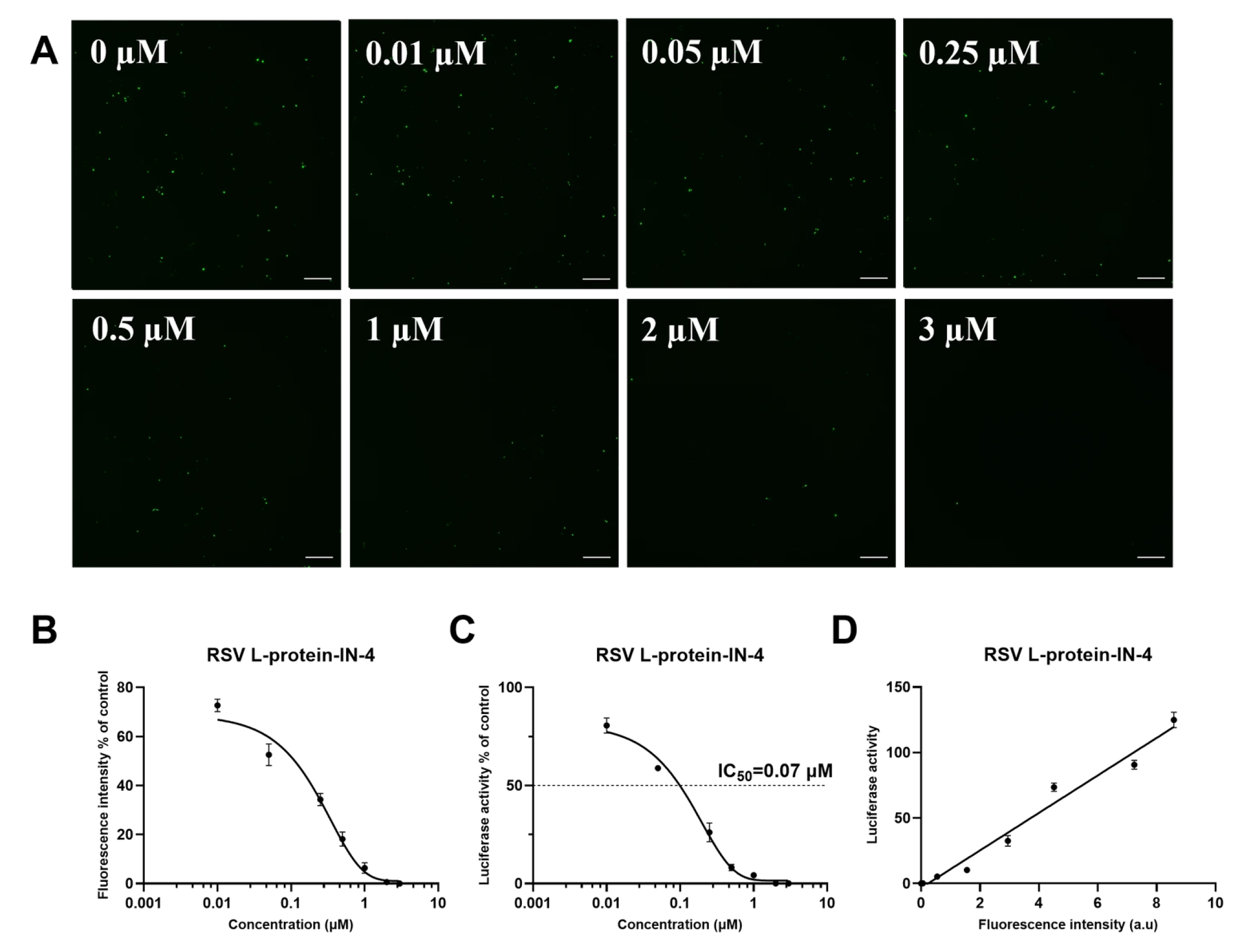
图3. RSV L-protein-IN-4处理下Mini-NLuc-sfGFP系统中报告基因信号分析
研究团队进一步在真实RSV感染模型中验证了上述结果,发现两种小分子抑制剂同样可剂量依赖性地减少感染并抑制病毒基因组复制,说明双报告微型基因组系统的检测结果与真实病毒抑制效应具有良好一致性。
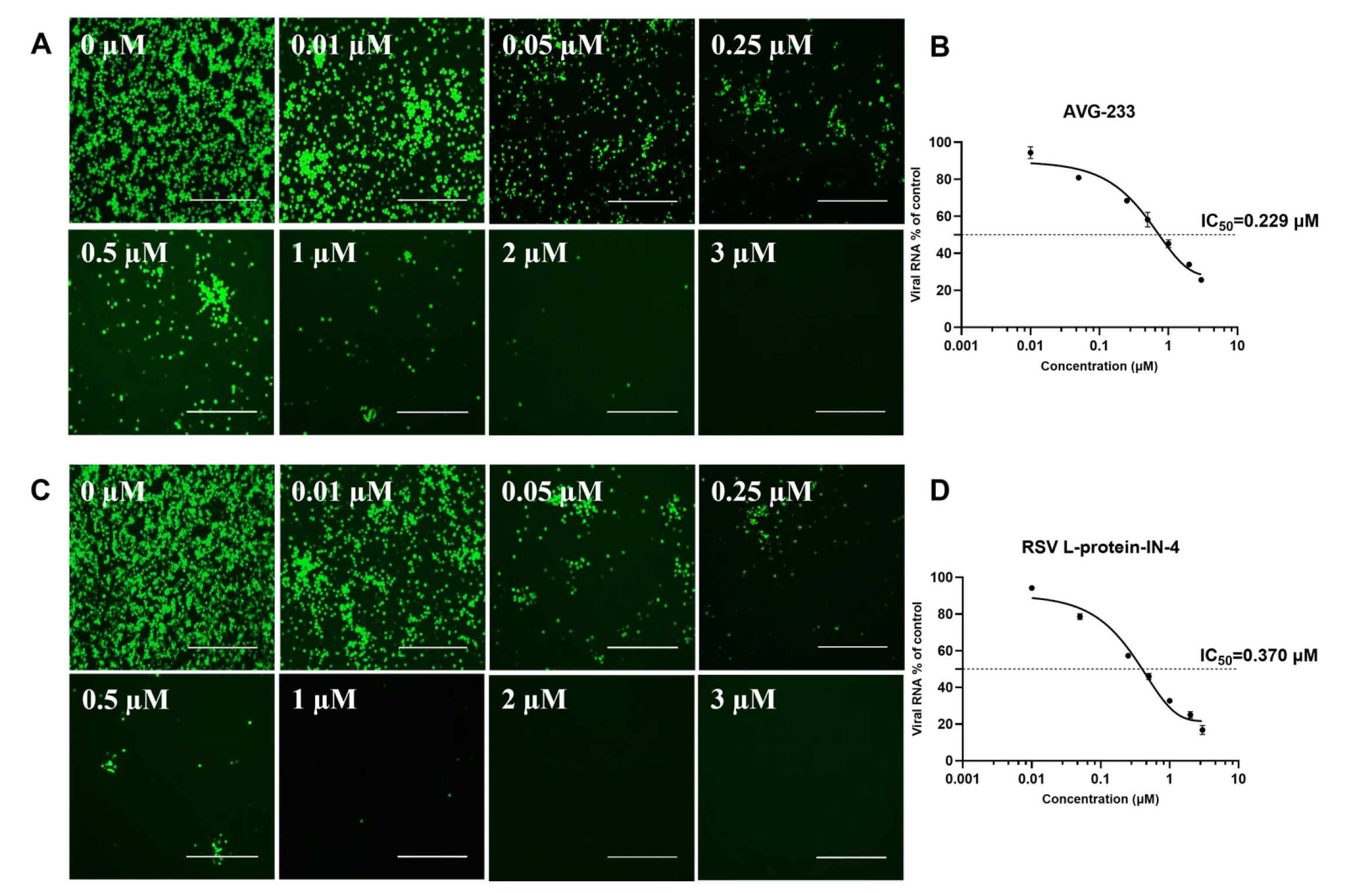
图4. 免疫荧光验证两种小分子化合物的抗RSV活性
结论
综上,该双报告微型基因组系统不仅可作为抗RSV药物筛选与药效预测的高效初评平台,更通过融合NanoLuc的精准定量优势与sfGFP的可视化能力,推动抗病毒研发由传统活病毒依赖模式向安全、可扩展的新模式转变,并为其他病毒研究提供了可借鉴的通用技术思路。
阅读英文原文:https://www.mdpi.com/1999-4915/18/3/304
Viruses 期刊介绍
主编:Eric O. Freed, Center for Cancer Research, USA
涵盖人类病毒和病毒疾病,动物病毒,植物病毒,病毒免疫、疫苗和抗病毒药物以及朊病毒等各方面研究,目前已被 SCIE (Web of Science)、MEDLINE (PubMed) 等数据库收录。
2024 Impact Factor:3.5
2024 CiteScore:7.7
Time to First Decision:17.2 Days
Acceptance to Publication:2.7 Days
期刊主页:https://www.mdpi.com/journal/viruses

https://blog.sciencenet.cn/blog-3516770-1532576.html
上一篇:Foods:谷蛋白是健康风险还是营养资源?
下一篇:Agriculture 南京林业大学生态与环境学院的程虎副教授、祝艳副教授共同创建特刊:农业土壤中的微纳塑料污染