博文
Pathogens 李密、舒红兵研究:Phyaslin F经AFG3L2介导VISA/MAVS降解抑制RNA病毒固有免疫
||
文章导读
RNA病毒感染后,病毒RNA被RIG-I样受体 (RLRs) 识别,与锚定在线粒体外膜上的病毒诱导信号接头蛋白VISA (又名MAVS、IPS-1) 的CARD结构域发生相互作用,触发固有免疫应答 (Innate Immune Response)。VISA的活性受到严格调控,其异常激活或抑制会导致免疫疾病或感染失控。关于由VISA介导的先天性抗病毒反应是如何受调控的,以及是否能够作为药物开发的靶点来对抗由RNA病毒感染所引发的疾病,这些都有待进一步研究。
2026年1月,武汉大学李密、舒红兵研究组在 Pathogens 期刊发表了题为“Physalin F Promotes AFG3L2-Mediated Degradation of VISA/MAVS to Suppress Innate Immune Response to RNA Virus”的研究文章,首次发现天然化合物Physalin F能够通过直接结合并激活线粒体蛋白酶AFG3L2,促进先天免疫信号通路中的关键接头蛋白VISA/MAVS的降解,从而抑制宿主对RNA病毒的先天免疫反应。该研究不仅揭示了一种全新的RLR信号通路负调控机制,也为治疗由RNA病毒引起的过度免疫反应相关疾病提供了新的潜在药物靶点。
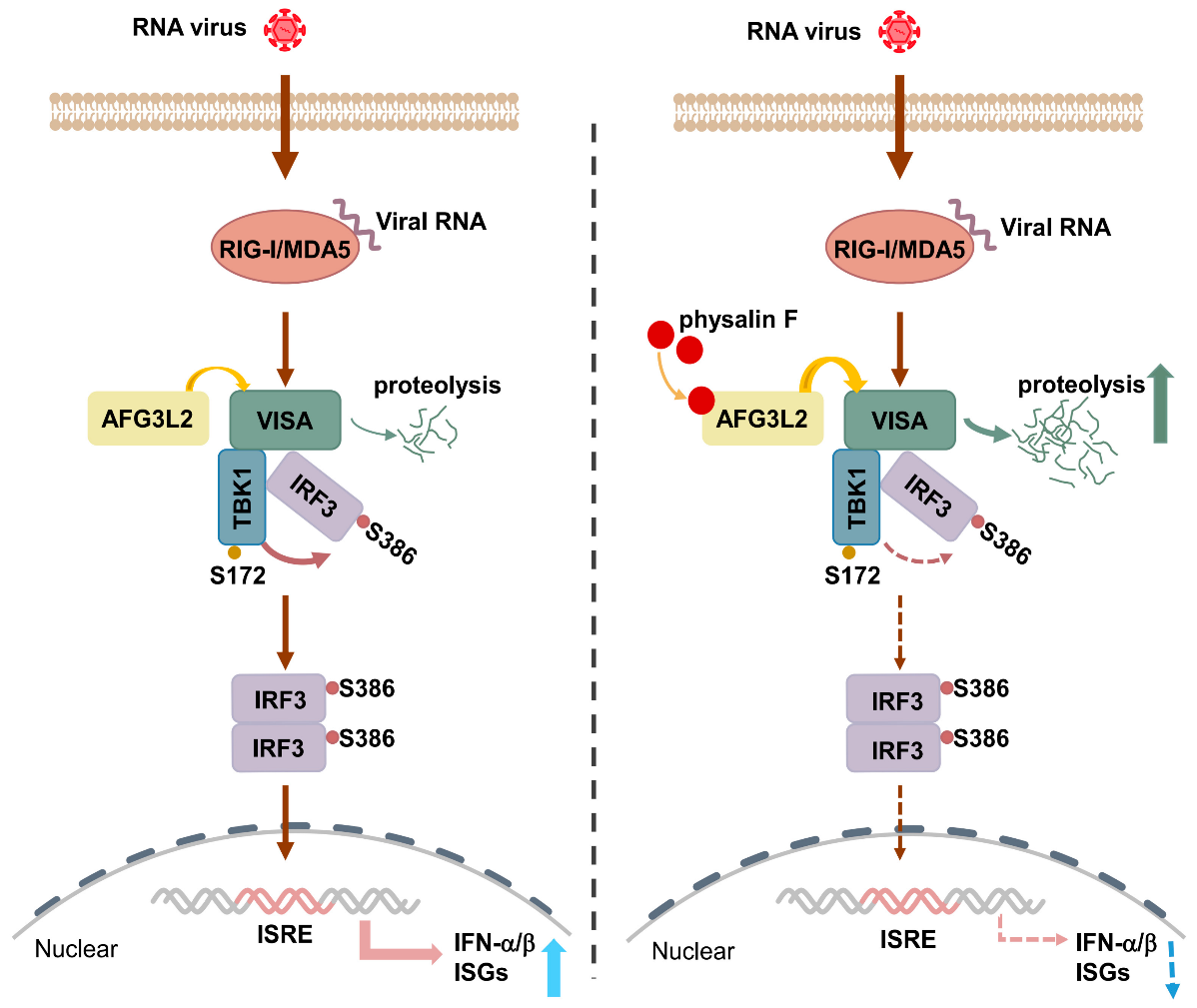
Physalin F-AFG3L2抑制RNA病毒固有免疫应答
研究过程与结果
为了鉴定固有免疫应答的天然小分子抑制剂,作者设计了一种高通量功能性筛选方法,从一个包含903种来源于植物、微生物等天然小分子化合物库中,寻找能够抑制RNA病毒 (如仙台病毒) 诱导的抗病毒效应基因表达的活性分子。通过系统性的筛选,一种来源于灯笼果的环状多氧甾体类天然产物,Physalin F在多种人源细胞系、小鼠原代免疫细胞以及小鼠体内模型实验中,均显示出抑制RNA病毒触发的先天免疫信号的活性。
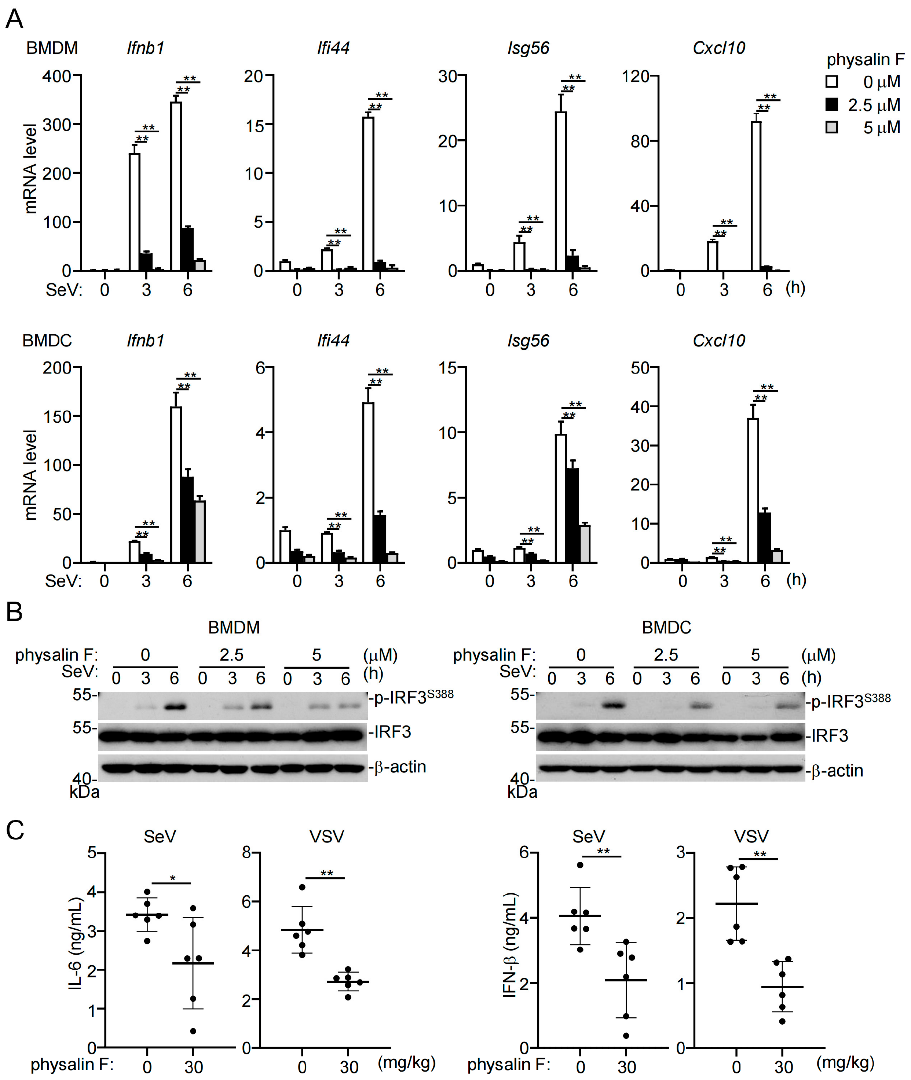
在原代小鼠细胞系和小鼠实验中,Physalin F抑制RNA病毒诱导的固有免疫应答 (原文图2)
接下来,作者通过有限蛋白酶解耦合质谱 (LiP-MS) 和细胞热转移实验 (CETSA),鉴定出线粒体m-AAA蛋白酶AFG3L2是Physalin F的直接结合靶点。
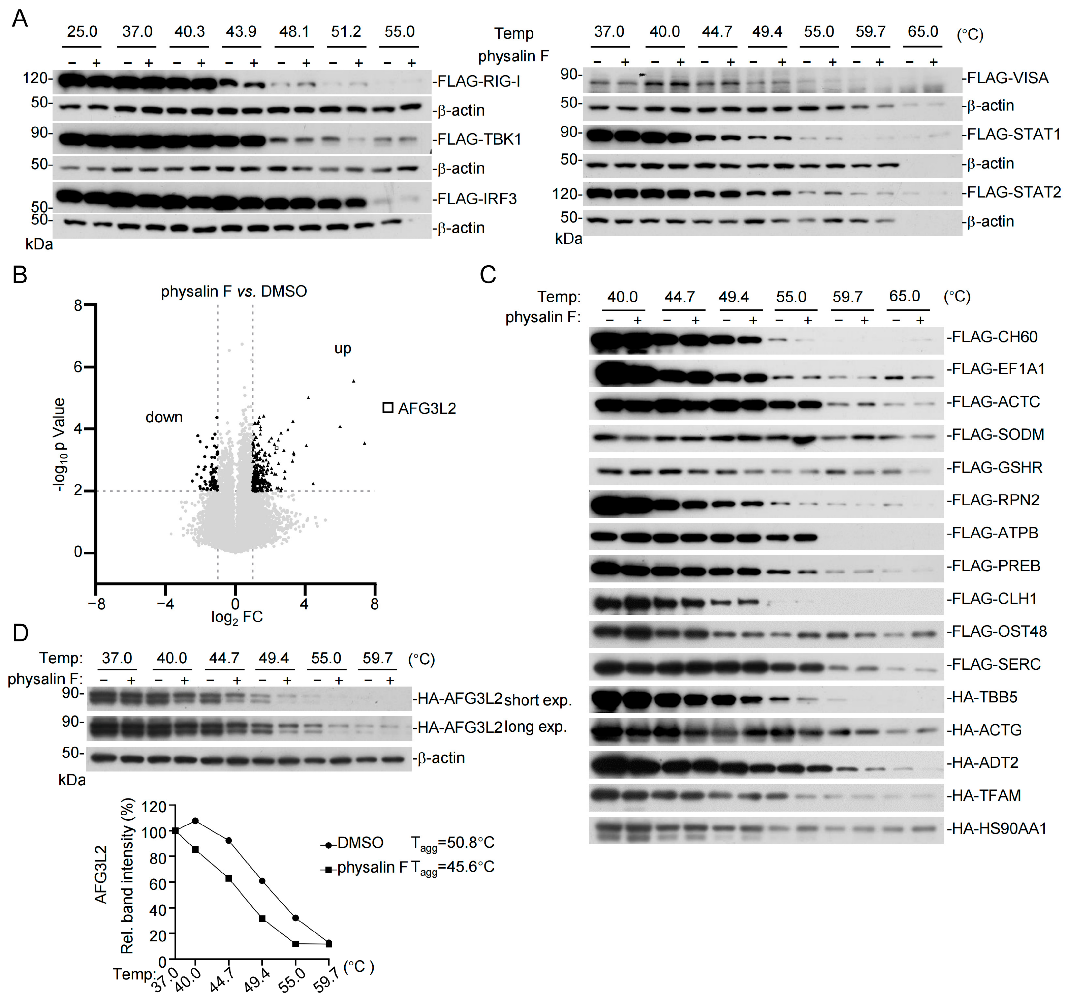
鉴定AFG3L2为Physalin F的作用靶点 (原文图3)
作者进一步探究并验证了 AFG3L2 能够通过Physalin F来抑制先天性抗病毒信号传导,并通过实验探索了其中的作用机制。AFG3L2在生理条件下持续降解位于线粒体外膜的先天免疫信号枢纽蛋白VISA,以维持其基础水平,防止自身免疫激活。Physalin F结合AFG3L2后,增强其蛋白酶活性,从而加速VISA的降解,进而抑制由RIG-I样受体介导的整个下游抗病毒信号通路。敲低AFG3L2会增强抗病毒信号并升高VISA蛋白水平;而过表达AFG3L2则抑制信号。更重要的是,AFG3L2的蛋白酶活性缺失突变体无法介导VISA降解和Physalin F的抑制作用,证明了其蛋白酶活性的关键作用。
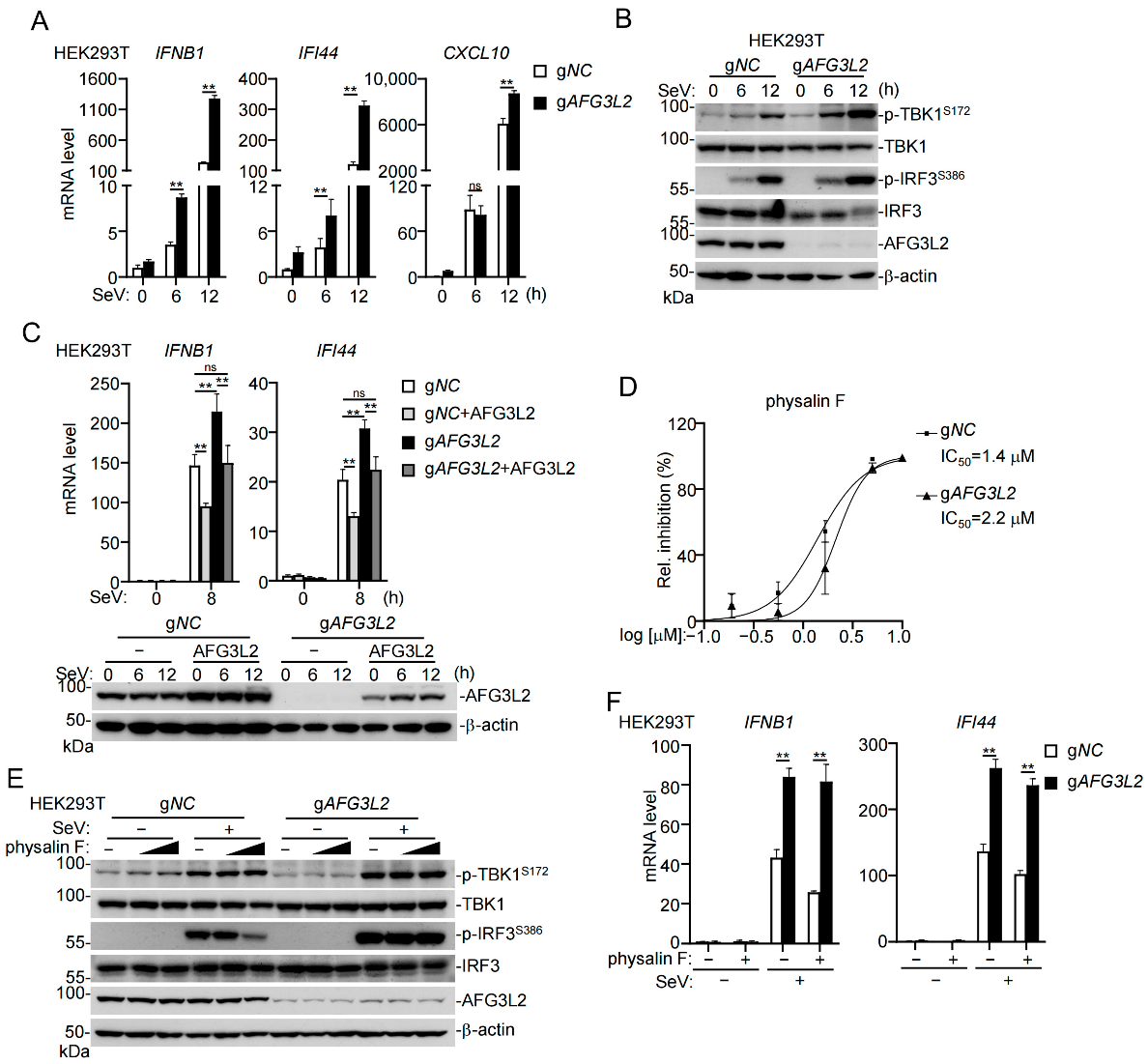
Physalin F通过靶向AFG3L2负反馈调节先天抗病毒反应 (原文图4)
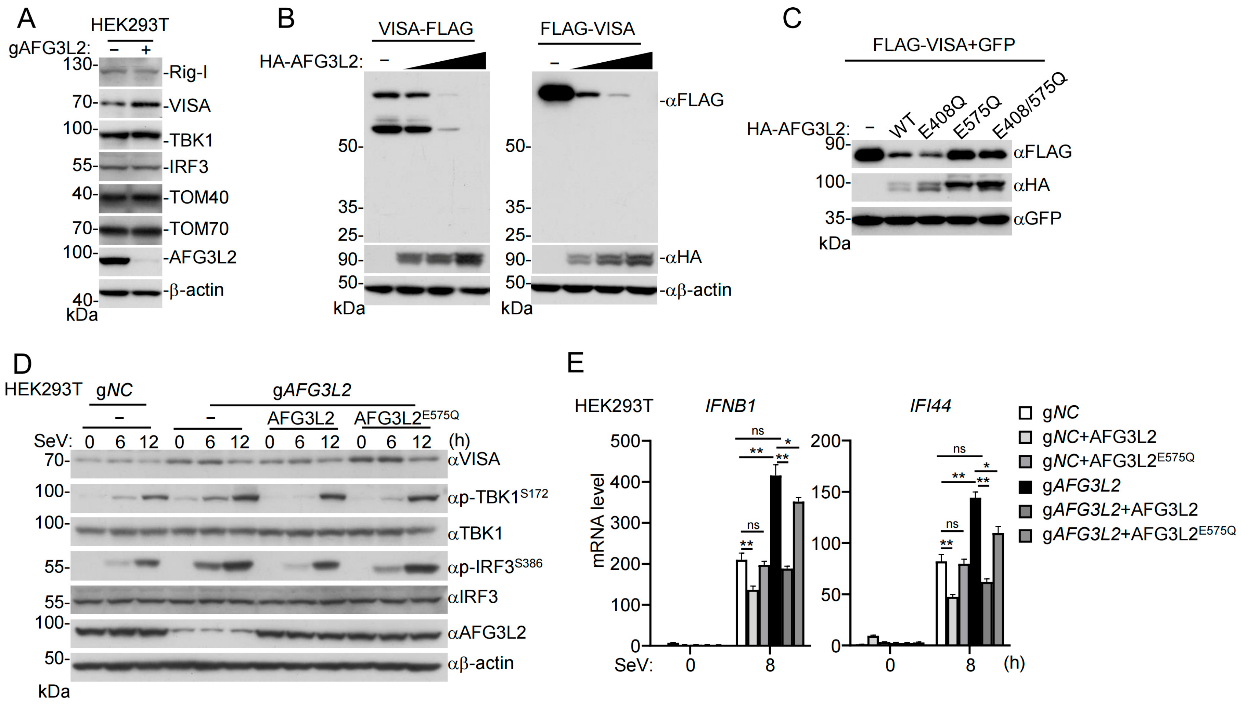
AFG3L2通过降解VISA负反馈调节抗病毒先天免疫 (原文图5)
最后,结合作者过往研究成果,通过构建三种AFG3L2截断体,精确定位Physalin F结合域及功能关键位点,发现Physalin F结合于AFG3L2的锌金属蛋白酶结构域,具体位于氨基酸739-750区域。
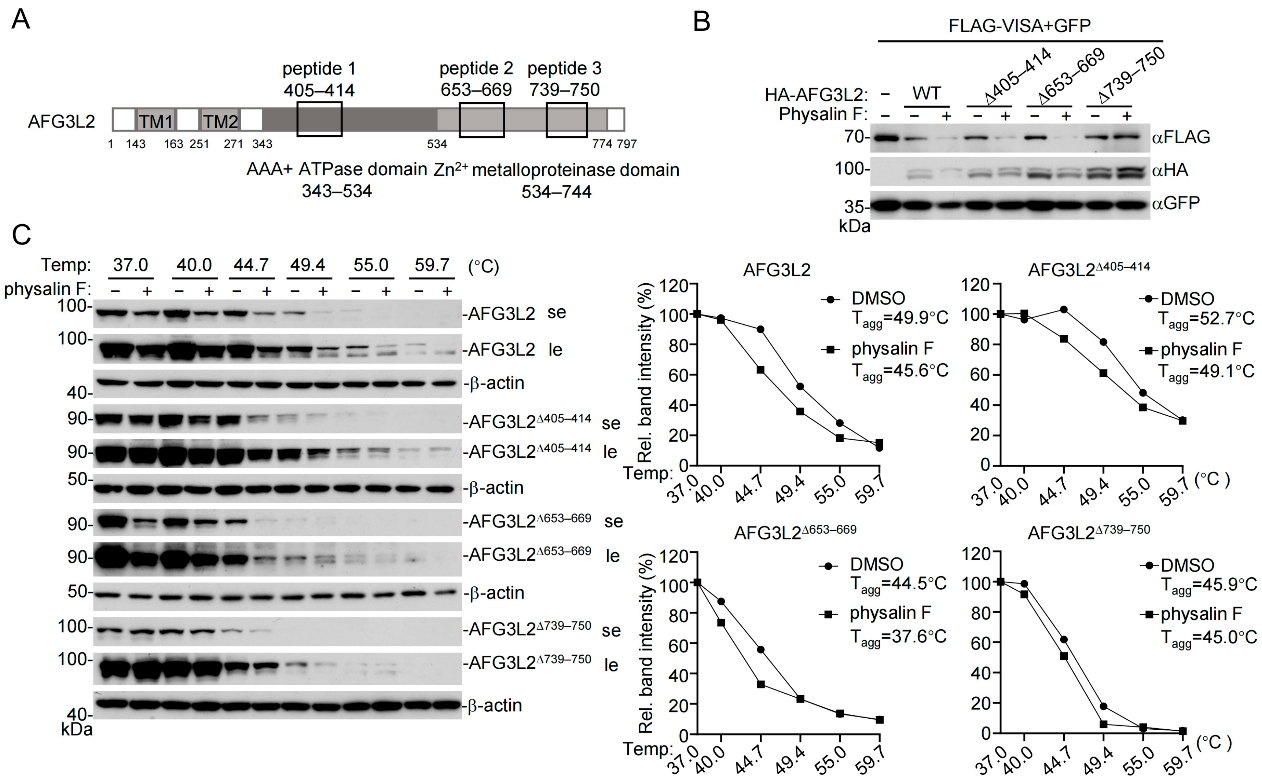
AFG3L2中physalin F位点的定位 (原文图6)
研究总结
本文聚焦于RNA病毒触发的先天免疫反应调控机制,是一项从现象到机制、从靶点发现到功能验证的系统性工作。研究团队从903种天然小分子化合物中,通过高通量筛选发现Physalin F (来源于灯笼果的环状多氧甾体) 能显著抑制仙台病毒诱导的I型干扰素表达。进一步机制研究揭示,Physalin F通过直接结合线粒体m-AAA蛋白酶AFG3L2 (位于线粒体内膜),增强其蛋白酶活性,从而加速先天免疫信号枢纽蛋白VISA/MAVS的降解。
该研究首次提出AFG3L2介导的VISA降解是RLR通路的生理性负反馈机制,发现了一条全新的免疫负调控通路,为理解免疫稳态调控提供了新视角,同时为开发基于天然产物的免疫调节剂奠定了理论基础,指出了潜在的药物研发新方向。
阅读英文原文:https://www.mdpi.com/2076-0817/15/1/74
Pathogens 期刊介绍
主编:Hinh Ly, University of Minnesota, Saint Paul, USA
期刊涵盖有关病原体和病原体与宿主相互作用的所有方面研究,为该领域提供前沿的学术交流平台。期刊已经被 Scopus、SCIE (Web of Science)、PubMed、PMC 、MEDLINE 等数据库收录。
2024 Impact Factor:3.3
2024 CiteScore:6.8
Time to First Decision:14.1 Days
Acceptance to Publication:2.6 Days
期刊主页:https://www.mdpi.com/journal/pathogens

https://blog.sciencenet.cn/blog-3516770-1527498.html
上一篇:Veterinary Sciences:兽医学与生命科学领域重印本推荐
下一篇:Agronomy和Genes期刊3月31日中国科学院动物研究所专场 | MDPI 作者培训会