博文
Nutrients:中国农业大学王勤教授团队——蒲公英多糖通过激活AKT/mTOR通路逆转小鼠肥胖
||
研究背景
脂质沉积 (即脂肪堆积) 是当前全球性的健康问题,与肥胖、2型糖尿病、心血管疾病及非酒精性脂肪性肝病等慢性代谢性疾病密切相关。高脂饮食 (HFD) 已被广泛证实可促进这类疾病的发生。尽管已有多种药物 (如西布曲明、奥利司他等) 用于肥胖治疗,但其潜在副作用和成瘾风险限制了临床应用。
近年来,天然多糖类成分——尤其是来自蒲公英的多糖 (TMPs)——显示出抗肥胖潜力。研究表明,TMPs能够抑制体重增加、改善胰岛素抵抗、调节糖脂代谢,并可能通过抑制胰脂肪酶活性及调节血脂水平发挥作用,但其具体活性成分及作用机制尚不明确。
AKT/mTOR信号通路在细胞生长、代谢、脂肪形成和能量稳态中起核心调控作用,并参与白色脂肪向棕色脂肪的转化 (褐变) 过程。该通路对产热和葡萄糖稳态具有重要影响,但其在米色脂肪形成中的具体作用尚存争议。基于上述背景,中国农业大学王勤教授团队提出假设:TMPs可能通过调控AKT-mTOR通路,改善高脂饮食诱导的肥胖及相关脂质代谢异常。
研究设计
该研究将30只6周龄健康雄性小鼠随机分为正常饮食组 (Control)、高脂饮食组 (HFD) 及高脂饮食添加0.3% TMPs干预组 (HFD-TMP),每组10只;ND组饲喂标准饲料,HFD组饲喂60%高脂饲料,HFD-TMP组在HFD饲料基础上补充0.3% TMPs。所有小鼠在标准明暗循环环境下单笼饲养,分组采用随机盲法进行。本研究进行了葡萄糖耐量试验 (GTT) 和胰岛素耐量试验 (ITT),小鼠禁食12小时后分别腹腔注射葡萄糖 (2 g/kg) 或胰岛素 (1 U/kg),并于注射后不同时间点检测血糖浓度。实验第10周,将小鼠置于4℃冷环境中12小时,采用数字温度计测量直肠核心温度,并利用红外热成像仪记录棕色脂肪组织 (BAT) 温度。血清样本经离心分离后,采用ELISA法检测炎症标志物水平。取肝脏和脂肪组织,经福尔马林固定、乙醇梯度脱水、石蜡包埋和切片后,进行苏木精-伊红 (H&E) 染色,并于显微镜下观察形态。采用TRIzol法提取组织总RNA,经质量检测后逆转录为cDNA,使用SYBR Green系统进行实时荧光定量PCR (qPCR),以检测相关基因表达。采用Western Blotting检测目标蛋白表达。组织蛋白经RIPA裂解、BCA定量后,进行SDS-PAGE电泳并转膜,经封闭后依次孵育一抗 (4 ℃过夜) 和二抗 (室温1小时),TBST洗涤后成像。抗体包括C/EBPβ、PRDM16、UCP1、PGC1α、Akt/p-Akt、mTOR/p-mTOR (1:1000),以β-actin为内参。蛋白表达量通过灰度值分析并归一化处理。
表1.qRT-PCR引物序列。
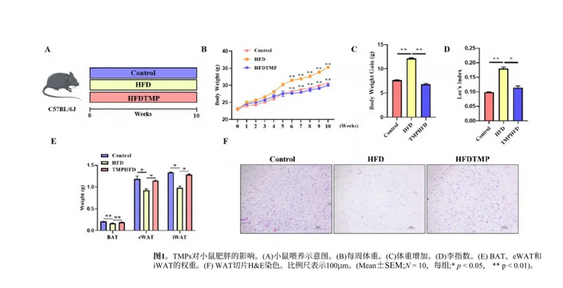
为了研究TMPs对肥胖的影响,小鼠被喂食HFD、HFD中添加0.3% TMPs (HFDTMP) 或对照饮食10周 (图1A)。服用HFD的老鼠比对照组的老鼠体重要高。然而,这种差异在补充TMP后得到了缓解 (图1B,C, p < 0.01)。由于Lee' s指数是评价动物肥胖程度的有效指标之一,故小鼠Lee' s指数被考虑在内。与HFD组相比,HFDTMP组的Lee' s指数显著降低 (图1D, p < 0.05)。hfd喂养的小鼠显示腹腔内脂肪的积累增加,而摄入TMP明显减轻了这种积累。此外,虽然HFD导致BAT、eWAT和iWAT的体重升高,但HFDTMP组的体重接近对照小鼠的平均体重 (图1E, p < 0.05)。三组之间的食物摄入量没有显著差异 (图S1)。此外,H&E染色组织学检查显示,补充TMPs的小鼠在WAT中显示出脂肪细胞大小 (图1F)。
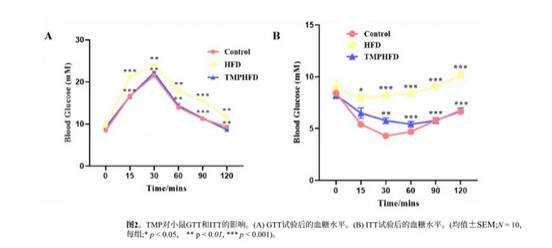
GTT结果表明,与HFD组相比,HFDTMP组的小鼠表现出更好的葡萄糖耐量 (图2A)。此外,ITT结果显示HFDTMP组小鼠的胰岛素敏感性增加 (图2B)。
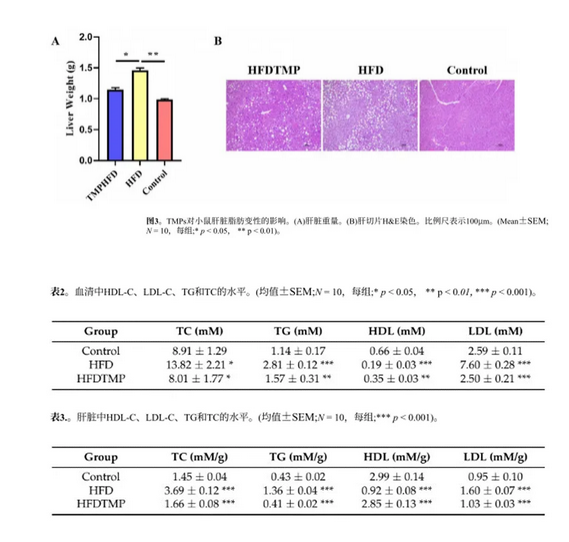
HFD的消耗导致肝脏重量的增加,这可以通过补充TMPs有效地逆转 (图3A)。使用H&E染色的组织学检查表明,消耗HFD导致肝脏中异常的甘油三酯积累。然而,补充HFDTMP的小鼠表现出最小的脂质沉积 (图3B)。正如预期的那样,给小鼠喂食HFD 10周会导致高脂血症,其特征是血清和肝脏中高密度脂蛋白胆固醇 (HDL-C) 水平降低,低密度脂蛋白胆固醇 (LDL-C)、甘油三酯[19]和总胆固醇 (TC) 水平升高 (分别见表2和表3)。值得注意的是,与HFD组相比,HFDTMP组在高脂血症方面有明显改善 (表2)。
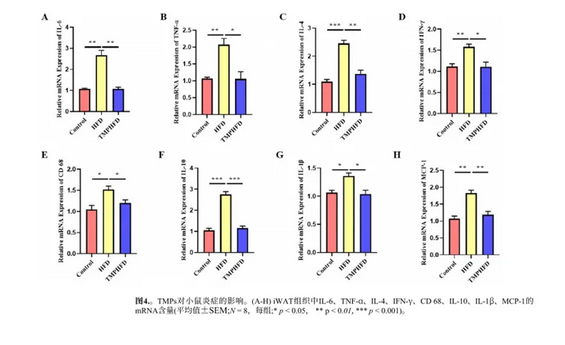
为了研究TMPs对小鼠炎症的影响,该研究采用ELISA、RT-qPCR和Western blotting来测量炎症标志物的水平。ELISA结果显示,HFD组小鼠血清中白细胞介素6 (IL-6)、白细胞介素10 (IL-10) 和肿瘤坏死因子α (TNF-α) 水平升高,而TMP可显著减轻HFD诱导的炎症 (表4)。此外,TMP可显著降低IL-6、TNF-α、白细胞介素4 (IL-4)、IL-1β、干扰素-γ (IFN-γ)、cd68、白细胞介素1β (IL-1β)和单核细胞趋化蛋白-1 (MCP-1)。此外,与对照组相比,这些标记物的蛋白表达水平显著降低 (图4A-H)。总体而言,研究结果表明MPs可能主要通过抑制这些基因的表达来减轻炎症。
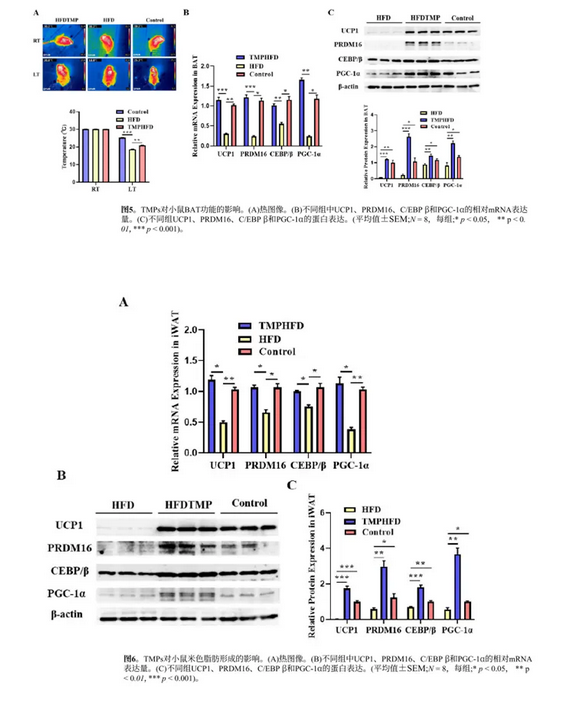
在冷暴露前,各组之间的体表温度没有明显差异。然而,在冷刺激后,喂食HFD的小鼠表面温度显著低于鼠粮组 (p < 0.01)。补充TMP可有效缓解这种下降 (p < 0.05)。与对照小鼠相比,饲喂HFD的小鼠的BAT表现出与白色脂肪相似的表型。然而,饮食中的TMPs显著降低了BAT中的脂质积累 (图5B)。此外,摄入TMP后,hfd喂养小鼠BAT中PRDM16、UCP1、PGC-1α和CEBP/β的mRNA和蛋白质水平也有所恢复 (图5C, p < 0.01)。HFDTMP组的iWAT中多室米色脂肪细胞的积累更多 (图6A, p< 0.05)。此外,在添加TMPs的小鼠iWAT中,产热基因的mRNA表达显著升高 (图6B, p < 0.05),表明米色脂肪细胞的形成增强。关键蛋白成分 (包括UCP1、PRDM16、PGC-1α和CEBP/β) 的改变证实这一观察结果。
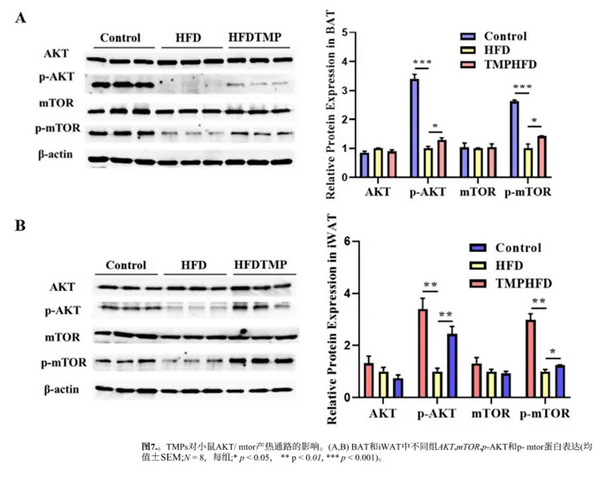
结果显示,hfd喂养小鼠BAT和iWAT中p-AKT和p- mtor蛋白水平均降低 (图7A,B, p< 0.05)。TMP处理显著缓解了这种抑制,HFDTMP组BAT和iWAT中p-AKT和p- mtor的相对蛋白水平均恢复 (图7A,B, p < 0.05)。
研究总结
本研究探讨了TMPs对高脂饮食 (HFD) 诱导肥胖小鼠的改善作用。结果表明,补充TMPs显著减轻了小鼠体重增长,改善了胰岛素敏感性和葡萄糖耐量,提示其可能通过抑制α-葡萄糖苷酶活性减少葡萄糖吸收,并促进胰岛素分泌。此外,TMPs有效降低了血清总胆固醇、甘油三酯和低密度脂蛋白水平,减少了肝脏和脂肪组织中的脂质积累,并缓解了肝脏脂肪变性。
TMPs还表现出对脂肪代谢的积极调节作用,包括增强棕色脂肪组织 (BAT) 的功能和促进腹股沟白色脂肪组织 (iWAT) 向米色脂肪转化。组织学分析显示,TMPs干预组中多室米色脂肪细胞增多,产热相关基因 (如UCP1、PRDM16、PGC-1α和CEBP/β) 的mRNA和蛋白表达均显著上升,表明TMPs可能通过激活产热和棕色化过程增强能量消耗,从而对抗肥胖及相关代谢异常。
本实验结果提示了TMPs作为一种肥胖调节饮食干预的潜力,并为进一步研究其具体的分子途径提供了基础。然而,需要进一步的研究,特别强调临床试验,以加强TMPs与肥胖之间的联系,并确定调节人类这些代谢反应所需的最佳剂量。
原文出自 Nutrients 期刊:https://www.mdpi.com/2072-6643/16/19/3330
Nutrients 期刊介绍
主编:
Lluis Serra-Majem, University of Las Palmas de Gran Canaria, Spain; Maria Luz Fernandez, University of Connecticut, USA
期刊主题涵盖常量营养素、微量营养素、生物活性营养素、运动营养、公共卫生和饮食相关疾病等学科领域。
2024 Impact Factor:5.0
2024 CiteScore:9.1
Time to First Decision:12.9 Days
Acceptance to Publication:2.3 Days


https://blog.sciencenet.cn/blog-3516770-1514428.html
上一篇:Healthcare:论文选题灵感——人工智能在医疗健康中的应用与评估
下一篇:Journal of Xenobiotics 微生物联手植物:破解金属胁迫的生物修复新维度