博文
代谢学人——Cell Metabolism:谁动了我的甘氨酸?
||
代谢学人
Cell Metabolism:雪旺招兵买马,"脂"为拯救细胞
撰文 | 郑宇含 张婷 仲银召 张彦康 李雨
编辑 | 孟美瑶
校对 | 张彦康

背景介绍
代谢功能障碍相关脂肪性肝病(MASLD,以前称为非酒精性脂肪肝NAFLD)是全球肝病的主要病因,发病人数持续上升。肝脂肪变性是MASLD的标志性特征,虽然在早期是可逆的,但仍有可能发展为更严重的代谢功能障碍相关脂肪肝炎(MASH)。此外,MASLD也是肝功能衰竭的主要原因。有研究表明,MASLD发病和恶化的关键是代谢变化,其中脂肪酸和碳水化合物代谢途径的变化是MASLD的经典代谢变化途径。除此之外,氨基酸代谢也逐渐成为MASLD发病机制中的新特征。据报道,在临床前模型和MASLD患者血液循环和肝脏中均发现了特定氨基酸的水平变化。例如,血浆中较低的甘氨酸水平可能与MASLD、心脏代谢性疾病和代谢综合症有关。此前在临床前模型中也已经证明甘氨酸治疗能有效改善代谢。然而,有关MASLD中甘氨酸水平下降的机制仍不清楚。
肝脏是药物代谢的主要场所。在MASLD早期可逆阶段通常没有明显的临床症状,但肝脏的代谢变化可能会影响药物毒性。在本篇研究中,研究人员结合了MASLD和药物肝毒性模型,利用稳定同位素示踪等方法,阐明了肝脂肪变性时甘氨酸在线粒体中转化为丝氨酸的途径增强,从而使血浆和肝脏中甘氨酸水平降低。此外,研究人员探究了有限的甘氨酸供应对肝脏中谷胱甘肽(GSH)生物合成和对乙酰氨基酚(APAP)敏感性的影响。最终,研究人员发现甘氨酸治疗或遗传手段敲除肝细胞中SHMT2可以有效改善APAP对MASLD的肝毒性。

敲黑板啦!
1.MASLD早期阶段肝脏中一碳代谢发生变化;
2.脂肪肝中甘氨酸水平下降促进肝脏氧化应激,并提高肝脏对APAP毒性敏感;
3.肝细胞SHMT2催化甘氨酸合成丝氨酸,是脂肪肝中甘氨酸下降的主要原因;
4.通过饮食或遗传干预可提高肝脏中甘氨酸水平,并缓解APAP诱导的肝脏损伤。
研究结果
1.脂肪肝中一碳代谢发生变化
为了探究MASLD早期的基础代谢变化,研究人员分析了MASLD早期仅出现脂肪变性时的肝脏代谢组。首先,研究人员用高脂肪、高蔗糖饮食(WD)或标准饮食(CD)喂养小鼠10周,发现与CD小鼠相比,WD小鼠体重和肝重均显著增加,且血浆丙氨酸转氨酶 (ALT)、天冬氨酸转氨酶 (AST)、乳酸脱氢酶 (LDH) 和胆固醇水平均升高(图1A-B,S1A-S1D)。此外,WD小鼠肝脏体积明显增大,呈黄色,且肝脏中脂质积累水平升高,肝脏甘油三酯和胆固醇含量增加(图1C-D,S1E-S1F),这表明WD小鼠发生了肝脏脂肪变性。接下来,研究人员对WD和CD小鼠肝脏和血浆进行非靶向代谢组分析,鉴定出324种肝脏代谢物和260种血浆代谢物。与CD小鼠相比,WD小鼠肝脏中有107种肝脏代谢物和88种血浆代谢物发生了显著变化,其中肝脏和血浆中许多甲基化代谢物显著降低(图1E-H)。并且通路富集分析显示WD小鼠肝脏和血浆中发生显著改变的代谢物主要富集在丝氨酸和甘氨酸代谢途径以及甲基化循环(即蛋氨酸代谢和甜菜碱代谢)中(图1I-J)。
参考文献: [1]Yang M, et al. Nat Rev Cancer,2016,16(10),650-662. [2]Ducker GS, et al. Cell Metab.2017,25(1),27-42.拓展阅读:一碳代谢一碳单位是指只含一个碳原子的有机基团,有关一碳单位生成和转移的代谢称为一碳单位代谢。一碳单位包括甲基、甲烯基、甲炔基、甲酰基及亚氨甲基等,分别来自甘氨酸、组氨酸、丝氨酸、色氨酸、蛋氨酸等,其中丝氨酸是主要来源。 一碳单位不能游离存在,通常与四氢叶酸(Tetrahydrofolic acid,FH4)的N5、N10位结合进行转运或参加生物代谢,其中FH4是一碳单位代谢的辅酶。如丝氨酸可在丝氨酸羟甲基转移酶(Serine hydroxymethyltransferase,SHMT)作用下将一个碳单位转移到四氢叶酸上,产生甘氨酸和N5,N10-CH2-四氢叶酸,进而为细胞提供一碳单位。色氨酸分解代谢能产生甲酸,甲酸可与FH4结合产生N10-CHO-FH4。蛋氨酸分子中的甲基也是一碳单位,在ATP的参与下蛋氨酸生成S-腺苷蛋氨酸(Sadenosylmethionine),其是活泼的甲基供体。 一碳单位功能众多,其是合成嘌呤和嘧啶的原料,在核酸生物合成中发挥重要作用;此外,S-腺苷蛋氨酸可提供甲基参与体内多种物质合成,比如肾上腺素、胆碱、胆酸等。
调节甲基化过程的主要途径之一是叶酸或其他甲基载体(如三甲基甘氨酸,即甜菜碱)中的一碳单位转移到不同的底物上。而肝脏是一碳代谢的主要场所,且已有研究表明MASLD小鼠肝脏的脂质甲基化发生了改变。据报道,丝氨酸羟甲酰转移酶(SHMT)催化的途径是一碳代谢的关键反应,即SHMT负责催化丝氨酸与甘氨酸的相互转化,并伴随着甲基向四氢叶酸的转移/转出,这一过程分别由SHMT1和SHMT2催化,发生在胞质和线粒体中。此外,在肝脏中,甘氨酸可作为甲基供体,产生甲基四氢叶酸和CO2;还可在甘氨酸-N-甲基转移酶(GNMT)的催化下,作为甲基受体,产生单甲基甘氨酸(肌氨酸)。有研究表明GNMT基因的缺失会促使小鼠肝脏脂肪变性。事实上,与CD小鼠相比,WD小鼠肝脏中甘氨酸、肌氨酸和甜菜碱水平显著下降(图1G-H)。且与先前研究结果一致,在MASLD早期阶段,小鼠肝脏和血浆中甘氨酸水平也显著下降(图1K-L)。为了确定甘氨酸的减少是由肝脏脂肪变性而非特殊饮食引起的,研究人员采用高果糖、高脂肪饮食(HFHFD)喂养小鼠,发现与CD小鼠相比,HFHFD小鼠体重增加,血浆ALT水平升高,肝脏甘油三酯水平增加并导致轻度肝脏脂肪变性,同时血浆甘氨酸显著减少(图S1G-S1K)。总之,基于肝脏和血浆非靶向代谢组学以及两种饮食小鼠模型的研究结果表明,在MASLD早期阶段,小鼠肝脏和血浆中甘氨酸水平下降。
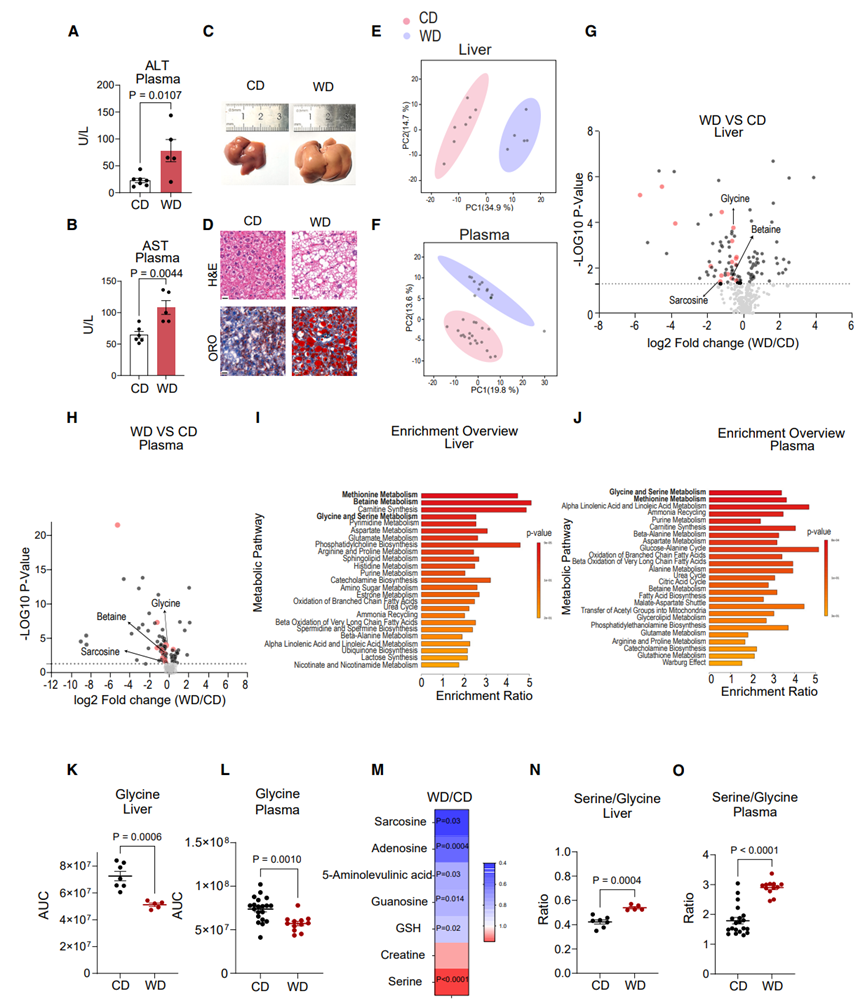
图1.MASLD小鼠肝脏中一碳代谢下调
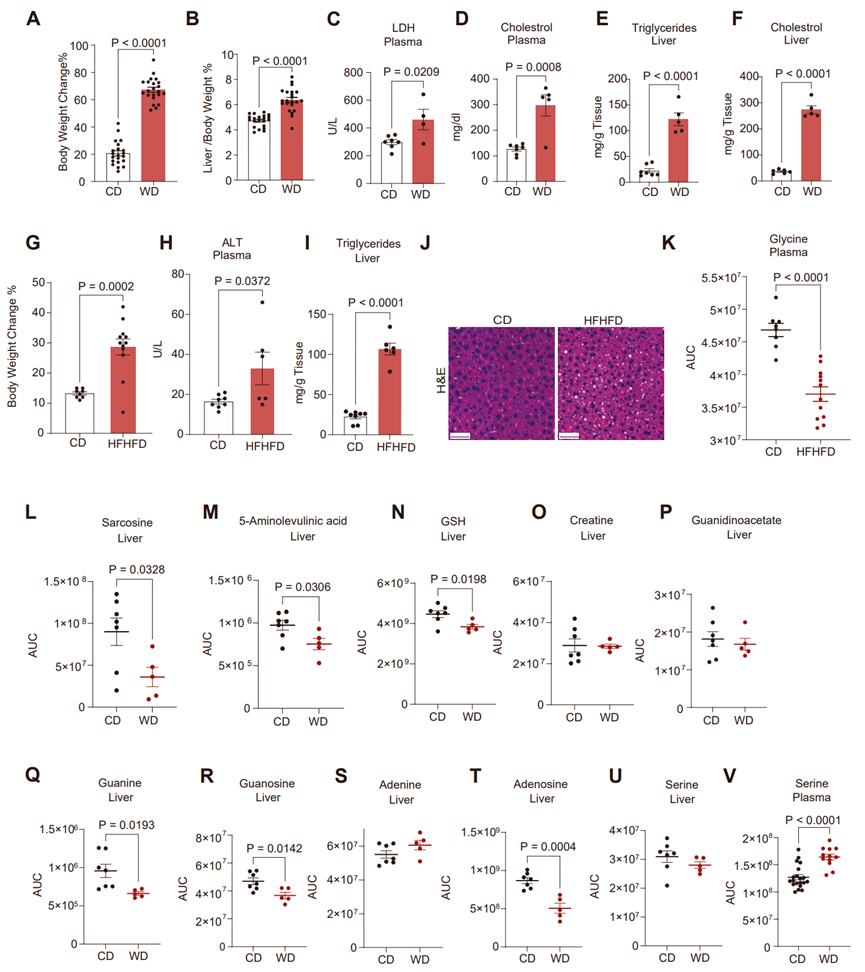
图S1. MASLD早期阶段肝脏的代谢组学分析
2.丝氨酸合成增加导致脂肪肝中甘氨酸水平下降
为了探究MASLD小鼠肝脏和血浆中甘氨酸水平下降的潜在代谢机制,研究人员首先检测了甘氨酸的下游产物,发现WD小鼠肝脏中大多数甘氨酸衍生代谢物水平下降(图1M,S1L-S1T),这可能是由于甘氨酸的供应减少。然而,与CD小鼠相比,WD小鼠肝脏丝氨酸水平没有明显变化,血浆丝氨酸水平显著升高,使得WD小鼠肝脏和血浆中丝氨酸/甘氨酸比例升高(图1N-O,S1U-S1V)。这表明,MASLD小鼠肝脏和血浆甘氨酸水平的下降可能是转化为了丝氨酸。为了验证这一结论,研究人员利用13C2标记甘氨酸对CD小鼠和WD小鼠进行稳定同位素示踪,注射13C2标记甘氨酸显著提高了CD和WD小鼠血浆和肝脏中甘氨酸水平,尽管WD小鼠肝脏甘氨酸水平仍低于CD小鼠(图2A-C),同位素示踪结果显示CD和WD小鼠肝脏和血浆中一大部分丝氨酸是由甘氨酸转化而来,且其中一部分丝氨酸的三个碳原子均带有13C2标记(M+3),这表明甘氨酸可能通过SHMT催化和线粒体甘氨酸裂解系统这两条途径转化为丝氨酸(图2D-F)。并且,与CD小鼠相比,WD小鼠中甘氨酸向丝氨酸的转化速率更高,但甘氨酸下游其他代谢物的13C2标记水平并无明显变化(图2G,S2A-S2J)。随后,为了验证甘氨酸转化为丝氨酸是否是MASLD小鼠肝脏和血浆甘氨酸水平下降的原因,研究人员利用泛SHMT抑制剂SHIN1处理WD小鼠,SHIN1可同时靶向抑制SHMT1和SHMT2的酶活性,结果发现SHIN1治疗抑制了甘氨酸向丝氨酸的转化,并显著降低了WD小鼠肝脏和血浆中丝氨酸水平,同时提高了甘氨酸水平(图2H-2K)。由于肾脏是丝氨酸生物合成的主要器官,研究人员检测了WD小鼠肾脏中甘氨酸水平,结果显示SHIN1治疗并不影响肾脏甘氨酸水平(图S2K-S2M)。总之,这些结果表明MASLD小鼠甘氨酸水平下降是由于肝脏SHMT促进了甘氨酸转化为丝氨酸。接下来,研究人员想要探究甘氨酸转化为丝氨酸后的去向。丝氨酸与棕榈酰CoA缩合形成鞘氨醇是鞘磷脂代谢的第一步(图S3A)。众所周知,脂肪肝中会积累鞘磷脂。与CD小鼠相比,WD小鼠肝脏中鞘氨醇水平显著升高,且含有13C2标记的鞘氨醇水平也显著升高(图S3B-S3C)。而抑制SHMT活性可显著降低含13C2标记的鞘氨醇水平(图S3D)。总之,这些结果表明WD小鼠肝脏中甘氨酸转化为丝氨酸,可促进鞘磷脂的合成。接下来,为了探究脂肪肝中甘氨酸水平的下降是否是肝细胞代谢变化的直接结果,且SHMT2是否参与其中,研究人员利用CRISPR-Cas9方法和Cre-lox系统构建了肝细胞特异性缺失SHMT2的小鼠(Shmt2HKO)(图2L,S3E-S3F)。结果发现,在WD喂养的Shmtfl/fl小鼠和Shmt2HKO小鼠体重和肝重没有明显差异的情况下,Shmt2HKO小鼠血浆甘氨酸水平显著上调(图2M)。总之,这些结果表明,在WD小鼠肝脏中,肝细胞SHMT2介导了甘氨酸的利用。
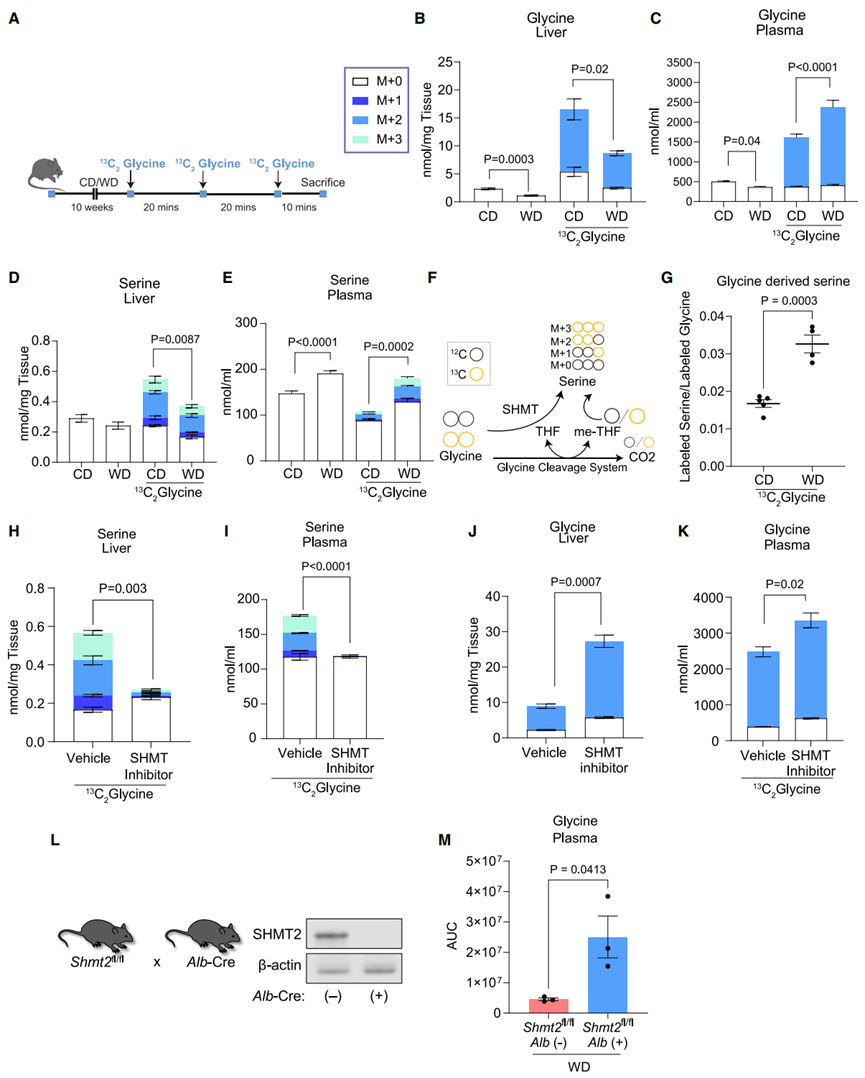
图2. 丝氨酸合成增加导致脂肪肝中甘氨酸水平下降
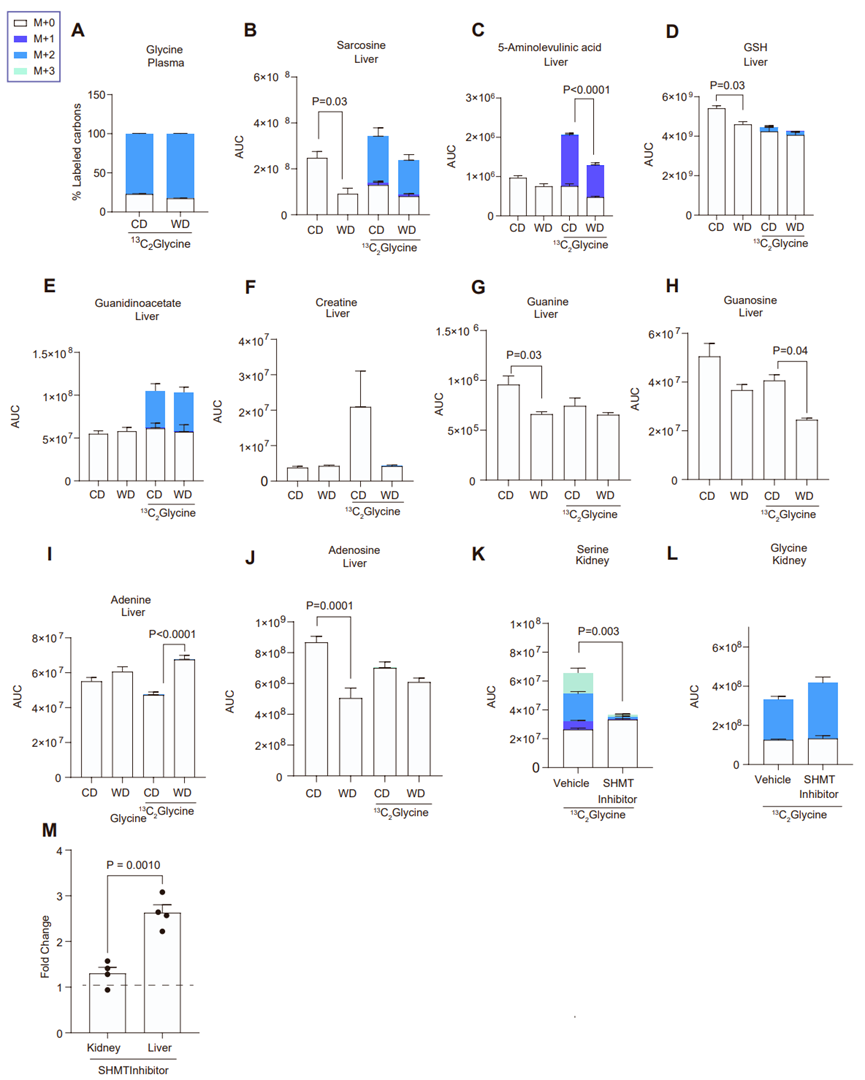
图S2. MASLD小鼠的甘氨酸示踪实验
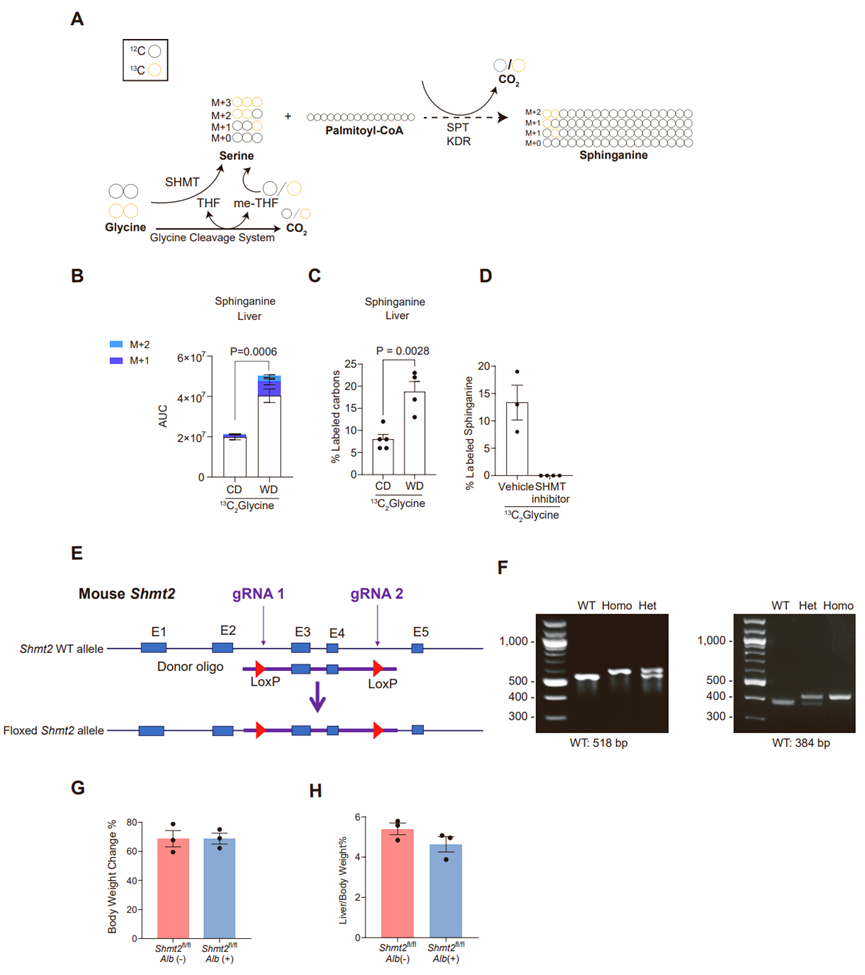
图S3.鞘氨醇来自于甘氨酸以及构建肝细胞特异性敲除Shmt2的小鼠
3.脂肪肝中甘氨酸水平下降促使肝脏对外源物质引起的氧化应激更加敏感
代谢性疾病中甘氨酸水平下降会导致谷胱甘肽(GSH)合成受损,GSH是细胞内一种主要的抗氧化剂,由谷氨酸、半胱氨酸和甘氨酸合成(图S4A)。非靶向代谢组学显示与CD小鼠相比,WD小鼠肝脏中GSH水平下降,同时甘氨酸水平降低(图1L,S1N),而谷氨酸和半胱氨酸水平无明显差异(图S4B-S4C),且GSH中13C2标记水平也较低(图S2D),这表明与丝氨酸合成相比,甘氨酸转化为GSH的速率较慢。据报道,棕榈酸(PA,饱和脂肪酸)负荷会诱发细胞脂毒性,主要表现为氧化应激和内质网应激,这被认为是MASLD的主要诱因,而油酸(OA,单不饱和脂肪酸)能抑制脂毒性(小编注:现下文章中一般用饱和或不饱和脂肪酸等诱导肝细胞构建NAFLD细胞模型。棕榈酸(PA)是饮食和血清中最丰富的饱和脂肪酸,而油酸(oleic acid,OA)是最丰富的不饱和脂肪酸,将PA和/或OA加入肝细胞中,诱导肝细胞内的脂质沉积,以此得到的 NAFLD 模型已被国内外研究广泛应用。但部分文献已报道,PA可呈剂量依赖性降低细胞活力,而OA对PA诱导的细胞毒性具有保护作用,所以联合诱导(OA+PA(2:1))效果更佳)。于是,为了研究脂质积累对肝细胞中甘氨酸和GSH代谢的影响,研究人员利用PA或OA处理永生化的小鼠肝细胞系AML12,处理24h后肝细胞中会积累脂滴(图S4D),这是肝脏脂肪变性的表现。与体内结果一致,PA处理显著降低了AML12细胞中甘氨酸和GSH的水平,并促进AML12细胞氧化应激,而OA对AML12细胞无明显影响(图3A-C)。据报道,肝脏GSH在中和外源物质的过程中起着关键作用,因此肝脏GSH水平下降可能对药物代谢及其毒性产生有害的影响。对乙酰氨基酚(APAP)是一种常用的处方药,广泛用于镇痛和解热。然而,过量摄入APAP会引起急性肝衰竭。在安全剂量下,APAP会在肝脏中转化为无毒化合物,其中一小部分药物代谢产生活性自由基,即N-乙酰对苯醌亚胺(NAPQI),然后被GSH中和(图3D)。随后,研究人员用APAP处理AML12细胞12h,发现APAP处理显著提高了AML12细胞中超氧化物水平,且PA与APAP联合处理进一步促进了AML12的超氧化物水平,而甘氨酸或GSH处理显著降低了PA和APAP诱导的超氧化物水平(图3E-3F),这表明甘氨酸在缓解APAP诱导的氧化应激中发挥重要作用。流行病学调查表明,MASLD患者发生APAP毒性的风险更高,但在临床前研究中尚无此定论。因此研究人员想要探究WD小鼠(肝脂肪变性且肝脏GSH较低)是否更容易发生APAP毒性。首先,研究人员用300-600mg/kg的给药剂量处理CD小鼠,这个剂量相当于人类单次最大剂量的2-4倍,结果显示CD小鼠血浆中APAP水平及其下游主要代谢物(APAP与硫酸和葡糖苷酸的偶联物)水平显著升高,且呈剂量依赖性(图3D,S5A-S5C)。然而,与谷胱甘肽结合的NAPQI分解代谢产物,即APAP-半胱氨酸和APAP-巯基,在300mg/kg处理时即到达最大值(图S5D-S5E)(小编注:这里检测的是与GSH结合的NAPQI分解代谢产物,在300mg/kg APAP处理CD小鼠时到达最大值,表明此时GSH已经全部与NAPQI分解代谢产物结合,即体内GSH已被耗尽)。据报道,APAP代谢主要发生在表达细胞色素p450酶CYP2E1的肝脏中央静脉周围细胞(第3区)。组织学分析表明,在给药24h后,不同剂量APAP均引起了第3区细胞坏死,但450mg/kg APAP和600mg/kg APAP处理引起了第3区以外的区域更广泛的损伤(气球样变性)(图S5F)。此外,450mg/kg APAP和600mg/kg APAP处理时CD小鼠均出现了痛苦迹象(数据未展示),而300mg/kg APAP处理时,9只CD小鼠中只有1只出现了痛苦迹象(图S5G)。因此,研究人员选择了300mg/kg的APAP给药剂量进行后续研究。接下来,为了探究APAP对脂肪肝的毒性影响,研究人员给WD和CD小鼠单次注射300mg/kg APAP,结果显示APAP处理24h后,与CD小鼠相比,WD小鼠血浆ALT和AST水平显著升高,且WD小鼠肝脏有明显出血(图4A-D),组织学分析进一步确定APAP处理后WD小鼠肝脏的第3区出血(图4E-F),并且WD小鼠均出现了明显的痛苦迹象(图S5G)。动力学研究显示,APAP处理3h后,CD和WD小鼠肝脏中GSH均耗尽,且WD小鼠肝脏GSH含量恢复能力显著低于CD小鼠(图4G),同时WD小鼠肝脏中GSSG/GSH水平(氧化型谷胱甘肽与还原型谷胱甘肽的比值)显著升高,血红素加氧酶1(Hmox1)和NAD(P)H醌脱氢酶1(Nqo1)的基因表达水平也显著上调(图4H-4I),表明APAP处理显著诱导了WD小鼠肝脏的氧化应激。为了研究WD小鼠肝脏对APAP毒性的敏感性增加是由肝脏脂肪变性直接引起的,而不是由CD和WD饲料成分差异造成的,研究人员对比了WD小鼠和低脂低糖(LFD)小鼠,WD和LFD饲料在成分组成方面是类似的,结果发现与LFD小鼠相比,WD小鼠的体重、肝重、血浆ALT和AST水平显著升高,肝脏表现出明显的脂质积累现象(图S5H-S5L)。APAP处理后,WD小鼠血浆ALT和AST水平显著高于LFD小鼠,且WD小鼠肝脏有明显出血(图S5M-S5O)。总之,这些结果表明,肝脏脂肪变性(而非营养成分)显著促进了肝脏对APAP毒性的敏感性。
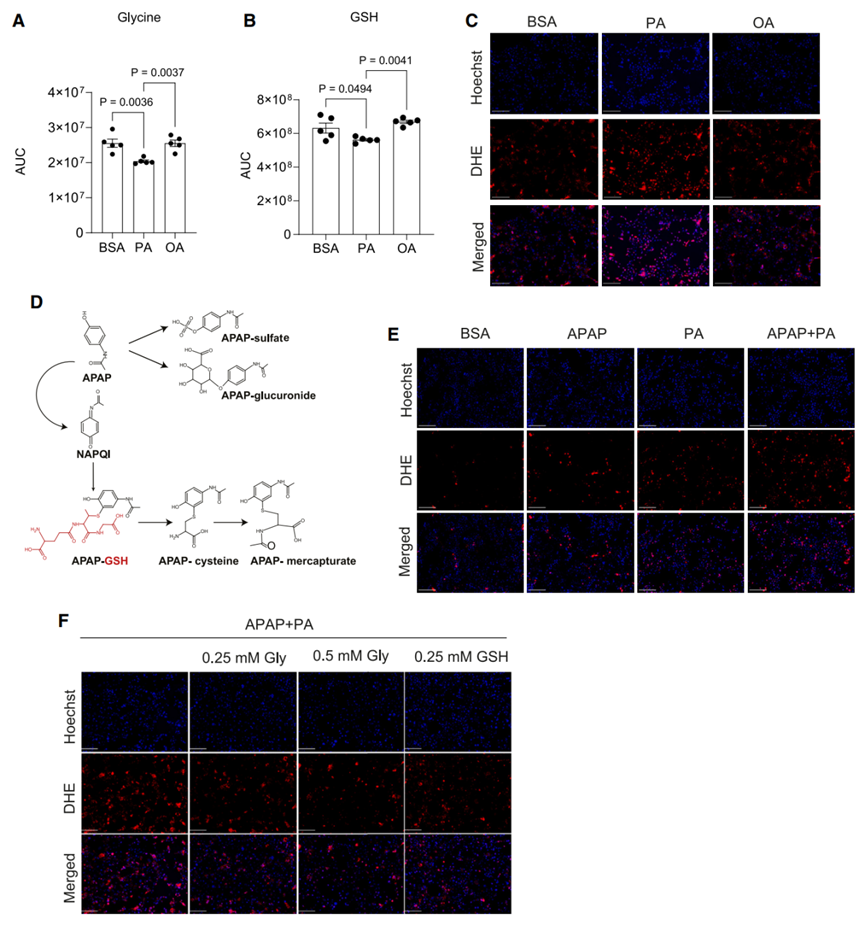
图3.肝脏脂质积累降低肝细胞内甘氨酸和GSH水平,并促进肝细胞对APAP毒性的敏感性
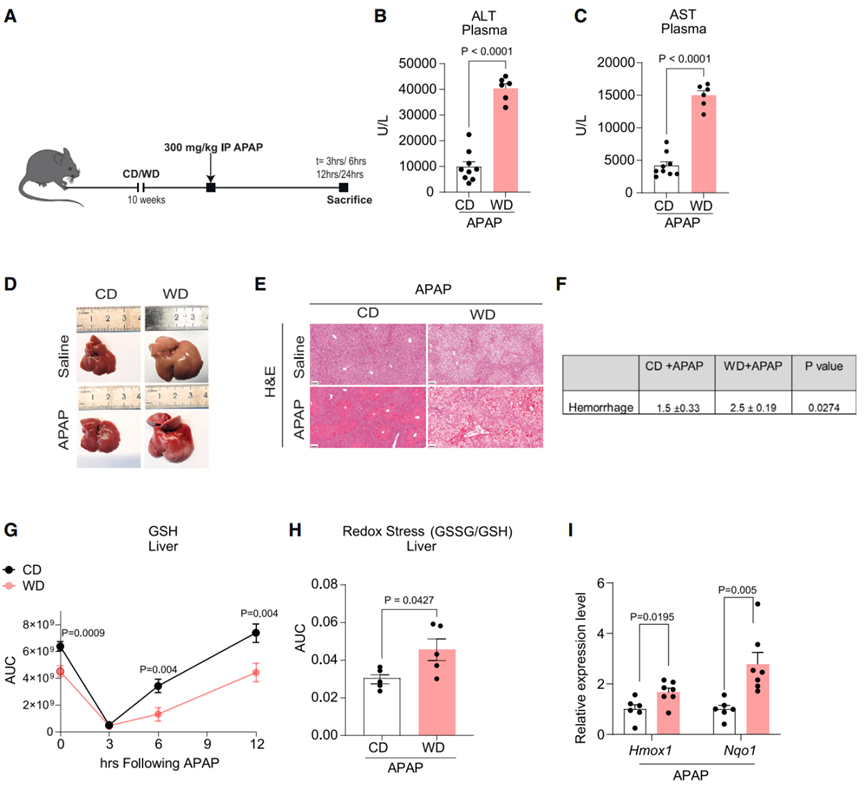
图4. MASLD小鼠肝脏恢复GSH能力下降,氧化应激增加,并伴随肝脏损伤
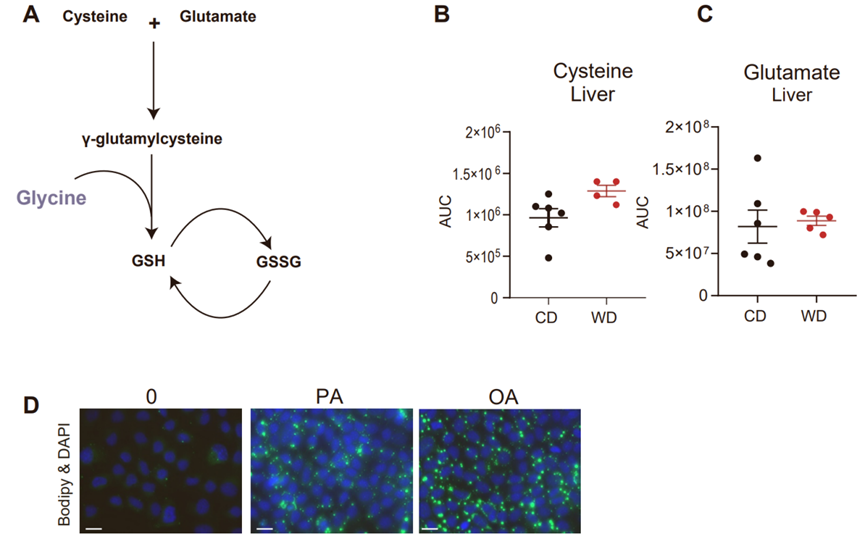
图S4. 肝脏脂质积累降低甘氨酸水平,进而抑制GSH合成
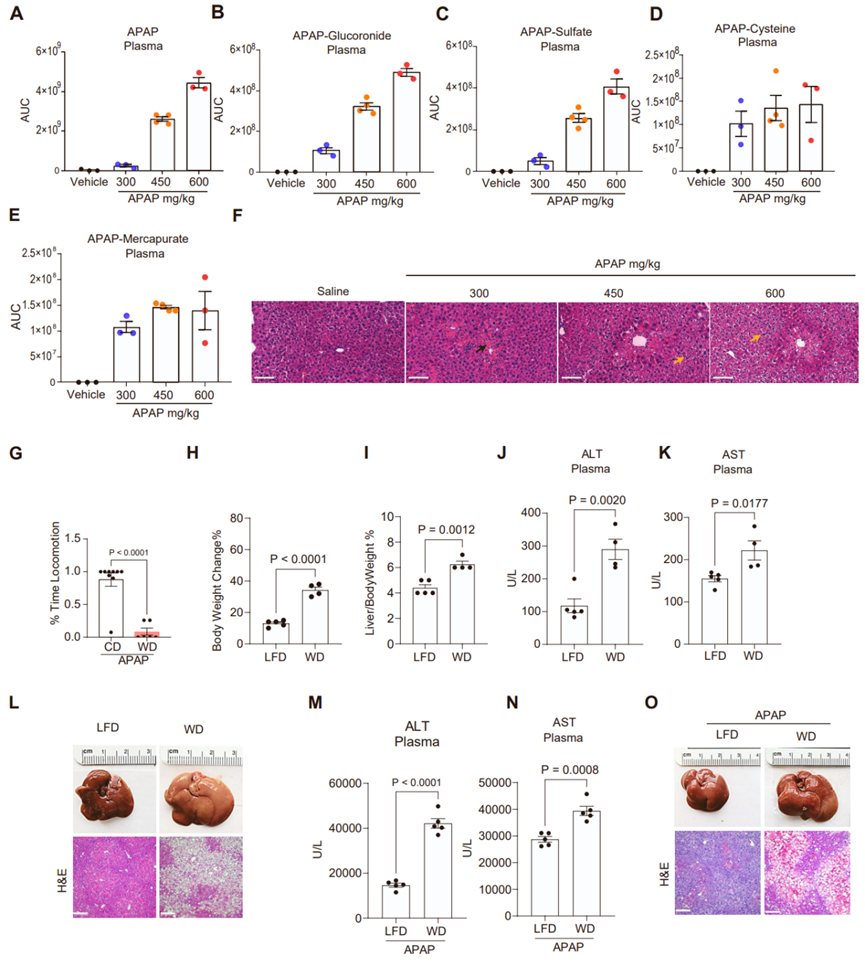
图S5. LFD和WD小鼠肝脏的APAP代谢和毒性研究
4.甘氨酸治疗可提高肝脏GSH水平,并缓解APAP诱导的肝脏损伤
由于甘氨酸水平下降会促进肝脏对APAP毒性的敏感性,于是研究人员想要确定甘氨酸治疗是否能缓解APAP对脂肪肝的毒性影响。研究人员在APAP处理后立刻用1g/kg甘氨酸灌胃治疗WD小鼠,并在GSH水平耗竭时(APAP处理后3h)再次用甘氨酸治疗(图4G,5A)。结果表明,甘氨酸治疗可显著提高WD小鼠肝脏甘氨酸水平和GSH水平(图5B-C)。并且,研究人员用13C2标记的甘氨酸治疗WD小鼠,发现甘氨酸治疗6h后WD小鼠肝脏中含13C2标记的GSH水平显著升高(图 5D),表明甘氨酸参与脂肪肝中GSH的合成。此外,甘氨酸治疗后WD小鼠肝脏中GSSG/GSH水平显著下降,GSH与4-羟基壬烯醛(4-HNE,脂质过氧化产物)结合水平降低,且组蛋白H2A磷酸化(γ-H2A.X,表征DNA双链断裂损伤)水平也显著下降(图5E-5G)。此外,甘氨酸治疗显著缓解了WD小鼠的肝损伤水平,这一效果与N-乙酰半胱氨酸(NAC)的治疗效果相当(图5H-I,S6A-S6B)。NAC是治疗由过量APAP引起的肝损伤的标准药物,主要通过补充半胱氨酸以促进GSH的合成。值得注意的是,等量的D-丙氨酸(不参与GSH的合成途径或其他主要代谢途径)治疗并不影响APAP诱导的WD小鼠肝脏损伤水平(图S6A-S6B)。与这些结果一致的是,甘氨酸治疗还显著缓解了APAP诱导的WD小鼠肝脏出血和细胞坏死现象,并减轻了APAP处理时WD小鼠的痛苦迹象(图5J-5M)。总之,这些结果表明,甘氨酸治疗可减轻APAP诱导的MASLD小鼠肝脏损伤现象。
有趣的是,甘氨酸转化为丝氨酸后,还可通过转硫途径与同型半胱氨酸结合形成半胱氨酸,进而转化为GSH(小编注:此处作者进行了甘氨酸补充,在此条件下,丝氨酸可通过转硫途径与同型半胱氨酸结合形成半胱氨酸,进而转化为GSH。机体甘氨酸代谢去路和其本身丰度有关系。在低甘氨酸水平下,其合成的丝氨酸去路是本文开头提到的鞘磷脂,而在高甘氨酸水平下,其合成的丝氨酸去路包括谷胱甘肽通路)。事实上,甘氨酸治疗显著提高了WD小鼠肝脏中同型半胱氨酸和半胱氨酸水平(图S6C-S6E)。
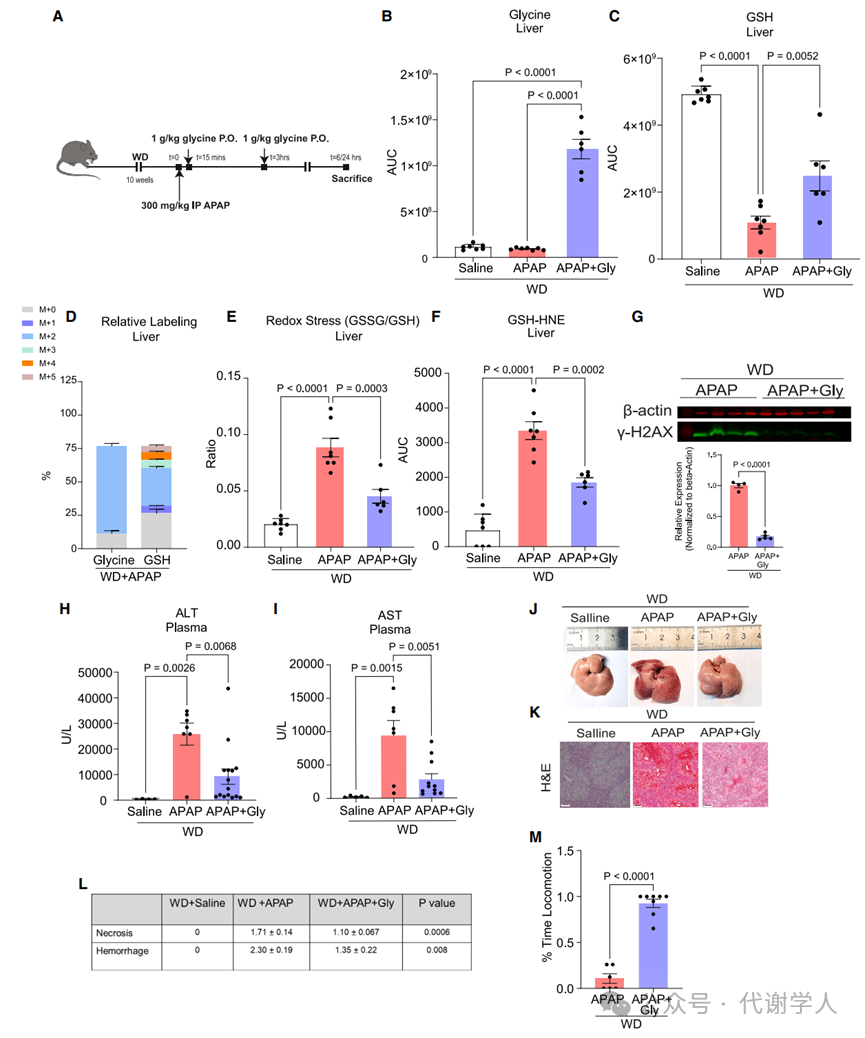
图5. 甘氨酸治疗可提高肝脏GSH水平,并缓解APAP诱导的肝脏损伤
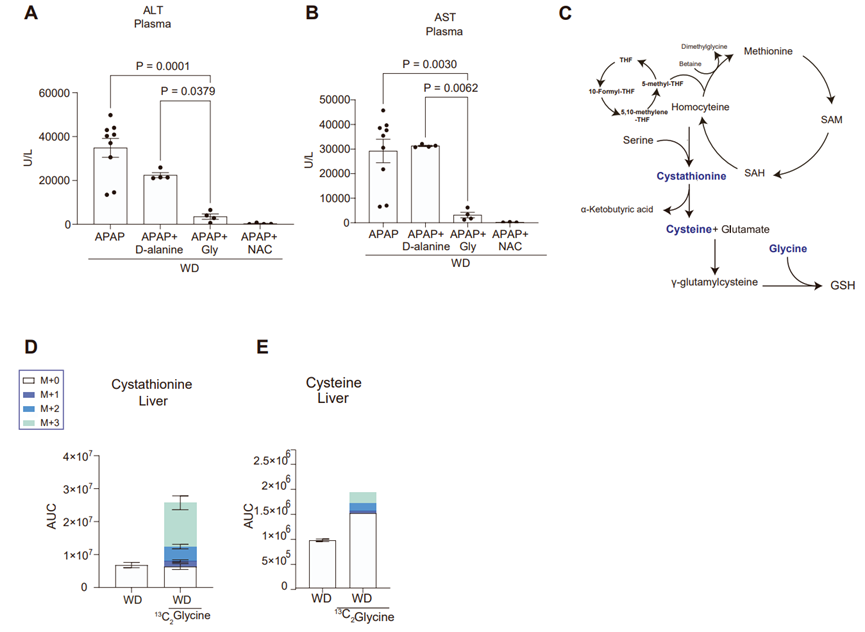
图S6. 甘氨酸治疗缓解APAP诱导的肝脏损伤,以及转硫途径
5.肝细胞特异性敲除SHMT2可提高脂肪肝中甘氨酸和GSH水平,并缓解APAP引起的肝脏损伤
鉴于脂肪肝中甘氨酸水平的下降是由肝细胞SHMT2催化甘氨酸转化为丝氨酸所驱动的,于是研究人员试图确定肝细胞SHMT2的缺失能否改善APAP引起的肝损伤现象。研究人员给Shmt2fl/fl和Shmt2HKO小鼠饲喂WD饮食10周,随后注射APAP(图6A)。结果发现,与Shmt2fl/fl小鼠相比,Shmt2HKO小鼠肝脏中甘氨酸和GSH水平显著升高,且氧化应激水平和DNA损伤水平显著下降(图6B-6E)。此外,与Shmt2fl/fl小鼠相比,Shmt2HKO小鼠血浆ALT水平也显著下降,肝脏出血现象和细胞坏死程度明显改善,小鼠的痛苦迹象减轻(图6F-6I)。总之,这些结果表明,肝细胞SHMT2的缺失可提高甘氨酸水平,进而促进GSH的合成,缓解MASLD中APAP诱导的肝脏损伤现象。
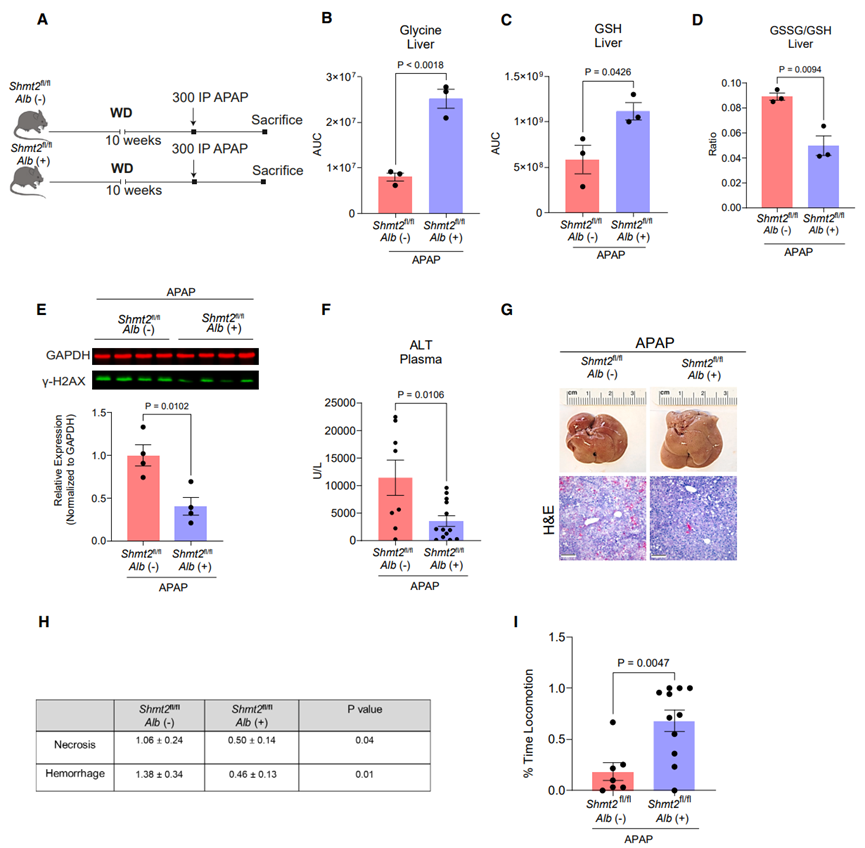
图6. 肝细胞特异性敲除SHMT2可以缓解APAP诱导的肝脏损伤
总结
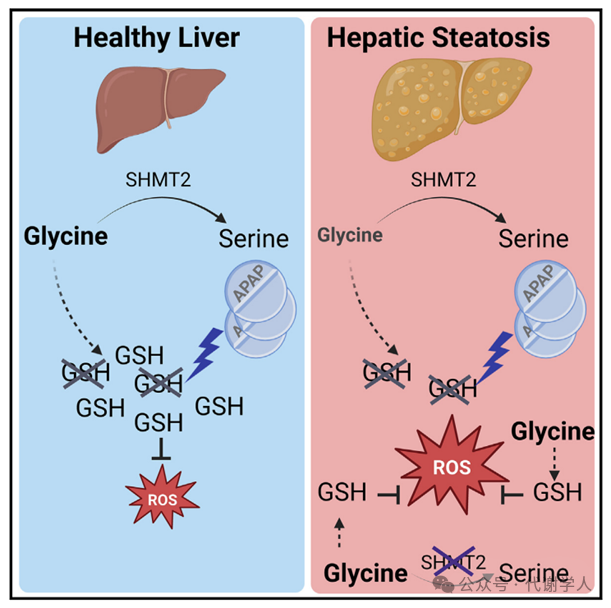
本文中,研究人员首先通过肝脏和血浆的非靶向代谢组学分析发现,MASLD早期阶段的小鼠肝脏中甲基化代谢物水平下降,表明在肝脏脂肪变性阶段,肝脏的一碳代谢发生了改变,并且甘氨酸(一碳代谢的核心成分)水平显著下降。稳定同位素示踪实验表明,SHMT催化甘氨酸转化为丝氨酸,是脂肪肝中甘氨酸水平下降的主要原因。此外,脂肪肝中甘氨酸水平的下降导致肝脏对APAP毒性更加敏感,进一步研究发现甘氨酸水平的下降会抑制GSH的合成,从而促进APAP诱导的肝脏氧化应激损伤,产生严重的肝脏毒性。而甘氨酸治疗或肝细胞特异性敲除SHMT2可提高肝脏甘氨酸水平,促进GSH的合成,进而缓解APAP引起的肝脏损伤。总之,本篇研究揭示了MASLD早期阶段肝脏代谢变化引起甘氨酸水平下降,促使MASLD小鼠对药物毒性更加敏感。
原文链接:https://www.cell.com/cell-metabolism/fulltext/S1550-4131(23)00464-3
https://blog.sciencenet.cn/blog-3483272-1419293.html
上一篇:Neuron: Irisin让你不再困在时间里
下一篇:代谢学人--NCB: “热辣滚烫”的秘密:唤醒脂肪EPAC1