博文
既有石蜡切片,为什么还要做冰冻切片免疫荧光?_ MCE 中国
|
Section.01
石蜡切片 VS 冰冻切片
有何区别?
组织样本的免疫荧光主要有两种制备方式:石蜡切片和冰冻切片。两者各有优劣,适用场景也大不相同。
石蜡切片免疫荧光 (Paraffin section) 虽在组织形态保存和长期储存方面具有优势,但其制备过程涉及高温烘烤、二甲苯脱蜡等步骤[1][2],容易导致某些敏感蛋白 (如细胞表面受体、细胞因子、磷酸化蛋白等) 的抗原表位被破坏或掩蔽,使得抗体“认不出”目标蛋白,造成假阴性。此外,石蜡切片的制备周期较长,不适用于医学病理检测等场景。
相比之下,冰冻切片免疫荧光 (Frozen section immunofluorescence) 直接将新鲜或快速冷冻的组织置于低温环境下进行切片。这一过程极大地缩短了制片时间,同时保留了组织中的多种抗原免疫活性。免疫荧光技术则进一步利用荧光标记的抗体与组织中的特定抗原结合,通过荧光显微镜观察,实现对抗原的精确定位和可视化[3]。
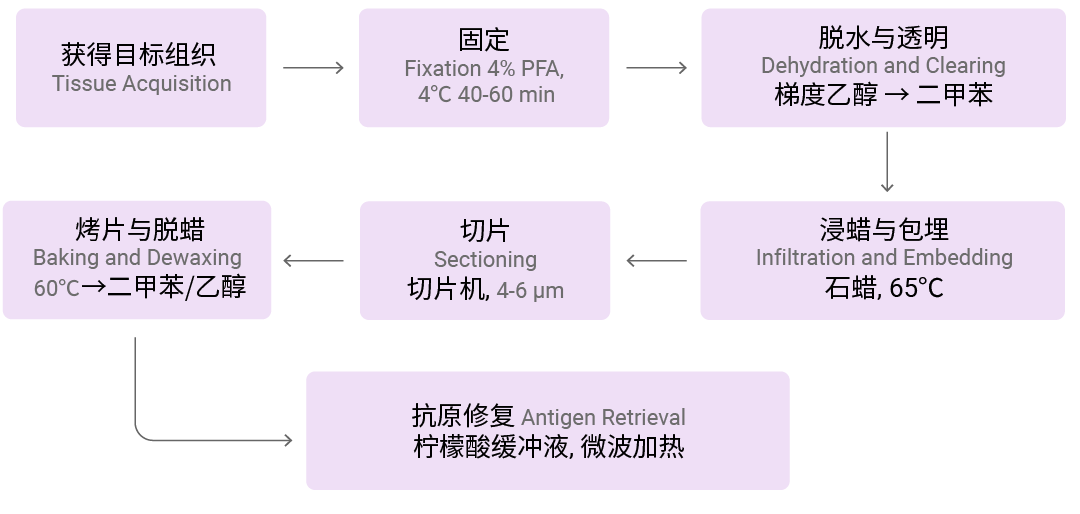
图 1. 石蜡切片 (上) 和冰冻切片 (下) 流程[2][4]。
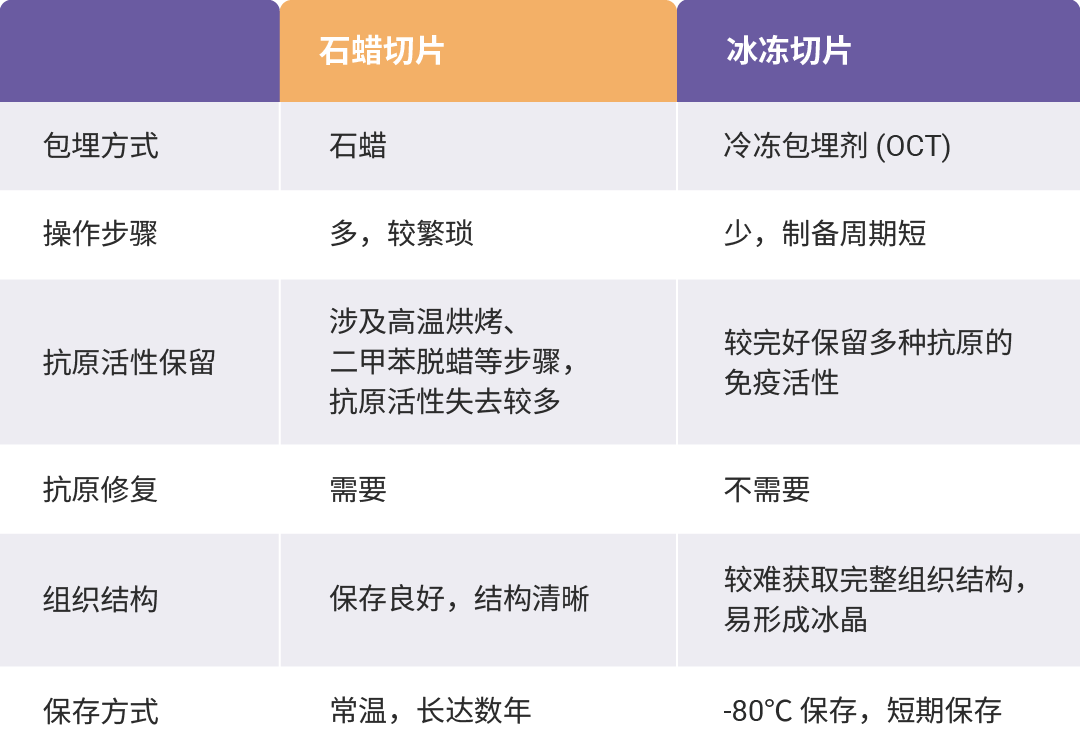
表 1. 石蜡切片、冰冻切片的区别[5]。
Section.02
为什么有些蛋白
“非冰冻不可”?
首先,当检测敏感蛋白/低表达抗原时,石蜡切片的高温、二甲苯脱蜡等步骤,会导致敏感蛋白抗原表位变性,让抗体无法识别。冰冻切片低温冷冻、不接触高温和有机溶剂,能保留抗原免疫活性,对细胞表面受体、磷酸化蛋白等敏感抗原的检测灵敏度远高于石蜡切片。此外,珍贵、难重复取材的组织样本也适合冰冻切片。
其次,在应急诊断/手术中快速诊断时,石蜡切片制备需 2-3 天,无法满足应急需求。冰冻切片 30 分钟内可完成包埋切片,1-2 小时完成染色,是手术切缘判断、急性病变诊断的首选,能为临床决策及时提供依据[1]。
此外,在进行多抗原共定位分析时——石蜡切片:不同抗原修复条件不一,易出现修复不均问题;冰冻切片:无需抗原修复,可同时孵育多种一抗,实现多通道荧光标记,清晰呈现多种抗原的空间分布关系。
Section.03
冰冻切片免疫荧光
怎么做?

图 2. OCT 包埋、冷冻切片以及显微镜下观察示意图[6]。
冰冻切片免疫荧光详细步骤[4][5]:
组织前处理
『取材与固定』
快速取出新鲜组织 (如小鼠脑、肝、肾等),用 1xPBS 冲洗去除血迹,浸没在 4% PFA,放在 4℃ 固定 12-24 小时。
『脱水』
随后将固定后的组织转移至 15% 蔗糖溶液 (4℃),待其完全沉底 (约数小时);转入 30% 蔗糖溶液 (4℃) ,继续孵育直至再次完全沉底 (一般过夜),目的是为了脱去水分;
『包埋与冷冻』
取出沉底的组织,用滤纸轻轻吸干表面多余水分。放入包埋模具中,用足量的 OCT 包埋剂完全覆盖组织,确保没有气泡。接着迅速放在干冰或液氮气相层进行速冻,直至形成白色硬块,取出后可立即放入 -80℃ 冰箱保存,或直接用于切片。
注意:
(1) 固定时间不宜过长,防止过度交联影响抗原暴露。
(2) 蔗糖溶液要用 PBS 配制,不推荐用水溶解。
(3) 若组织未完全沉底即进行冷冻,易因水分过多而产生冰晶空洞。
(4) 冷冻速度越快,形成的冰晶越小,组织结构保存越好。
切片与免疫染色
『切片』
提前将 OCT 包埋块放入冷冻切片机腔体 (温度 -20℃ 左右),平衡 30 分钟。
修整组织表面,设置切片厚度 (一般 5-10 μm)。转动切片机轮盘,辅以防卷板,连续平整切片并贴附在防脱载玻片上,置于室温晾干 30-60 分钟后储存于 -80℃ 或者直接进行下一步。
『封闭和穿孔』
将切片用 1xPBS 清洗 3 次,每次 5 min,目的是为了去除切片表面的 OTC,再甩去多余液体,在组织周围用疏水笔画圈,并向组织加入封闭液 (5% 正常山羊血清或 5% BSA+ 0.3% Triton X-100),室温孵育 1 h。
『一抗孵育』
吸去封闭液,立即在组织部分滴加合适比例的一抗,确保整个组织都覆盖。将载玻片放回湿润的盒子里,4℃ 冰箱过夜。接着取出后先放复温至室温,用 1xPBS 清洗 3 次,每次 5 min。
『二抗孵育』
再滴加荧光标记的二抗,室温避光孵育 1 h。用 1xPBS 清洗 3 次,每次 5 min。
『染核与封片』
尽量吸干玻片上残余的水分,在样品处滴加含有 DAPI 的抗荧光淬灭封片剂,盖上盖玻片进行封片,尽量排除气泡。室温通风晾干 2-4 小时,或 4℃ 避光保存过夜。
『观察和图像处理 』
使用荧光显微镜或共聚焦显微镜观察并拍照。图片可用 ImageJ 软件进行分析处理。
注意:
(1) 操作过程中应避免组织长时间处于干燥状态;
(2) 荧光染色过程需要避光。
Section.04
常见问题+
解决方案
Q1. 背景普遍较高,非特异性信号多
可能原因:封闭不充分;荧光二抗非特异性结合;组织样品干燥时间长
解决方案:延长封闭时间;二抗种属来源一致或使用;操作过程保持组织样品湿润。
Q2. 显微镜下视野中“黑洞”较多
可能原因:蔗糖脱水不彻底;冷冻速度太慢形成冰晶;封片时未排尽气泡
解决方案:确保 30% 蔗糖完全沉底;包埋时用液氮/干冰速冻;封片确保气泡全部去除。
Q3. 组织容易脱落载玻片
可能原因:载玻片材料不合适;切片未在室温下复温就染色。
解决方案:选用Superfrost Plus 防脱载玻片;室温下复温 30 min 左右。
其实!石蜡切片和冰冻切片,从来不是“对立关系”,而是“互补关系”——
(1) 如需做常规病理、长期存档、不敏感抗原检测,选石蜡切片,省心又稳定;
(2) 如需做敏感抗原、低表达抗原、术中快速诊断,选冰冻切片,精准又高效。
冰冻切片免疫荧光的核心优势是“保留抗原活性”,这是石蜡切片无论如何优化都难以替代的。虽说冰冻切片步骤略多,但只要掌握正确方法,避开常见坑,就可获得实验顺利!
产品推荐
Tissue and Cell Fixative (4% Paraformaldehyde, PFA) (HY-DY3003)
组织细胞固定液 (4% PFA)
蔗糖
AntiFade Mounting Medium (with DAPI) (HY-K1047)
抗荧光淬灭封片剂 (含 DAPI)
Polyethylene glycol mono(4-tert-octylphenyl) ether (HY-Y1883A)
聚乙二醇单辛基苯基醚 X-100
参考文献
[1] Qin C, et al. The Cutting and Floating Method for Paraffin-embedded Tissue for Sectioning. J Vis Exp. 2018 Sep 5;(139):58288.[2] Zaquot et al. (2020). Immunofluorescence Staining of Paraffin Sections Step by Step.[3] Punchihewa et al. (2021). Immunostained Frozen Sections Vs Traditional Permanent Paraffin Sections for Lentigo Maligna.[4] Davis et al. Preparation of Frozen Sections.[5] Spencer L T. Microtomy for paraffin and frozen sections[J]. Bancroft’s Theory and Practice of Histological Techniques, 8th ed.; Suvarna, SK, Layton, C., Bancroft, JD, Eds, 2018: 84-95.[6] Ma X, et al. Protocol for Xenium spatial transcriptomics studies using fixed frozen mouse brain sections. STAR Protoc. 2024 Dec 20;5(4):103420.


https://blog.sciencenet.cn/blog-3536222-1528590.html
上一篇:国自然申报中的ai药物筛选_MCE 中国