ВЉЮФ
ПЦбажњЙЅ Ѓќ RTKsЁУ МШЪЧМЄУИ, вВЪЧЪмЬх ИЩЛѕвбећРэКУ, ЫйРРЃЁЃќ MCE
|
жкЫљжмжЊЃЌЕААзжЪгаФЧУДЖрЖрЖрЖрЖрЖрЕФЙІФмЭљЭљЖМЪЧашвЊОЙ§аоЪЮВХФмЪЕЯжЕЮЃЌЖјЕААзжЪЕФаоЪЮЭЈГЃгЩУИЧ§ЖЏЁЃGЃЌгаетбљвЛРрМцОпМЄУИгыЪмЬхЕФЫЋжиЙІФмЕФУИРрЃЌСЫНтвЛЯТЃП
Section.01
ЪмЬхРвАБЫсМЄУИ (RTKs)ЃЌ
СЫНтвЛЯТЃЁ
ЬсЕНУИЃЌДѓМвзюЪьЯЄЕФгІИУЪЧетвЛЖдЃКМЄУИ (Kinase) ЁЊЁЊ СзЫсЛЏЃЌСзЫсЛЏУИ (Phosphorylase) ЁЊЁЊ ШЅСзЫсЛЏЁЃОпЬхаЁ M ВЛдйзИЪіЃЌИааЫШЄЕФаЁЛяАщПЩвдЗЗЭљЦкЭЦЮФЃКЁАМЄУИЁБгыЁАСзЫсУИЁБЃЌАаЯђжЮСЦСНЪжзЅЁЃ
БОЦкЮвУЧжиЕувЊСФЕФЪЧаХКХЭЈТЗжаЕФживЊВЮгыепЁЊЁЊЕААзМЄУИЃЁЦфжаЃЌЪмЬхРвАБЫсМЄУИ (Receptor Tyrosine Kinases, RTKs) ОпБИМЄУИгыЪмЬхЕФЫЋжиЙІФмЃЌЪЧЙцФЃзюДѓЕФвЛРрПчФЄУИСЊЪмЬхЃЁ
RTKs ЕФНсЙЙзщГЩ
RTKs МвзхгЩБЃЪиЕФНсЙЙгђЙЙГЩЃЌМДОпБИХфЬхНсКЯЮЛЕуЕФЯИАћЭтНсЙЙгђЁЂЕЅДЮПчФЄЕФЪшЫЎ ІС Тна§ЧјЃЌвдМАгЕгаРвАБЫсЕААзМЄУИ (PTK) ЛюадЕФЯИАћФкНсЙЙгђ[1][2]ЁЃ
ЯИАћЭтНсЙЙгђЃКОпБИХфЬх (ЩњГЄвђзг) НсКЯЮЛЕуЃЌИКд№ЪЖБ№ВЂНсКЯЬиЖЈХфЬхЁЃДЫВПЗжАќКЌЖржжОпгаЬиЖЈАБЛљЫсађСаЕФНсЙЙгђЃЌР§ШчИЛАыызАБЫсНсЙЙгђЁЂЫсадНсЙЙгђЁЂУтвпЧђЕААзбљНсЙЙгђЕШЁЃ
ПчФЄЧјЃКЭЈГЃЮЊЕЅДЮПчФЄЕФЪшЫЎ ІС Тна§ЧјЃЌЦ№ЕНСЌНгАћЭтЧјгыАћФкЧјЕФзїгУЁЃ
ЯИАћФкНсЙЙгђЃККЌгаРвАБЫсЕААзМЄУИЛюадгђЃЌНшжњздСзЫсЛЏвдМАЖдЯТгЮаХКХЕААзЕФСзЫсЛЏРДЦєЖЏаХКХзЊЕМЁЃ
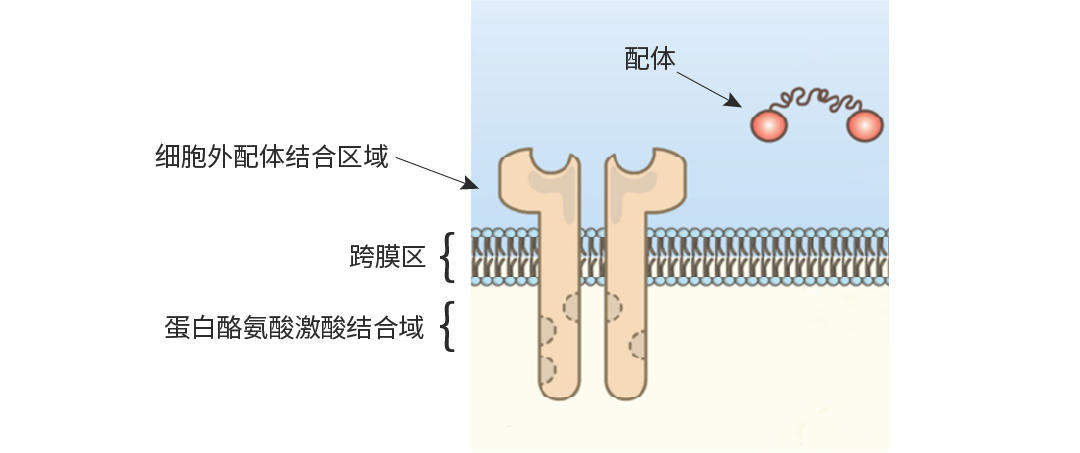
ЭМ 1. RTKs НсЙЙгђ[2]ЁЃ
RTKs ЕФМЄЛю
RTKs ЕФМЄЛюЪЧвЛИіЖрЮЌЖШЕФЙ§ГЬЃЌЪмЭтВПХфЬхПЩМАадгыФкдкЪмЬхЙЙЯѓЖЏСІбЇжЎМфЮЂУюЦНКтЕФгАЯь[1][3]ЁЃдкЗжзгВуУцЩЯЃЌRTKs МЄЛюВЂЗЧЕЅвЛЕФЪТМўЃЌЖјЪЧВЛЭЌЕїНкЛњжЦЕФЛуОлЃЌетаЉЛњжЦЗДгГСЫЫќУЧЫљЕїПиЕФИДдгЩњЮяЯЕЭГЁЃ
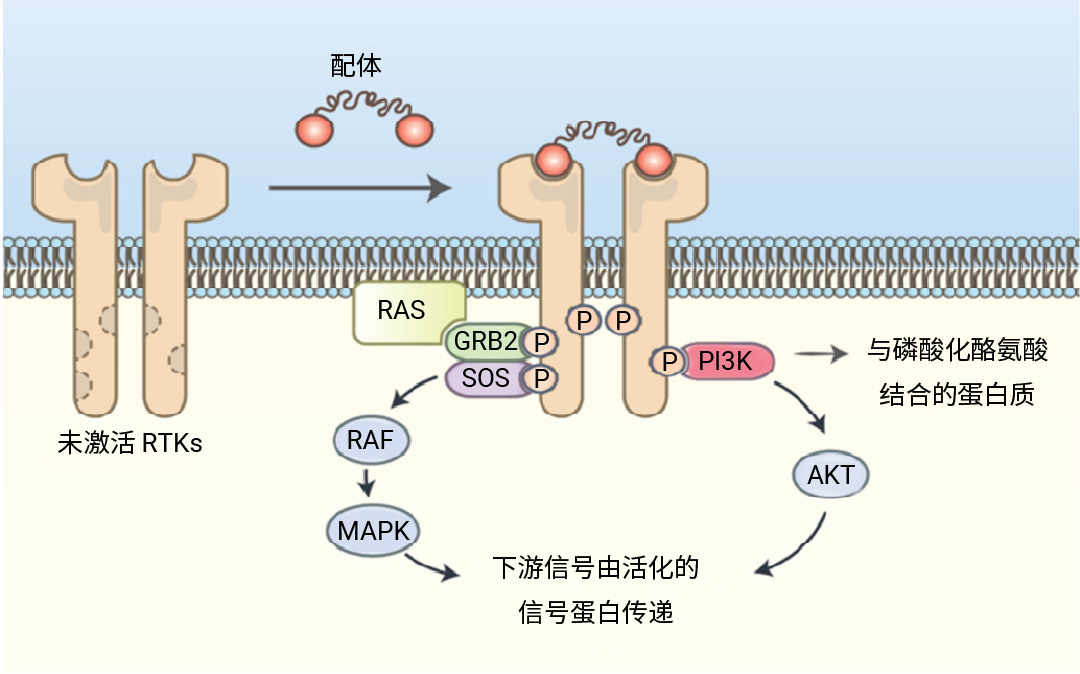
ЭМ 2. RTKs МЄЛюЙ§ГЬ[2]ЁЃ
Section.02
RTKsМвзхДѓХЬЕу
ШЫРрЬхФквбМјЖЈГі 58 жж RTKsЃЌетаЉЕААзвРОнЦфЯИАћЭтНсЙЙгђЕФзщГЩВювьБЛЛЎЗжЮЊ 20 ИіМвзхЃЌЦфЖРЬиЕФНсЙЙЬиеїОіЖЈСЫЫќУЧдкЯИАћаХКХДЋЕМжаЙІФмЕФЖрбљад (ЭМ 1)[1][3]ЁЃЭЌвЛМвзхЕФГЩдБЭЈГЃФмЙЛЪЖБ№ВЂНсКЯЯрЭЌЛђНсЙЙЯрЫЦЕФХфЬхЃЌДгЖјМЄЛюЬиЖЈЕФЯТгЮаХКХЭЈТЗЁЃ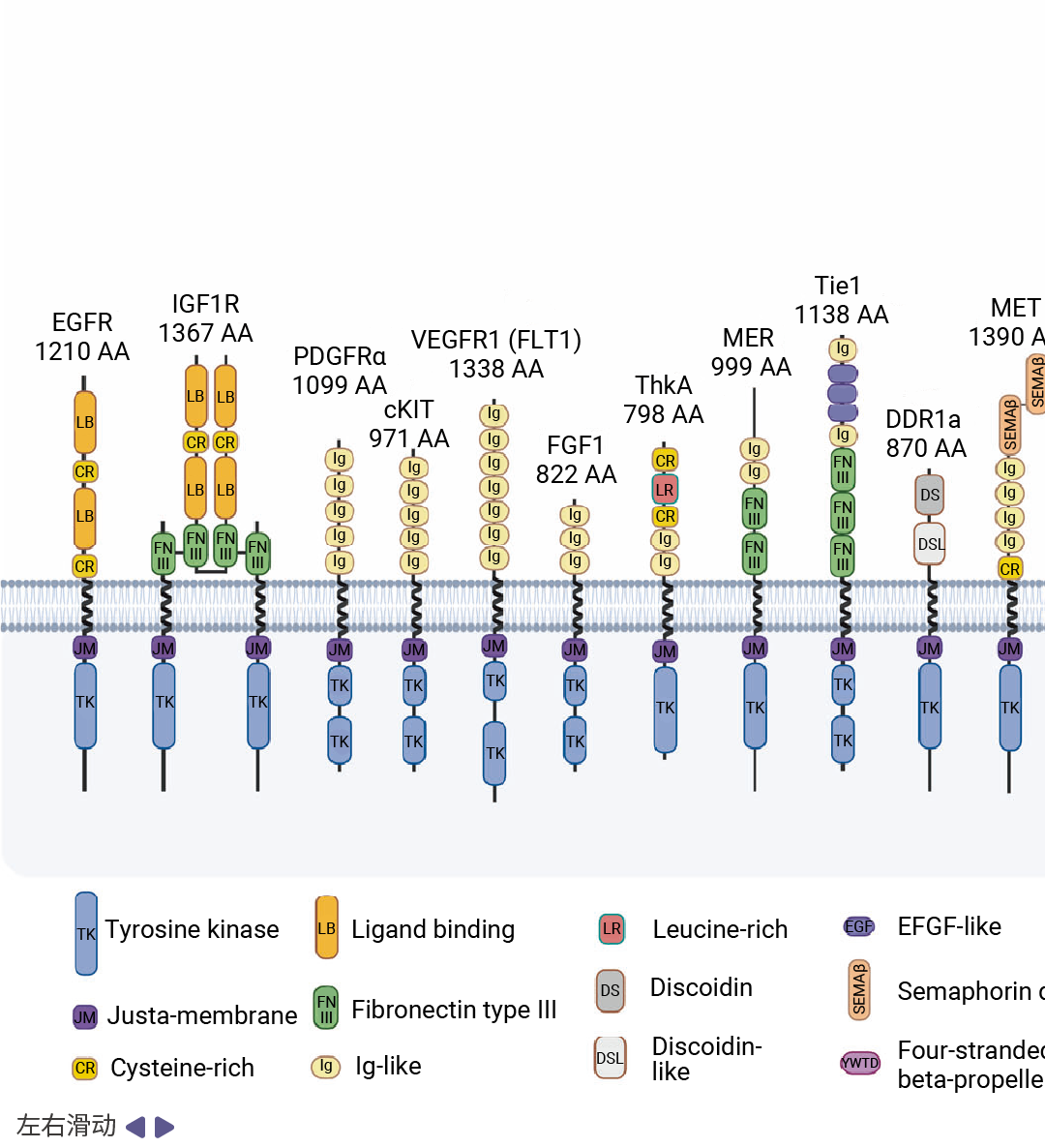
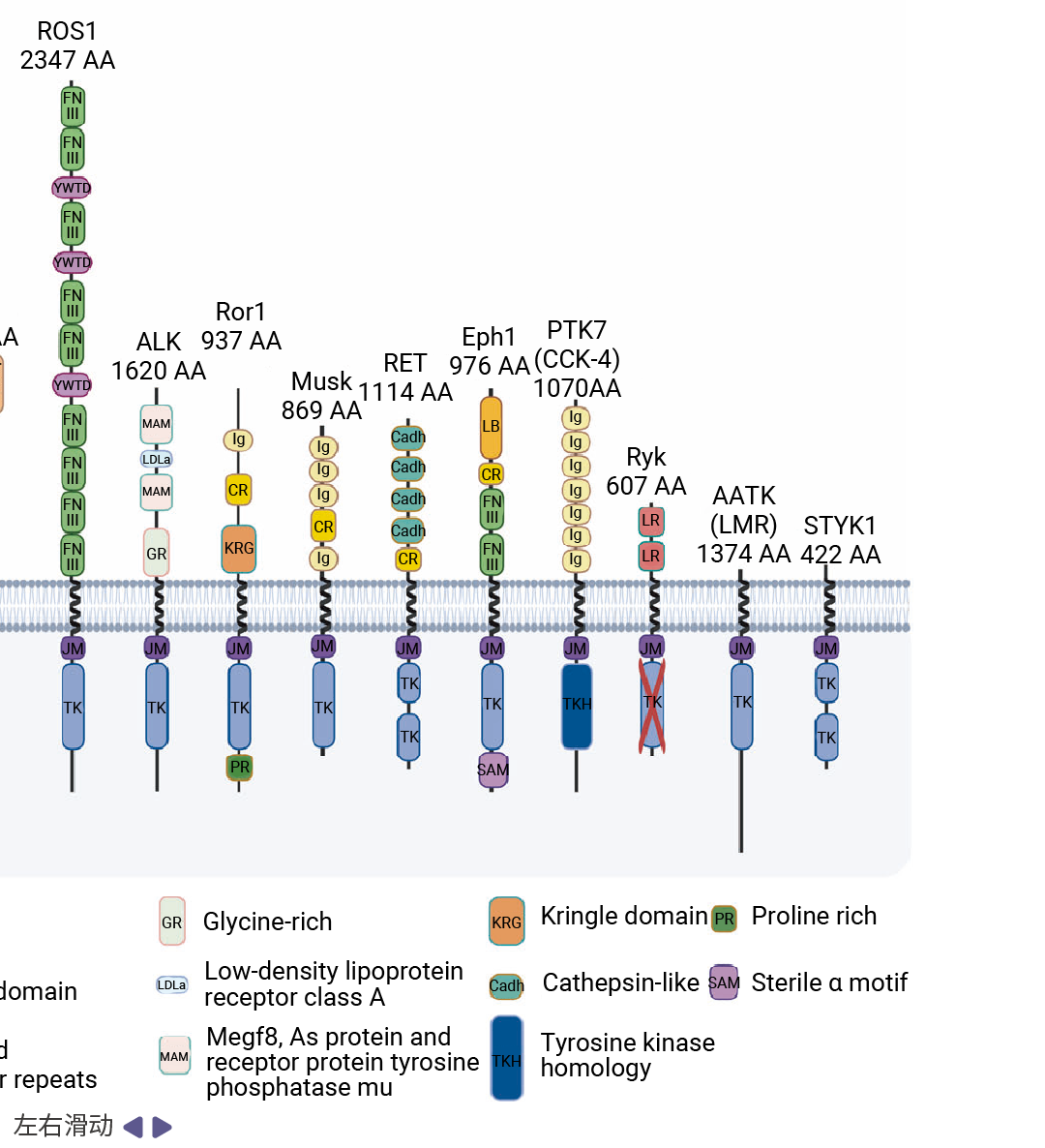
ЭМ 3. 20 жжЪмЬхРвАБЫсМЄУИЕФНсЙЙ[3]ЁЃ
ЯТУцЮвУЧжиЕуНщЩмЯТ RTKs жаЕФБэЦЄЩњГЄвђзгЪмЬх (EGFR/ErbB)ЁЂЩіЩЯЯйЫиЪмЬх (Eph) КЭГЩЯЫЮЌЯИАћЩњГЄвђзгЪмЬх (FGFR)ЁЃ
БэЦЄЩњГЄвђзгЪмЬх (EGFR/ErbB)
БэЦЄЩњГЄвђзгЪмЬх (EGFR/ErbB) МвзхгЩЫФжжИпЖШЭЌдДЕФЪмЬхРвАБЫсМЄУИЙЙГЩЃЌКИЧ ErbB - 1 (HER1/EGFR)ЁЂErbB - 2 (HER2/Neu)ЁЂErbB - 3 (HER3) КЭ ErbB - 4 (HER4)ЁЃетаЉЪмЬхдкМфГфжЪЁЂЩЯЦЄМАЩёОдЊРДдДЕФзщжЏжаЙуЗКБэДяЃЌЭЈЙ§ЕїПиЯИАћЕФдіжГЁЂЗжЛЏКЭДцЛюЃЌВЮгыЖржжЩњРэЙ§ГЬ[4]ЁЃ
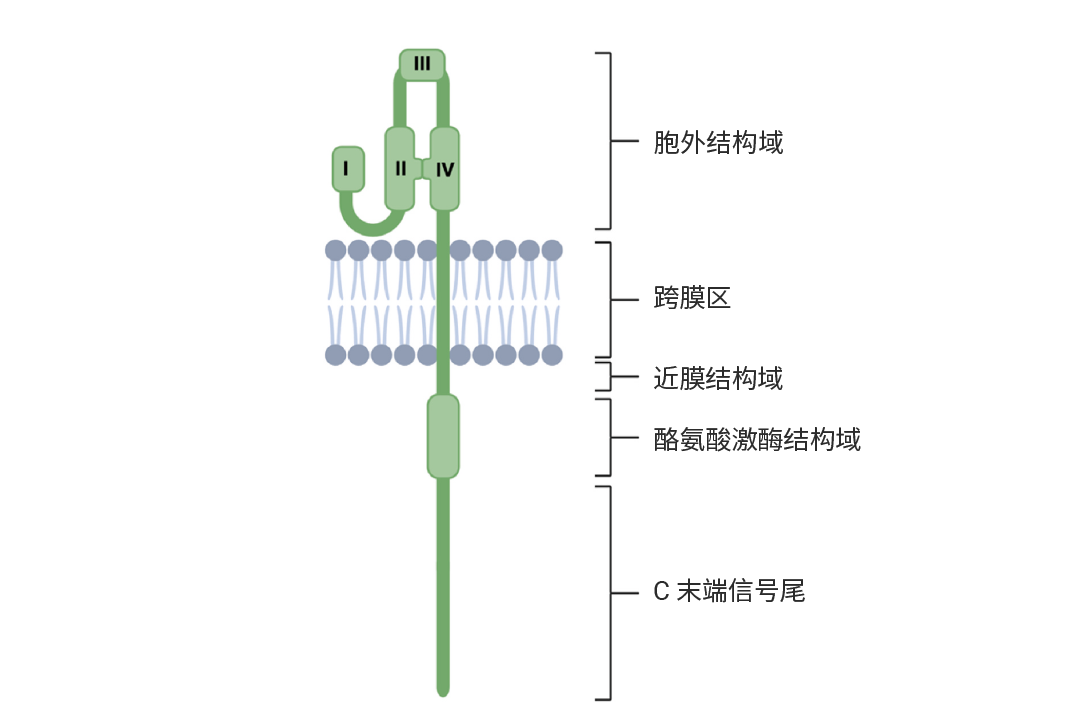
ЭМ 4. ErbB-3 ЪмЬхЕФЕЅЬхаЮЪНЪОвтЭМ[6]ЁЃ
Eph ЪмЬх
Eph ЪмЬхЪЧФПЧАвбжЊЕФЪмЬхРвАБЫсМЄУИ (RTKs) жазюДѓЕФМвзхЃЌЦфХфЬхЮЊВњЩњДйКьЯИАћЩњГЩЫиЕФИЮАЉЪмЬхЯрЛЅзїгУЕААз (Ephrins)[7]ЁЃдкВИШщЖЏЮяжаЃЌИУМвзхвбМјЖЈГі 14 ИіГЩдБЁЃвРОнађСаЭЌдДадЁЂХфЬхНсКЯЬиадвдМАНсЙЙВювьЃЌЫќУЧБЛЯЕЭГЕиЛЎЗжЮЊ EPHA (АќКЌ EPHA1 - 8 МА EPHA10) КЭ EPHB (АќКЌ EPHB1 - 4 МА EPHB6)ЁЃ
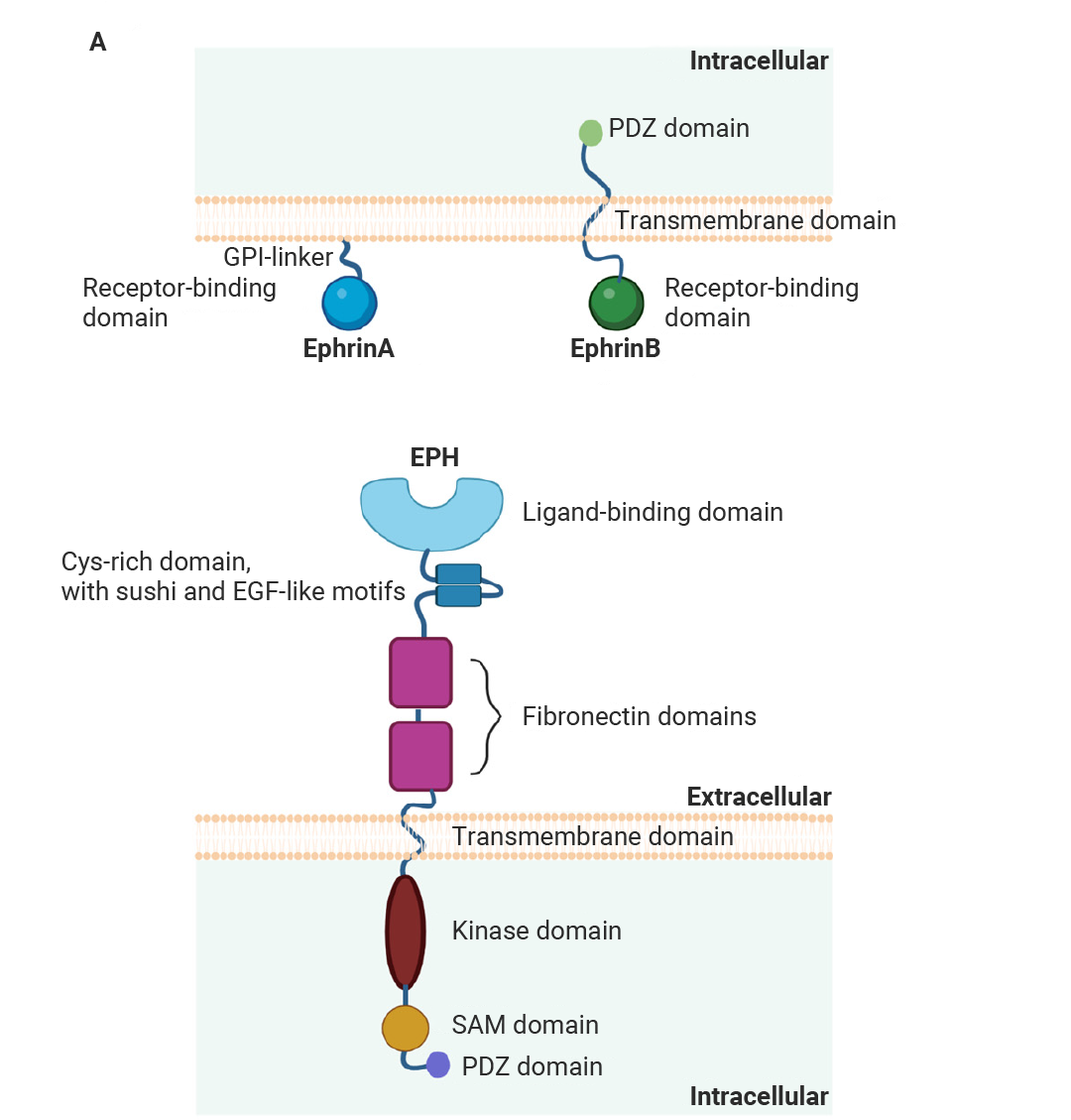
ЭМ 5. Ephrins гы Eph ЪмЬхЕФНсЙЙ[8]ЁЃ
ГЩЯЫЮЌЯИАћЩњГЄвђзгЪмЬх (FGFR)
ГЩЯЫЮЌЯИАћЩњГЄвђзгЪмЬх (FGFR) ЪЧвЛРрОпгаИпЖШБЃЪиадЕФПчФЄРвАБЫсМЄУИЪмЬхЃЌФмЙЛЬивьадЕигыГЩЯЫЮЌЯИАћЩњГЄвђзг (FGF) ЕААзМвзхЕФВЛЭЌХфЬхЯрНсКЯЁЃдкМЙзЕЖЏЮяжаЃЌвбМјЖЈГіЮхжжВЛЭЌЕФФЄ FGFRЃЌЫќУЧОљСЅЪєгкРвАБЫсМЄУИГЌМвзх (FGFR1ЁЂFGFR2ЁЂFGFR3ЁЂFGFR4ЁЂFGFR5)[9]ЁЃЦфжаВПЗжЪмЬхгыВЁРэзДПіДцдкЙиСЊЃЌР§Шч FGFR3 жаЕФЕуЭЛБфПЩОгЩзщГЩаЭМЄЛюЪмЬхЃЌНјЖјв§ЗЂШэЙЧЗЂг§ВЛШЋЁЃ
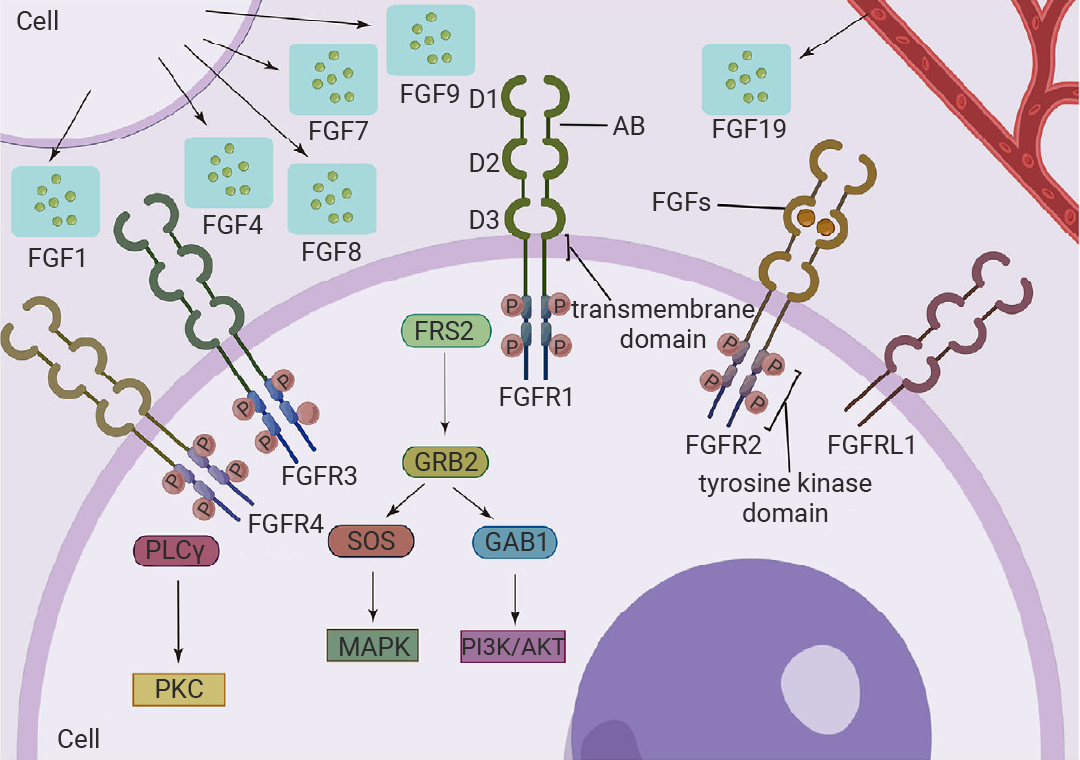
ЭМ 6. FGFR МвзхЕФЛљБОНсЙЙ[9]ЁЃ
Section.03
RTKs ЪЇЕїгыАЉжЂ
RTKs ЭЈЙ§ЕїПиЯИАћдіжГЁЂДцЛюЁЂЧЈвЦвдМАбЊЙмЩњГЩЕШЙиМќЭЈТЗЃЌЮЌГжЛњЬхЕФе§ГЃЩњРэЮШЬЌЁЃЕЋдкАЉжЂЕФЗЂЩњгыЗЂеЙЙ§ГЬжаЃЌRTKs ЕФвьГЃМЄЛюЪЧЧ§ЖЏжзСіЖёадзЊЛЏЕФКЫаФЛњжЦжЎвЛЁЃ
дкАЉЯИАћжаЃЌRTKs ЕФЪЇЕїжївЊгЩЙІФмЛёЕУадЭЛБфЁЂЙ§БэДягыЛљвђзщРЉдіЁЂШОЩЋЬхжиХХЁЂМЄУИНсЙЙгђжиИДвдМАздЗжУк/ХдЗжУкМЄЛюетЮхжжЛњжЦНщЕМ[3][10]ЁЃетаЉЛњжЦЛсжТЪЙ RTKs ЗЂЩњГжајадСзЫсЛЏЃЌНјЖјЙ§ЖШМЄЛюЯТгЮЕФжТАЉаХКХЭЈТЗЃЌДђЦЦЯИАћЩњГЄгыЫРЭіЕФЦНКтЃЌзюжев§ЗЂжзСізЊвЦЁЂбЊЙмЩњГЩвдМАжЮСЦФЭвЉадЁЃ
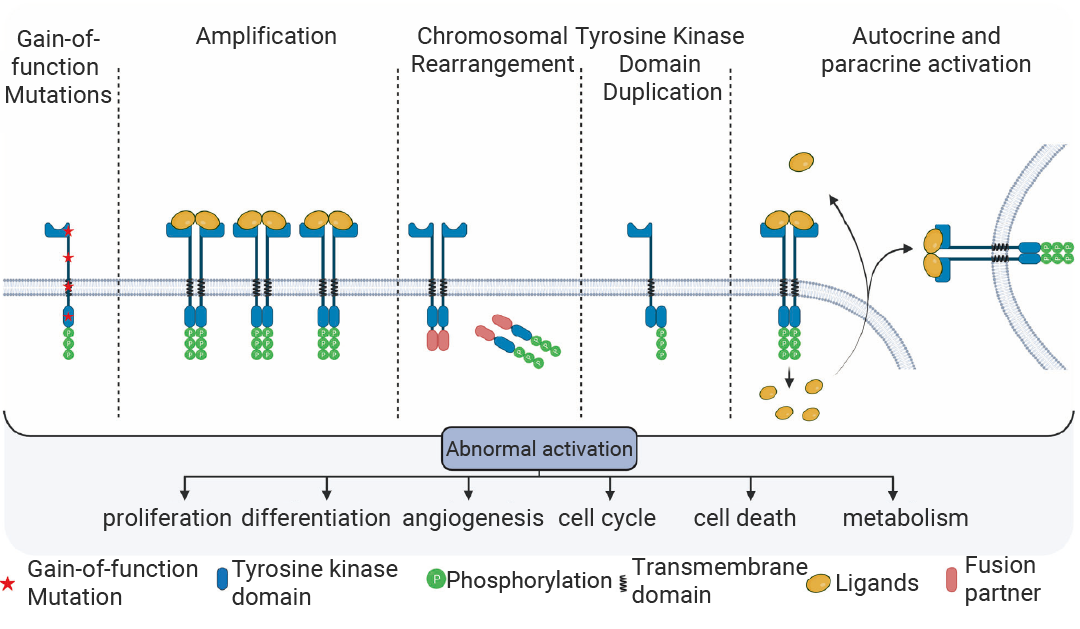
ЭМ 7. RTKs ЪЇЕїЛњжЦ[3]ЁЃ
ВњЦЗЭЦМі |
EGFR/ErbB МвзхгЩЫФжжНєУмЯрЙиЕФЪмЬхРвАБЫсМЄУИзщГЩЃЌЗжБ№ЪЧ ErbB-1 (HER1/EGFR)ЁЂErbB-2 (HER2)ЁЂErbB-3 (HER3) КЭ ErbB-4 (HER4)ЁЃ |
Eph ЪмЬхПЩЗжЮЊ EphA Лђ EphB бЧМвзхЃЌФіГнЖЏЮяжага 9 ИіEphA КЭ 5 Иі EphB ГЩдБЁЃ |
дкШЫРржаЃЌФПЧАМјЖЈГі 6 Иі FGFR МвзхГЩдБ (FGFR1-6)ЁЃ |
TAM ЪмЬхМвзхгЩШ§жжБЃЪиЕФЪмЬхРвАБЫсМЄУИзщГЩЃЌМД Tyro3ЁЂAxl КЭ MerЁЃ |
бЊЙмФкЦЄЩњГЄвђзгЪмЬх (VEGFR) Мвзх гЩШ§жжЕААзРвАБЫсМЄУИ (VEGFR1ЁЂVEGFR2 КЭ VEGFR3) КЭСНжжЗЧЕААзМЄУИЙВЪмЬх (neuropilin-1 КЭ neuropilin-2) зщГЩЁЃ |
Trk МвзхгЩ TrkAЁЂTrkB КЭ TrkC Ш§жжЪмЬхРвАБЫсМЄУИ (RTKs) зщГЩЃЌгжГЦЮЊЩёОгЊбјРвАБЫсЪмЬхМЄУИЁЃ |
ЪмЬхРвАБЫсМЄУИбљЙТЖљЪмЬх (ROR) МвзхЃЌАќКЌЯИАћЭтОэЧњбљАыызАБЫсИЛНсЙЙгђ (CRDs) КЭФЄНќЖЫ Kringle НсЙЙгђЁЃдкМЙзЕЖЏЮяжаЃЌRORs МвзхгЩ Ror1 КЭ Ror2 СНИіНсЙЙЯрЙиЕФГЩдБзщГЩЁЃ |
бЊаЁАхбмЩњЩњГЄвђзгЪмЬх (PDGFRs) жївЊЮЛгкбЊЙмФкЦЄЯИАћЁЂГЩЯЫЮЌЯИАћКЭ Kupffer ЯИАћЃЌга PDGFR-ІС КЭ PDGFR-ІТ СНжжРраЭЁЃ |
ХЬзДНсЙЙгђЪмЬхАБЫсМЄУИ (DDRs) МвзхАќРЈСНИіВЛЭЌЕФГЩдБЃЌDDR1 КЭ DDR2ЁЃDDRs БэДяЙуЗКЃЌDDR1 жївЊБэДягкЩЯЦЄЯИАћЃЌDDR2 жївЊБэДягкМфГфжЪЯИАћЁЃ |

[1] Zhang N, et al. Receptor tyrosine kinases: biological functions and anticancer targeted therapy. MedComm (2020). 2023;4(6):e446.
[2] Azad T, et al. Hippo Signaling Pathway as a Central Mediator of Receptors Tyrosine Kinases (RTKs) in Tumorigenesis. Cancers (Basel). 2020;12(8):2042.
[3] Tomuleasa C, et al. Therapeutic advances of targeting receptor tyrosine kinases in cancer. Signal Transduct Target Ther. 2024;9(1):201.
[4] Talukdar S, et al.. EGFR: An essential receptor tyrosine kinase-regulator of cancer stem cells. Adv Cancer Res. 2020;147:161-188.
[5] Chen Y, et al. ERBB3 targeting: A promising approach to overcoming cancer therapeutic resistance. Cancer Lett. 2024;599:217146.
[6] Yu J, et al. Antibody-Drug Conjugates Targeting the Human Epidermal Growth Factor Receptor Family in Cancers. Front Mol Biosci. 2022;9:847835.
[7] Zhu Y, et al. Recent advances of the Ephrin and Eph family in cardiovascular development and pathologies. iScience. 2024;27(8):110556.
[8] Stergiou IE, et al. EPH/Ephrin Signaling in Normal Hematopoiesis and Hematologic Malignancies: Deciphering Their Intricate Role and Unraveling Possible New Therapeutic Targets. Cancers (Basel). 2023;15(15):3963.
[9] Liu Q, et al. FGFR families: biological functions and therapeutic interventions in tumors. MedComm (2020). 2023;4(5):e367.
[10] Ebrahimi N, et al. Receptor tyrosine kinase inhibitors in cancer. Cell Mol Life Sci. 2023;80(4):104.
[11] Gotoh N. Somatic mutations of the EGF receptor and their signal transducers affect the efficacy of EGF receptor-specific tyrosine kinase inhibitors. Int J Clin Exp Pathol. 2011;4(4):403-409.
[12] Kannan S, et al. Conformational landscape of the epidermal growth factor receptor kinase reveals a mutant specific allosteric pocket. Chem Sci. 2018;9(23):5212-5222.
[13] Riese DJ 2nd, et al. Mutational activation of ErbB family receptor tyrosine kinases: insights into mechanisms of signal transduction and tumorigenesis. Bioessays. 2007;29(6):558-565.
[14] Hayes TK, et al. Comprehensive mutational scanning of EGFR reveals TKI sensitivities of extracellular domain mutants. Nat Commun. 2024;15(1):2742.
[15] Zhang P, et al. Targeting FGFR for cancer therapy. J Hematol Oncol. 2024;17(1):39.
[16] Liu Q, et al. FGFR families: biological functions and therapeutic interventions in tumors. MedComm (2020). 2023;4(5):e367.
[17] Krook MA, et al. Fibroblast growth factor receptors in cancer: genetic alterations, diagnostics, therapeutic targets and mechanisms of resistance. Br J Cancer. 2021;124(5):880-892.
https://blog.sciencenet.cn/blog-3536222-1513457.html
ЩЯвЛЦЊЃКИЩЛѕЗжЯэ Ѓќ ВЛЖЎОЭЮЪЁУ жЛгаУтвпЯИАћФмЗжУкЯИАћвђзгУД Ѓќ MCE
ЯТвЛЦЊЃКЧАбиНјеЙ Ѓќ Cell зюаТЗЂЯжЃКMitoxyperilysis ЁЊЁЊ аТЕФЯИАћШмНтадЫРЭіЭООЖ Ѓќ MCE
ШЋВПзїепЕФЦфЫћзюаТВЉЮФ
- • AI ЩИбЁ + ащФтЩИбЁЃКаТвЉбаЗЂЕФ ЁАЫЋв§ЧцЁБ ЕФКЫаФТпМ_MCE(MedChemExpress)
- • AACR ТфФЛЃЌaiвЉЮяЩИбЁЁЂаЁЗжзгвЉЮяЁЂЩњЮявЉЁЂПЙЬхХМСЊвЉЮяADC МЏССЯр_MCE
- • Neuron | TEE ЭЈЙ§ ReExc-BLAInh ЛиТЗФцзЊЧщаїеЯА_MCE(MedChemExpress)
- • ВЛжЙЛљвђгыЕААзЃЌЬЧДњТые§ГЩЮЊМВВЁеяСЦаТУмдП_MCE(MedChemExpress)
- • РрЦїЙйЖрЮЌМјЖЈЃЈЛљвђВтађЕШЃЉ__ MCE (MedChemExpress)
- • ПЙЬхХМСЊвЉЮя ADC КЭздЩэУтвпадМВВЁ_MCE(MedChemExpress)