博文
Pharmaceuticals:靶向血脑屏障的纳米粒子——特性与神经科学应用
||
研究背景
阿尔茨海默病 (AD)、帕金森病 (PD)、多发性硬化症 (MS) 及中风等神经系统疾病的治疗面临一个共同难题:如何将药物有效递送至脑部。血脑屏障 (BBB) 作为大脑的天然保护屏障,其紧密连接的内皮细胞结构阻止了大多数大分子和亲脂性低的药物分子进入脑实质,从而成为神经药物开发的核心挑战。
近年来,纳米颗粒 (NPs) 凭借其独特的理化性质,展现出作为高效药物递送平台的巨大潜力。尽管许多纳米颗粒已获得美国食品药品监督管理局 (FDA) 批准用于一般医学,但本文指出,目前仅有一种纳米颗粒获批用于脑靶向治疗 (治疗多发性硬化症)。然而,目前已有超过13项针对精神分裂症和胶质母细胞瘤等疾病的临床试验正在进行中,该领域正处于一个重要的转折点。本文综述了优化纳米颗粒以增强其血脑屏障穿透性的关键策略、评估模型、在病理条件下的应用前景以及未来的发展方向。
主要内容
一、 优化纳米颗粒穿透BBB的关键物理化学特性
NPs的BBB穿透效率高度依赖于其可设计的物理化学性质,主要包括尺寸与形状、化学组成与生物降解性、表面电荷三个方面。
1. 尺寸与形状:BBB内皮细胞间的紧密连接限制了分子量大于400 Da的物质自由通过。研究表明,NPs存在一个穿透BBB的“黄金窗口”:尺寸小于5纳米的NPs易被肾脏快速清除,而大于100纳米的则难以穿透BBB。最优尺寸范围通常在10-100纳米之间。形状上,尽管球形NPs最为常见,但棒状NPs因更易黏附于脑内皮细胞,表现出更高的脑内积累量。
2. 化学组成与生物降解性:材料的脂溶性直接影响其穿透脂质双分子层的能力。脂质体NPs因其与生物膜的相容性而被广泛应用。同时,材料的生物可降解性至关重要,如PLGA、壳聚糖等聚合物,能在完成递送任务后被安全清除,避免长期毒性,并实现可控的药物释放。
3. 表面电荷:BBB内皮细胞表面因富含蛋白聚糖而呈负电性,带正电荷 (阳离子) 的NPs通过静电吸附作用更易贴近并穿透细胞膜。然而,高浓度的阳离子NPs可能破坏BBB完整性并引发毒性。相比之下,中性或弱负电的NPs生物相容性更好,但可能需要依赖主动靶向策略。
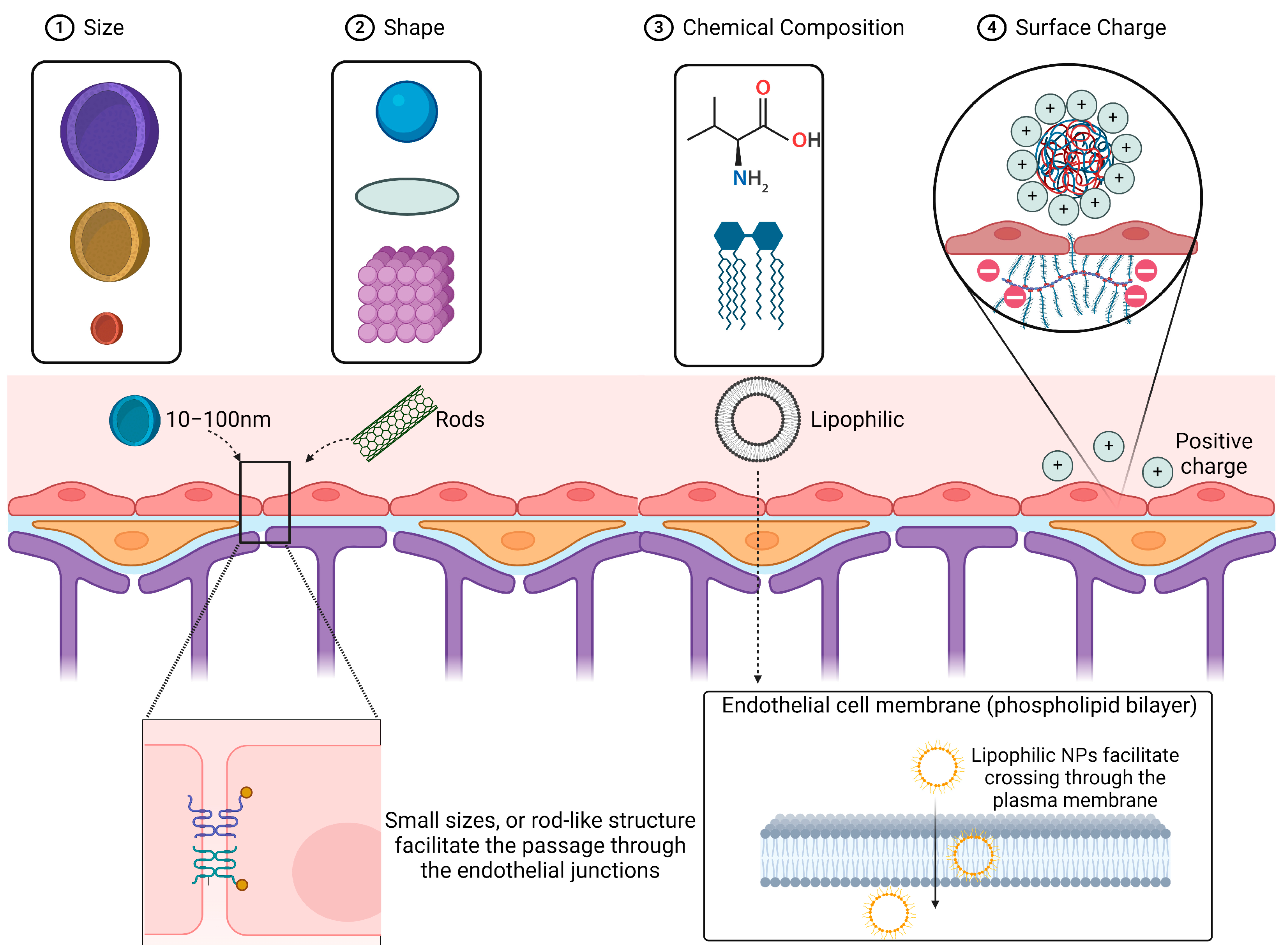
图1. 纳米粒子的尺寸、形状、化学成分和表面电荷是影响纳米粒子穿透血脑屏障能力的四个主要因素。具有棒状结构的小NPs、亲脂性NPs和带正电荷的NPs具有更高的穿越血脑屏障内皮连接的能力。
主动靶向:表面功能化修饰的核心策略
单纯依靠物理化学性质的被动靶向效率有限。对NPs表面进行功能化修饰,使其能够“识别”BBB上的特定受体,是实现高效主动靶向的关键。
1. 葡萄糖及衍生物:通过连接葡萄糖或麦芽糖酸,NPs可劫持BBB上高表达的葡萄糖转运蛋白1 (GLUT1),实现高效跨细胞转运。此法在脑肿瘤靶向中尤为有效。
2. 转铁蛋白 (Tf):Tf受体在BBB内皮细胞上高表达。Tf修饰的NPs通过受体介导的胞吞作用进入大脑。优化策略 (如使用酸可裂解连接键) 能促进NPs在胞内释放,提高入脑效率。
3. 胰岛素及特异性肽段:胰岛素是另一种对血脑屏障转运至关重要的配体,能与内皮细胞上的胰岛素受体 (IR) 结合。将肽与纳米颗粒偶联,可促进其穿透BBB。
4. 聚乙二醇 (PEG) 化:在NPs表面连接PEG长链,形成保护膜,减少循环中的纳米颗粒与其他血液成分的相互作用,降低调理作用和吞噬作用,从而减少从循环中的清除。此外,PEG可作为配体分子的连接剂,实现对大脑的主动靶向。
5. 肽:肽功能化的纳米颗粒为穿过血脑屏障和精准靶向治疗脑部疾病提供了一种有效途径。通过使用受体特异性肽,这些系统能够增强血脑屏障穿透性,提高细胞摄取率,并实现针对胶质母细胞瘤和神经退行性疾病的靶向递送,在临床前研究中显示出强大的治疗潜力。
6. 适体与表面活性剂:适体由单链寡核苷酸 (DNA或RNA) 组成,能折叠成特定三维结构并与特定分子结合。核酸适体可通过筛选获得高亲和力、高特异性的靶向分子。覆盖在NPs表面的表面活性剂 (如聚乙烯醇和泊洛沙姆188) 还可调节BBB的渗透。

图2. NP表面修饰及NP通过内皮细胞转运的机制。(A) 用于NPs的配体和化学基团包括葡萄糖、转铁蛋白、胰岛素、适体、肽、聚乙二醇 (PEG) 和表面活性剂。这些表面功能化基团促进NPs通过血脑界面进入并被大脑摄取。(B) 具有配体和化学基团的NP可被葡萄糖转运蛋白 (GLUT-1)、转铁蛋白受体 (TfR)、低密度脂蛋白受体相关蛋白1 (LRP-1) 受体和胰岛素受体 (IR) 等细胞表面受体识别,通过不同的机制促进NP跨细胞转运。
评估NPs穿透效果的实验模型体系
评估NPs穿透BBB的效果需依赖多种实验模型,包括体外模型和体内模型。
1. 体外模型:
Transwell模型:血脑屏障内皮细胞单层培养在多孔膜插入物上,其他神经细胞培养在基底外侧室中。虽缺乏直接细胞间通讯,但可通过分泌可溶性蛋白间接调节BBB。
3D模型与微流控芯片:水凝胶共培养模型、脑微球/类器官能更好地模拟细胞外基质和细胞三维结构。微流控“芯片上的BBB”引入生理相关的流体剪切力,允许实时观测NPs的转运过程。
2. 体内模型与临床检测:
动物模型:小鼠和大鼠是最常用的动物模型,通过静脉注射后,利用荧光成像、质谱、放射性标记等手段定量分析NPs在脑组织中的分布。
疾病模型:如AD转基因鼠、脑肿瘤原位模型,可评估病理条件下的递送效果。
临床检测:正电子发射断层扫描 (PET) 和单光子发射计算机断层扫描(SPECT) 可用于可视化放射性标记的NPs在活体人脑中的分布。
未来展望与挑战
本文总结了影响NPs穿透BBB的关键特性,包括尺寸和形状、化学组成、表面电荷、表面活性剂以及与靶向配体或分子的结合等。随着对NPs的深入了解和开发,其在神经系统疾病治疗中的应用前景广阔。然而,如何进一步优化NPs的物理化学性质,提高其靶向效率和生物相容性,仍是未来研究的重点。同时,开发更加精准、高效的体外和体内评估模型,将有助于加速NPs递送系统的临床转化。
阅读英文原文:https://www.mdpi.com/1424-8247/17/5/612
Pharmaceuticals 期刊介绍
主编:Amélia Pilar Rauter, Universidade de Lisboa, Portugal
期刊主题涵盖了药物化学、药理学、生物制药、药物递送、药物控释、药物制剂、天然产物、药代动力学和纳米医学等。目前期刊已被SCIE、Scopus和PubMed等数据库收录,位列JCR“药物化学”和“药理学与药学”两个学科领域Q1区。
2024 Impact Factor:4.8
2024 CiteScore:7.7
Time to First Decision:16 Days
Acceptance to Publication:3.4 Days
期刊主页:https://www.mdpi.com/journal/pharmaceuticals

https://blog.sciencenet.cn/blog-3516770-1527350.html
上一篇:Plants:青年编委会名单公布!
下一篇:Nanomaterials:“生物学和医学”栏目 | MDPI 栏目推荐