博文
Cells:FASN驱动结直肠癌干性,FASN/ β-catenin/ NOTUM轴成为癌症预防新靶点
||
文章导读
结直肠癌 (Colorectal Cancer, CRC) 是全球癌症相关死亡主因之一,而癌细胞干性是肿瘤发生、进展和复发的关键。Wnt/β-catenin通路异常激活是结直肠癌核心特征,约80%结直肠癌的发病与 APC基因突变相关,该突变会引发β-catenin (β-连环蛋白) 累积并激活促癌信号。脂肪酸合成酶 (Fatty Acid Synthase, FASN) 过表达与结直肠癌患者不良预后相关,并与β-catenin通路互作增强癌细胞干性。NOTUM,一种羧基酯酶,虽能抑制Wnt信号,却为癌症干细胞特征蛋白之一,也与结直肠癌不良预后相关。本研究核心探究FASN、β-catenin与NOTUM的调控关系,及其对结直肠癌细胞干性的影响。
研究过程与结果
1.FASN缺失显著抑制小鼠肠道腺瘤中的癌干细胞标志物
研究人员在小鼠模型中敲除Fasn基因后,无论是杂合还是纯合缺失,都能观察到活化的β-catenin和NOTUM等干细胞标志物的表达水平急剧下降。
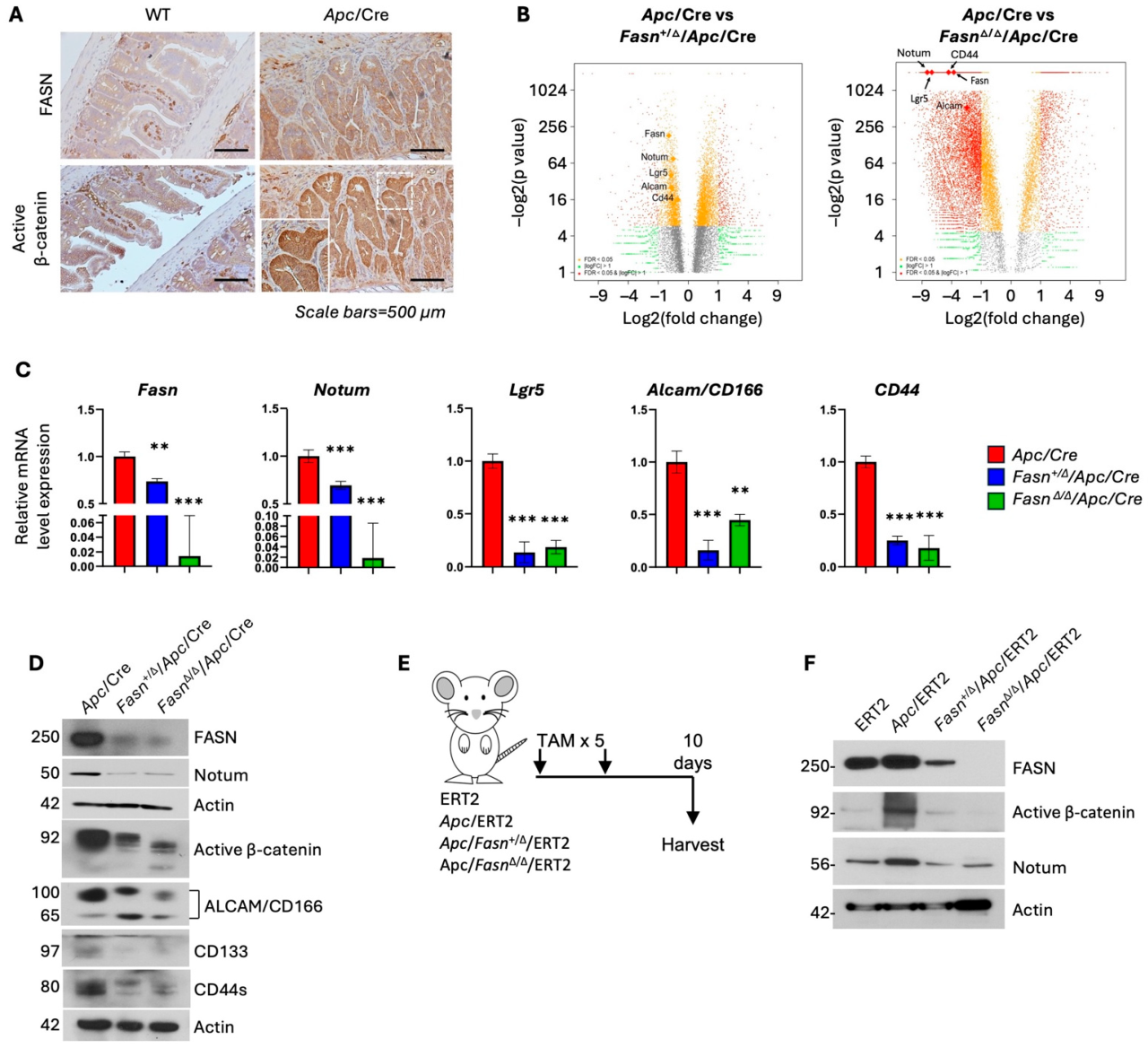
图1. 小鼠肠道组织中Fasn的杂合及纯合缺失降低了活性β-catenin的水平及NOTUM的表达。
2.FASN是维持腺瘤类器官生长和干性的关键
为了更直接地评估FASN对“干性”的影响,研究团队构建了可诱导的小鼠腺瘤类器官模型。首先通过药物诱导敲除Fasn基因后,腺瘤类器官的生长和克隆形成能力受到显著抑制。另外,使用FASN特异性抑制剂TVB-3664处理腺瘤类器官,同样得到了一致的结果。最后,无论是基因敲除还是药物抑制,都伴随着活化的β-catenin、NOTUM以及其他干性标志物蛋白水平的下调。
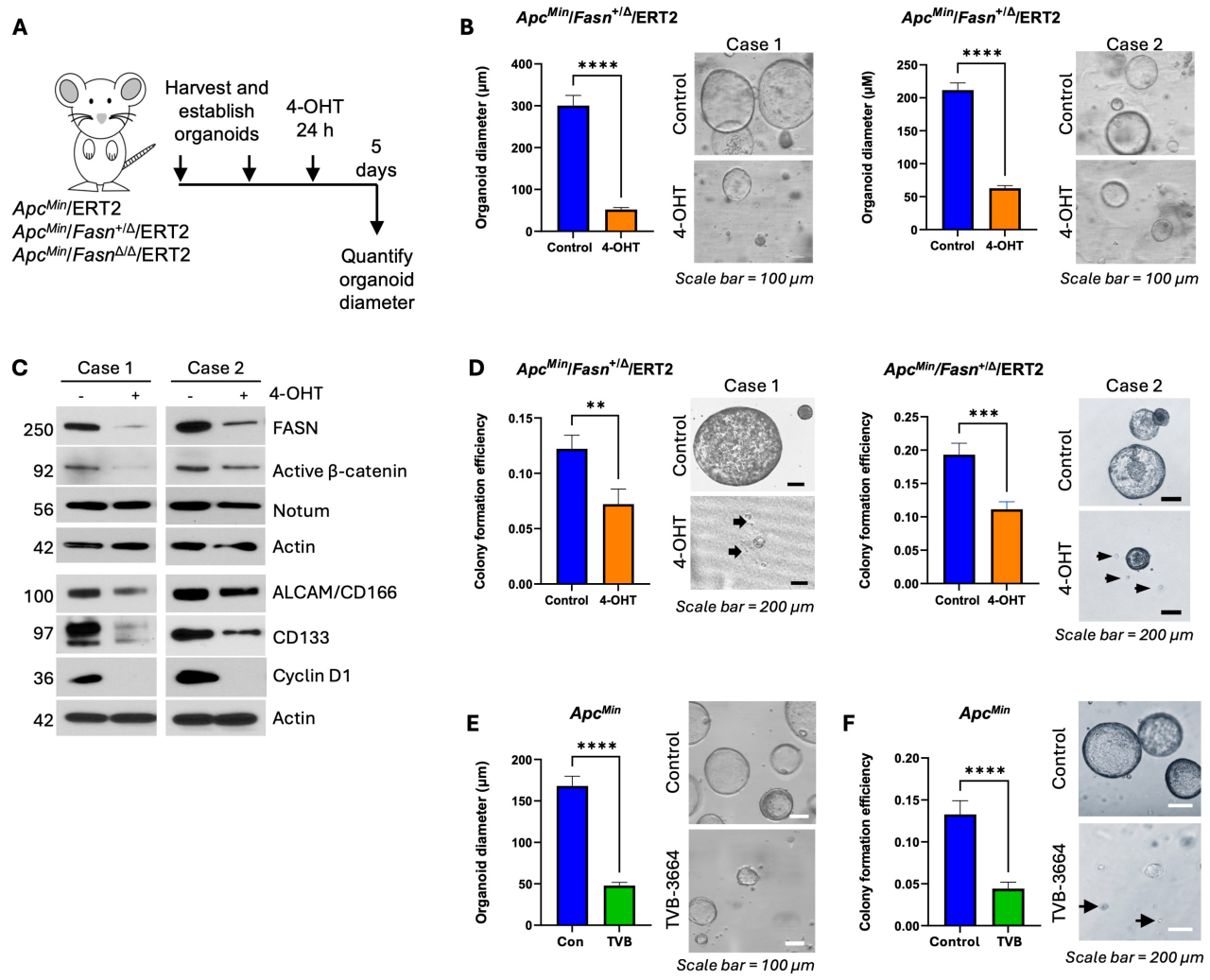
图2. FASN通过上调活性β-catenin、NOTUM、其他干细胞标志物,促进类器官形成与生长。
3.FASN/NOTUM轴在人类结直肠癌中高度相关且预后不良
团队分析了来自癌症基因组图谱 (TCGA-COAD) 的人类结直肠癌数据。在人类结直肠癌肿瘤组织中的NOTUM的mRNA表达远高于正常组织。在肿瘤组织中,FASN与NOTUM的mRNA表达水平呈现出强烈的正相关性,而在正常组织中则无此关联。高表达NOTUM的结直肠癌患者,其5年生存率显著低于低表达患者,凸显了该通路的临床重要性。
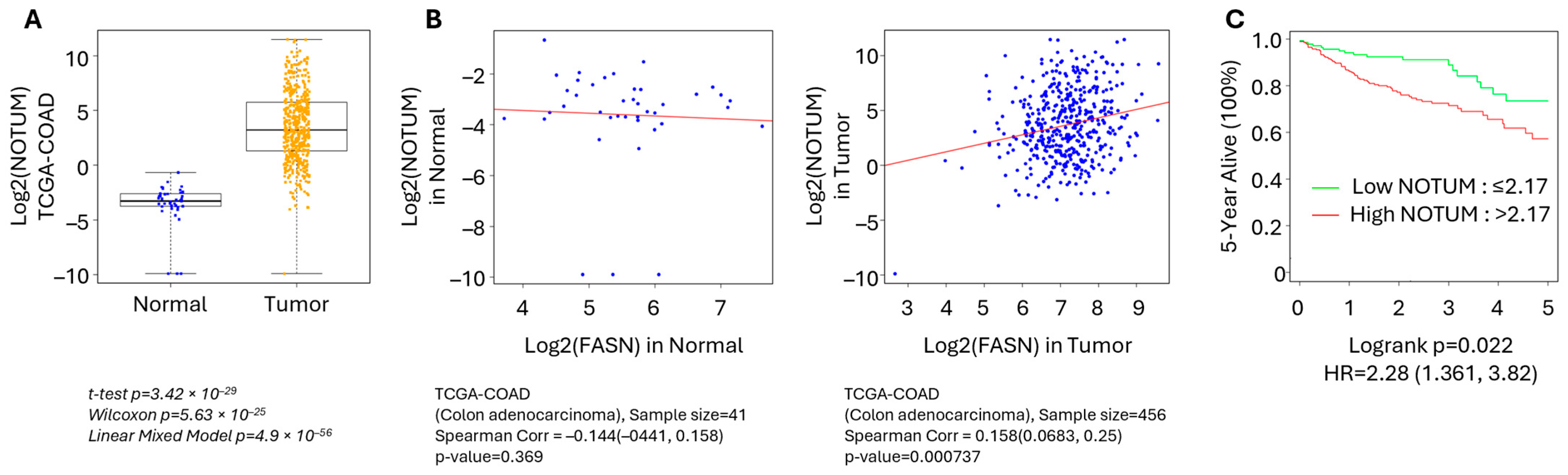
图3. NOTUM在人结直肠癌中呈过表达,并与FASN表达呈正相关。
4.FASN通过β-catenin直接调控NOTUM并增强癌细胞干性
过表达FASN的细胞能增强β-catenin的转录活性,并上调NOTUM的表达和分泌,同时增强了细胞的球体形成能力 (干性指标)。敲低FASN则产生相反效果,削弱β-catenin活性,降低NOTUM水平,并抑制干性。药理学抑制FASN不仅抑制了癌细胞的活力,还促进了分化标志物MUC2的表达,表明抑制FASN可能促使癌细胞从“干性”状态向分化状态转变。
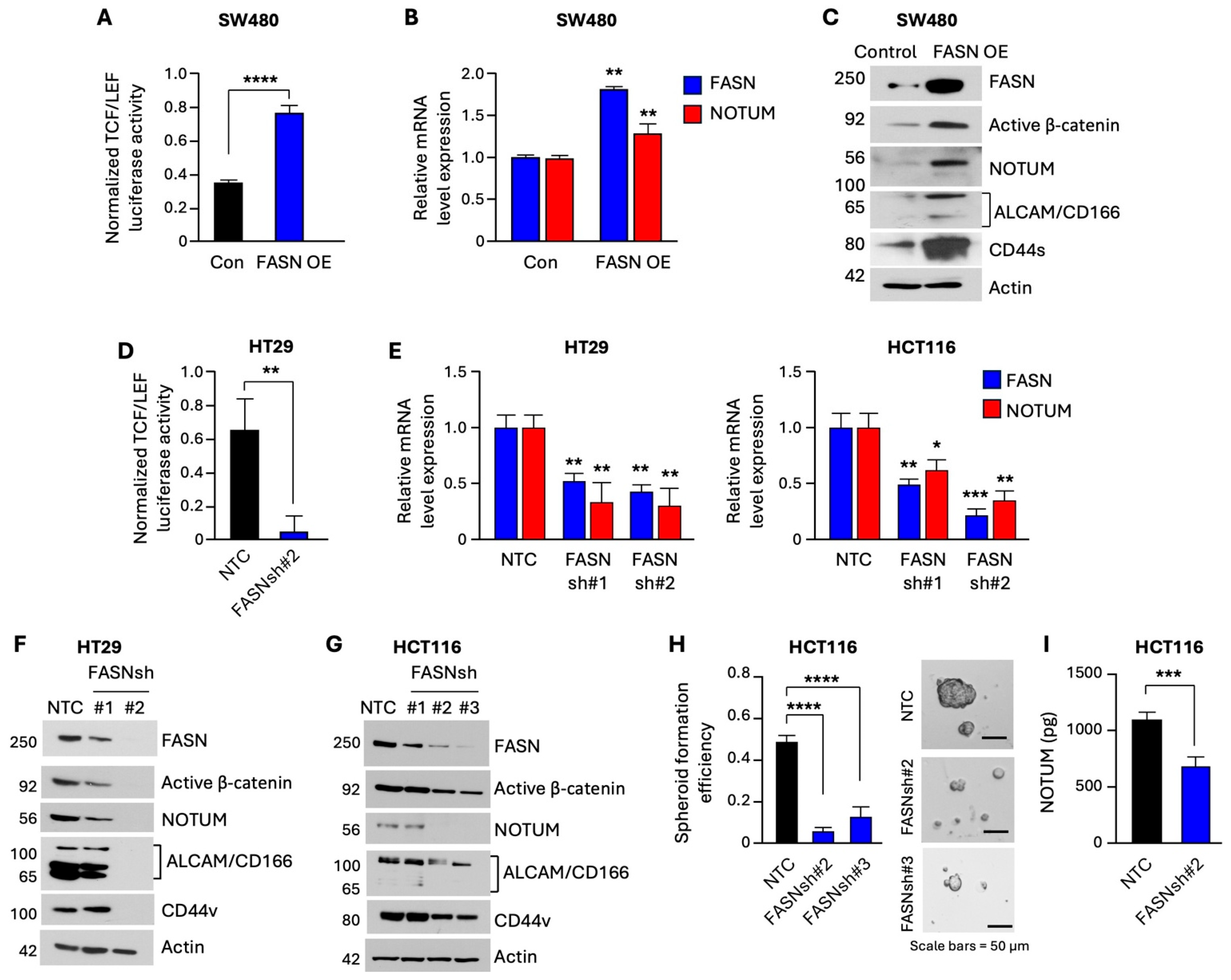
图4. FASN过表达增强β-catenin活性并提高NOTUM表达,从而促进结直肠癌干细胞特性。
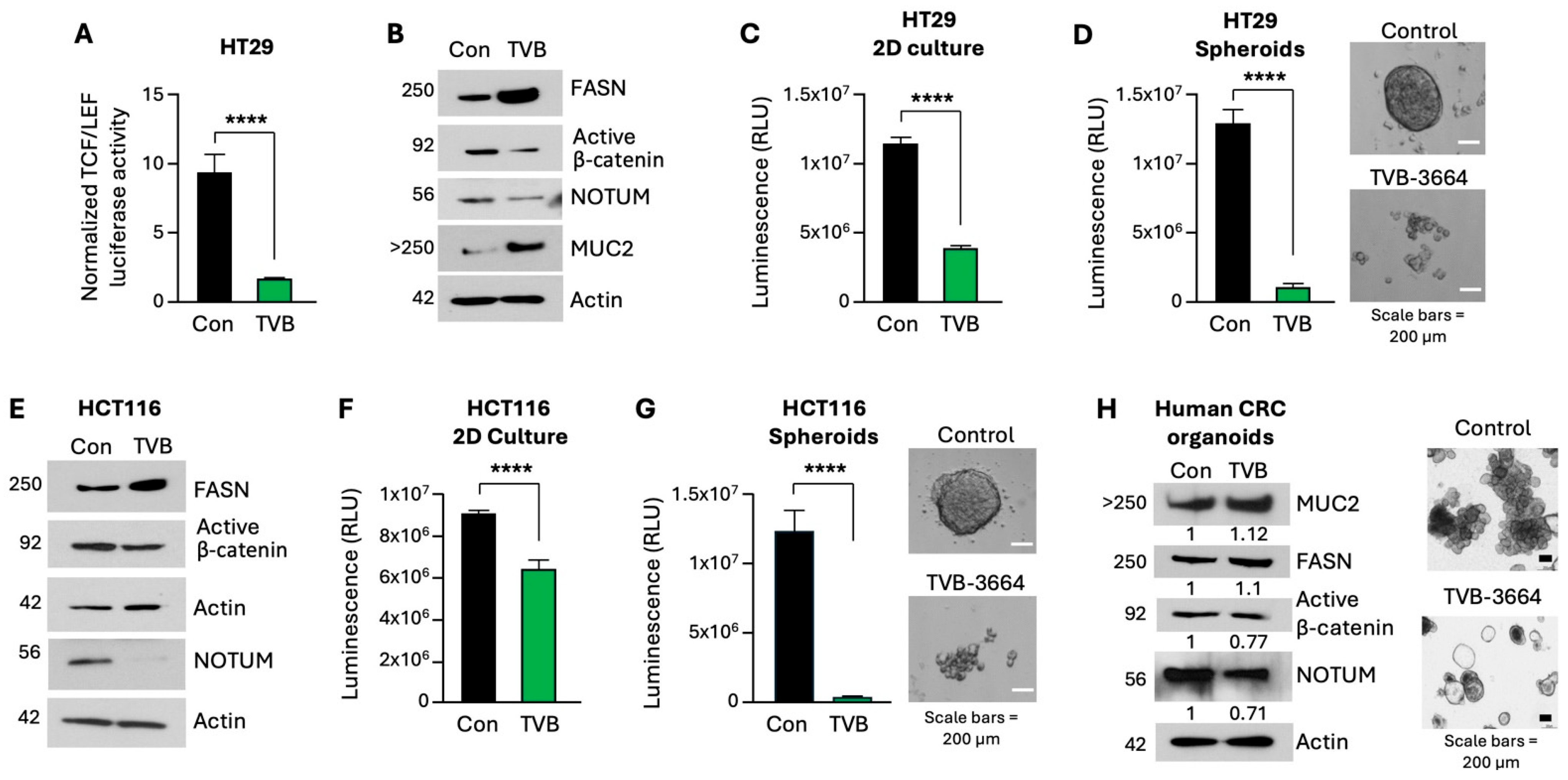
图5. 药理学抑制FASN可降低结直肠癌细胞中β-catenin活性、NOTUM表达水平及干细胞特性。
5.靶向β-catenin/NOTUM轴可有效抑制肿瘤生长
抑制β-catenin或直接抑制NOTUM (使用LP-922056或咖啡因),均能有效抑制腺瘤类器官和结直肠癌细胞的增殖与活力。这一发现尤其有趣,因为它将日常饮品中的咖啡因与一种潜在的抗癌机制联系起来,为未来的研究开辟了新思路。
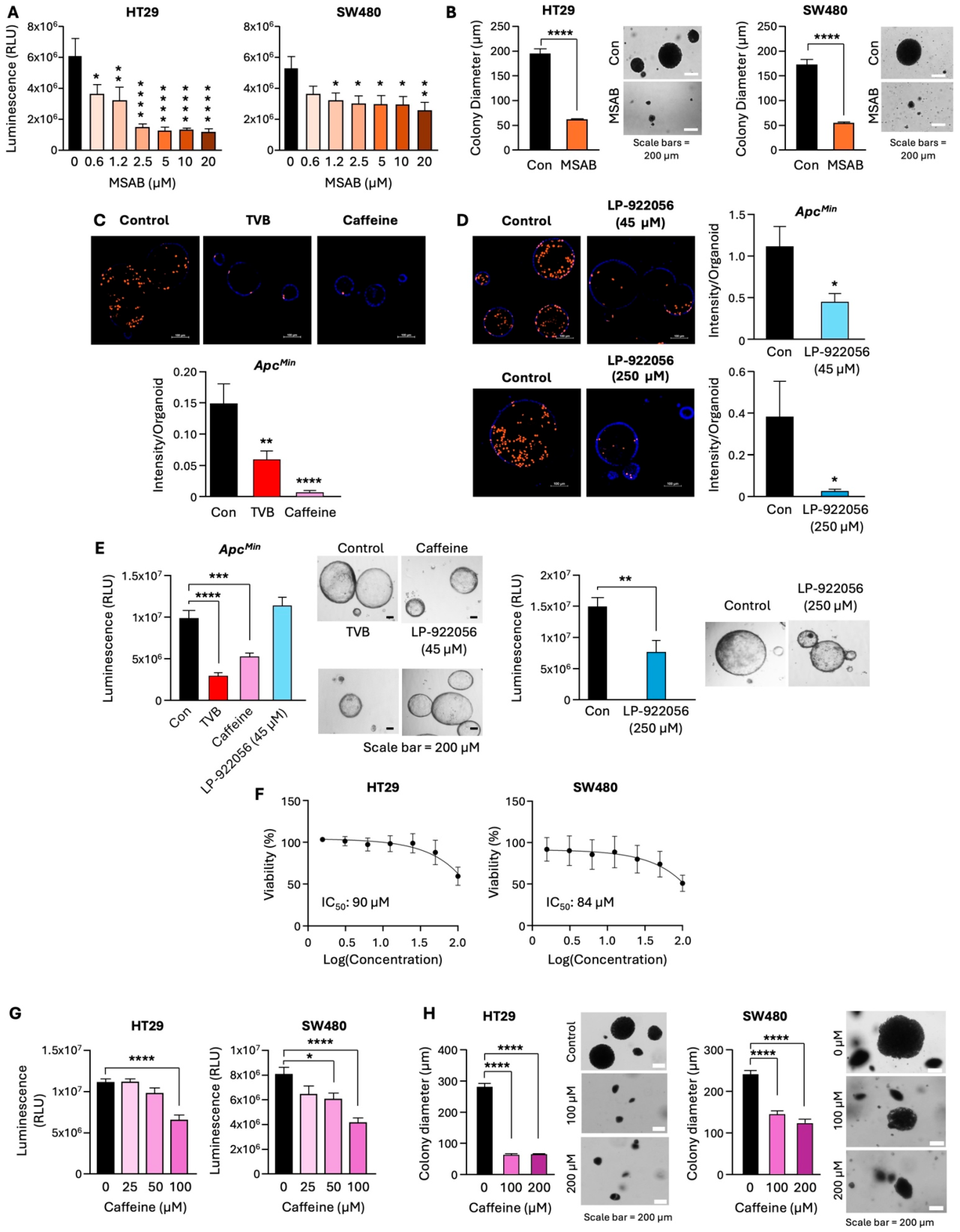
图6. 抑制β-catenin/NOTUM轴可降低结直肠癌的增殖能力。
研究总结
该研究明确了脂肪酸合成酶 (FASN) 与经典致癌通路 (Wnt/β-catenin) 及新兴靶点 (NOTUM) 之间的内在联系。同时该研究也提出靶向FASN可以作为上游干预策略,同时抑制β-catenin活性和NOTUM表达,从而削弱癌细胞干性。最后该研究还聚焦于预防,鉴于FASN在肿瘤早期就已上调,靶向FASN或其下游的β-catenin/NOTUM轴,可能成为针对高风险人群的一种极具前景的癌症预防性治疗策略。
阅读英文原文:https://www.mdpi.com/2073-4409/13/19/1663
Cells 期刊介绍
主编:Cord Brakebusch, The University of Copenhagen, Denmark; Alexander E. Kalyuzhny, University of Minnesota, USA
期刊涵盖细胞生物学、分子生物学和生物物理学等方面的研究。目前已被SCIE (Web of Science)、PubMed、MEDLINE、PMC等数据库收录。
2024 Impact Factor:5.2
2024 CiteScore:10.5
Time to First Decision:15.5 Days
Acceptance to Publication:2.8 Days
期刊主页:https://www.mdpi.com/journal/cells

https://blog.sciencenet.cn/blog-3516770-1525366.html
上一篇:2026 MDPI可持续发展大奖获奖者公布
下一篇:Nutrients南开大学胡耀中教授主持特刊:膳食营养素相互作用与免疫调节