博文
应变成像:将心外膜脂肪组织与心房重塑联系起来 | Hearts
||
心房颤动是一种常见的心律失常,受多因素机制的影响。左心房心外膜脂肪组织 (LA-EAT) 通过其内分泌和旁分泌活动,促进炎症、纤维化和电重塑,从而导致心房重塑。应变成像是早期检测心房功能障碍和心房颤动个性化治疗计划的重要工具。
发表在 Hearts 的一篇题为“Linking Epicardial Adipose Tissue to Atrial Remodeling: Clinical Implications of Strain Imaging”的综述探讨了LA-EAT与心房功能障碍之间的相互作用,强调了应变成像作为心房颤动治疗中诊断和预后工具的实用性。未来将这些成像方法纳入常规临床实践可优化心房颤动的治疗并改善患者的预后。
心外膜脂肪组织的组成和功能
心外膜脂肪组织 (EAT) 是一种独特的内脏脂肪库,位于心肌和心包内脏层之间 (图1),其成分包括脂肪细胞、炎症细胞、成纤维细胞和丰富的血管结构。EAT通过内分泌和旁分泌机制发挥作用,分泌生物活性分子,如脂肪因子 (如脂联素、瘦素)、细胞因子 (如白细胞介素-6、肿瘤坏死因子-α) 和趋化因子。虽然某些脂肪因子 (如脂联素) 具有保护心脏的作用,但发炎或扩张的EAT所分泌的大多数因子会产生一种促炎和促纤维化的环境。这种双重作用突显了它对心脏健康的重大影响,尤其是在房颤的发病机制中。
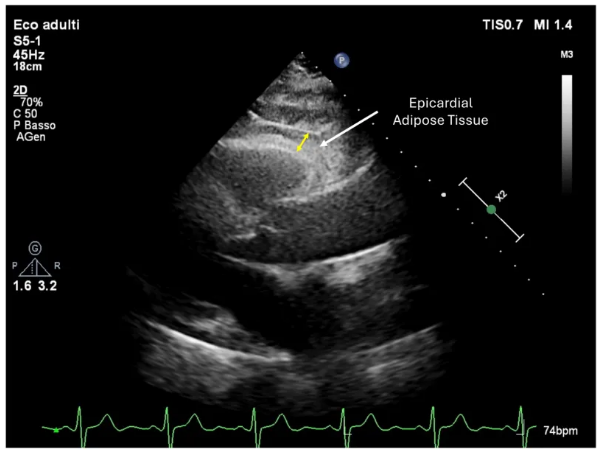
图1. 经胸超声心动图胸骨旁长轴切面显示EAT。黄色箭头表示EAT厚度。
左心房心外膜脂肪组织与心房颤动
左心房心外膜脂肪组织 (LA-EAT) 容量的增加与炎性细胞因子和氧化应激的分泌增加有关,从而促进了心律失常基质的形成。此外,LA-EAT还与心房纤维化和心房电重塑有关,这两者都是房颤的重要前兆。受衰老、肥胖或心血管疾病影响的局部心外膜或心内膜脂肪含量比全身脂肪含量更能预测心房颤动风险。
先前的研究表明,慢性肥胖导致广泛的双心房心内膜重塑,LA后心内膜电压降低,邻近的LA后心肌被心外膜脂肪浸润,为房颤的发生创造了独特的基质。
从机制上讲,EAT通过其内分泌活性和心肌细胞间的浸润促进结构重塑。它还环绕神经节丛,调节自律神经活动。反之,自律神经功能紊乱会改变EAT的内分泌活性,从而形成反馈回路。新出现的预防策略旨在通过减肥减少心外膜脂肪,或针对自律神经递质分泌降低房颤消融或手术后的复发率。
先进的成像技术
心脏计算机断层扫描 (图2)、心脏磁共振 (CMR) 和核医学技术为评估心房病理生理学和EAT提供了先进的成像功能。CMR具有高空间分辨率和晚期钆增强 (LGE),可对心房纤维化和EAT体积进行精确量化,通过直接观察结构重塑,补充超声心动图应变分析。核成像 (如使用18F-FDG示踪剂的正电子发射计算机断层显像) 可评估EAT的代谢活动和炎症情况。
在房颤合并纤维化的病例中,与正常心脏相比,心房脂肪含量最多可增加30-50%,纤维化组织占心房壁的10-25%,这在CMR中通过LGE可以识别。脂肪组织经常与纤维化共定位,为房颤的发展创造了结构和电基质。脂水分离和T1映射等CMR技术是量化这些异常的关键,可精确了解脂肪、纤维化和疾病严重程度之间的关系。
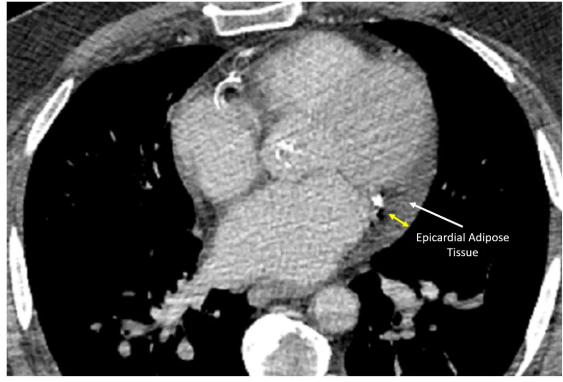
图2. 胸部计算机断层扫描显示心血管结构和EAT (箭头)。
结论和展望
应变成像、组织多普勒分析和容积评估的整合提高了识别和量化心房重塑的能力。这些方法有助于进行风险分层、指导治疗干预和监测针对LA-EAT的治疗效果。未来的研究应侧重于完善成像技术、优化治疗干预措施以及探索全身代谢因素与LA-EAT之间的相互作用。
原文出自 Hearts 期刊:https://www.mdpi.com/3151570
期刊主页:https://www.mdpi.com/journal/hearts
Hearts 期刊介绍
主编:Prof. Dr. Matthias Thielmann, University of Duisburg Essen, Germany
期刊研究领域涵盖基础、转化和临床研究,心血管医学创新科学所有领域以及相关学科。
Time to First Decision:18.6 Days
Acceptance to Publication:2.8 Days


https://blog.sciencenet.cn/blog-3516770-1479594.html
上一篇:四川农业大学李州教授团队——激活抗氧化防御、脯氨酸代谢及脱水基因表达调节白三叶交叉胁迫适应性 | Agronomy
下一篇:Entropy特刊征稿:信息和编码理论—分布式学习、存储、调度与安全
全部作者的精选博文
全部作者的其他最新博文
- • Metabolites 武汉纺织大学冯钰锜教授和朱泉霏教授主持特刊“质谱衍生化技术:解锁低丰度代谢组”
- • Nutrients:江苏大学陈震教授主持特刊"营养生物活性成分与脂质代谢疾病的综合探讨"
- • Processes:南京师范大学、西北工业大学、西安邮电大学学者共同创建特刊“电机及其驱动系统故障诊断与状态监测”
- • Electronics:西安交通大学、新疆大学、北京工业大学、西南交通大学学者共同创建特刊“下一代机器学习模型在状态监”
- • Cancers:苏州大学医学院程侠菊博士创建特刊"癌症治疗中的协同放疗和免疫疗法"
- • Information:重庆理工大学袁富江及其团队“联盟链PBFT共识算法的演化与优化策略”