博文
运动为什么能缓解“化疗痛”?复旦团队揭示外泌体跨血脑屏障镇痛新机制!  精选
精选
|
化疗诱导的周围神经病变(chemotherapy-induced peripheral neuropathy, CIPN)是肿瘤治疗中最常见、也最棘手的副作用之一。患者常出现手脚麻木、刺痛、感觉异常、平衡障碍,严重者甚至因疼痛和功能受限而影响后续治疗与生活质量。尽管临床上已认识到这一问题的重要性,但目前针对 CIPN 仍缺乏令人满意的干预手段。
近年来,越来越多研究提示,规律运动可能有助于缓解化疗相关神经毒性。已有系统综述和荟萃分析显示,运动干预在改善 CIPN 症状、减轻神经病理性疼痛、提升功能状态和生活质量方面具有积极作用。但一个关键问题始终没有被回答:运动究竟是通过什么分子机制发挥这种保护作用的?
近日,复旦大学陈世益/毛应启梁/罗智文教授团队在中国体育科学学会会刊《Sports Medicine and Health Sciences》发表论文《Exercise-induced circulating exosomes alleviate chemotherapy-induced 1 peripheral neuropathy through PHLDA1 blockade in microglia》。研究团队通过整合公共转录组数据、动物实验、细胞实验、小RNA测序和基因编辑等多层次证据,揭示了一个新的“运动-外泌体-miRNA-PHLDA1”调控轴:运动可通过循环外泌体将特定 miRNA 递送至脊髓小胶质细胞,抑制 PHLDA1 / NF-κB 介导的神经炎症,从而缓解化疗诱导的周围神经病变。
1、从“运动有用”到“为什么有用”
运动作为一种低成本、低风险、可推广的非药物干预手段,在肿瘤康复中的价值正在不断得到重视。既往临床研究已经提示,运动训练可在一定程度上预防或减轻 CIPN,但大多数证据仍停留在现象层面,关于其核心分子介质和靶细胞,仍缺乏清晰解释。
本研究的出发点,正是要回答这个机制空白:运动缓解 CIPN,究竟依赖什么“信号载体”?又作用于神经系统中的哪一类关键细胞?

表1 多项临床荟萃分析证实,多模式运动可有效改善化疗引起的周围神经病变(CIPN)症状。
2. 三大核心机制揭示“运动处方”镇痛密码
为此解决目前的空白,研究团队首先对多个公开的 CIPN 转录组数据集进行整合分析,筛选潜在关键分子,最终锁定PHLDA1作为一个值得重点关注的候选靶点。进一步结合 Human Protein Atlas 和单细胞资源分析发现,PHLDA1 在神经系统中具有明确表达,并在化疗相关病理状态下显著上调。
研究团队通过动物模型和单细胞测序等生物信息学分析,揭示了运动抗化疗痛的深层“纳米级”机制:
2.1 跨越血脑屏障的“纳米快递”:运动外泌体(Exo-E)
运动不仅是肌肉的收缩,更是全身器官的对话。研究发现,长期自主动轮跑运动会促使机体释放大量的血液循环外泌体(Exosomes)。这些直径仅为 30-150 纳米的微小囊泡,就像是坚固的“纳米快递车”,能够携带抗炎物质,成功穿透血脑屏障,精准进入脊髓背角,并被那里的中枢免疫细胞——小胶质细胞(Microglia)所吸收。

图1 运动诱导的血清外泌体(Exo-E)在电镜下的“纳米级”形态(左),及其成功跨越血脑屏障进入中枢神经系统的活体成像(右)。
2.2 精准投递“镇痛指令”:特定 miRNA 群
运动外泌体这个“快递车”里装了什么?通过对人类和动物运动后血清外泌体的深度测序,研究人员锁定了三个关键的“镇痛指令”:miR-122-5p、miR-181b-5p 和 miR-485-5p。化疗会导致脊髓中这些有益的微小RNA水平下降,而规律运动能显著提升它们在外泌体中的含量,并将其源源不断地输送给神经系统。
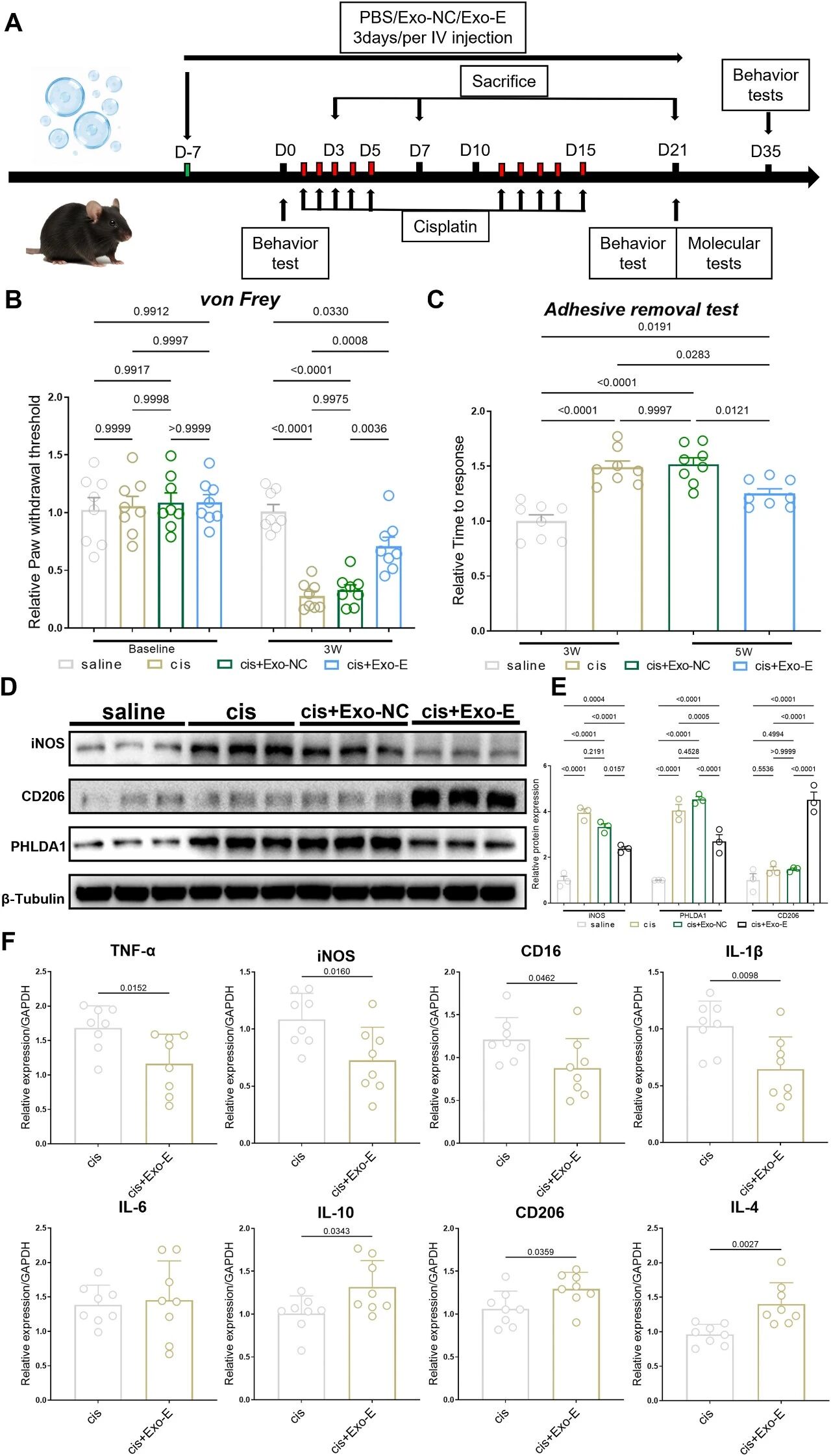
图2 动物实验证实,直接系统性注射“运动外泌体(Exo-E)”,即可成功模拟运动的益处,显著逆转顺铂化疗引发的神经病理性疼痛。
2.3 阻断神经炎症源头:PHLDA1 / NF-κB 通路
化疗药物(如顺铂)会异常激活小胶质细胞中的促炎基因PHLDA1,进而引发 NF-κB 炎症级联反应,释放大量 TNF-α、IL-6 等炎症因子,导致神经元过度兴奋和疼痛。
而运动外泌体运送来的特定 miRNA,能够精准“靶向并沉默”小胶质细胞中的 PHLDA1 基因。PHLDA1 被抑制后,NF-κB 炎症通路随之关闭,小胶质细胞从“促炎破坏态(M1)”恢复为“抗炎保护态(M2)”,减轻了炎症损伤。
这些分子事件相互交织,使运动不仅是“强身健体”,更是深层的“靶向基因治疗”。

图3 运动诱导的循环外泌体通过靶向抑制小胶质细胞PHLDA1基因,阻断神经炎症,从而缓解化疗痛的核心机制图。
小 结
化疗相关周围神经病变长期困扰着大量肿瘤患者,而运动作为一种安全、低成本、可推广的非药物干预方式,已经在康复实践中显示出价值。此次研究进一步揭示,运动可能通过循环外泌体携带特定 miRNA,跨越血脑屏障,靶向调控小胶质细胞中的 PHLDA1 / NF-κB 炎症通路,从而缓解化疗带来的神经损伤和疼痛。
这不仅让我们更深入地理解了“运动为何有效”,也为未来开发基于运动生物学效应的新型干预策略提供了启发。从“运动有益”到“机制可解”,这项工作为运动医学、神经免疫学与肿瘤康复的交叉研究提供了一个值得关注的新方向。
原文文献:
Mengran Xi, Renwen Wan, Wei Luo, Chunmeng Jiao, Hui Chen, Chieh-Ru Fu, Xinting Feng, Tianqi Wang, Xiaping Su, Shiyi Chen, Qi-Liang Mao-Ying, Zhiwen Luo. Exercise-induced circulating exosomes alleviate chemotherapy-induced peripheral neuropathy through PHLDA1 blockade in microglia. Sports Medicine and Health Science[J].2026, In Press.
https://doi.org/10.1016/j.smhs.2026.03.003.
https://blog.sciencenet.cn/blog-3496796-1528029.html
上一篇:Fundamental Research 张洳源、杨凌霄等:基于视觉皮层功能多样性的fMRI自然图像重构:连接神经科学
下一篇:Fundamental Research |董焕丽、高灿等:有机光电器件中三线态激子的调控与利用