博文
肠道菌群能导致自闭症的发生
||
肠道菌群能导致自闭症的发生
(胡敏 清华大学医学院)
2019年5月30日,美国著名学术期刊 Cell 发表题为“Human Gut Microbiota from Autism Spectrum Disorder Promote Behavioral Symptoms in Mice”的研究论文,文章证实自闭症患者来源的肠道菌群移植给无菌小鼠,无菌小鼠及其后代会出现自闭症的核心行为学表型,还会导致小鼠大脑中自闭症相关基因的可变剪接出现异常。微生物组及代谢组学分析指出,特定类型的微生物及其代谢产物是引发行为学异常的关键;部分代谢产物可明显改善自闭症小鼠模型的行为学异常并调节大脑的神经兴奋性。研究表明:肠道菌群可通过生成具有神经活性的代谢产物而调控小鼠的行为,提示肠-脑互作是自闭症发病和治疗的关键环节之一。
自闭症(Autism SpectrumDisorder,ASD)是一种发育障碍,其特征在于社交互动和沟通的困难,以及受限和重复的行为。在自闭症被命名之前很久就描述了一些自闭症症状和治疗的例子。马丁·路德(MartinLuther)在笔记本上记叙了一个可能患有严重自闭症的12岁男孩的故事。路德认为这个男孩是魔鬼所拥有的没有灵魂的肉体。一个在1798年被捕的野蛮孩子维克多,表现出自闭症的可能症状。
自闭症的症状是由大脑各种系统中与成熟相关的变化引起的。自闭症的发生方式尚不清楚。其机制可分为两个方面:脑结构的病理生理学和与孤独症相关的过程,以及大脑结构和行为之间的神经心理学联系。这些行为似乎有多种病理生理学。
有证据表明可能涉及肠-脑轴异常。2015年的一篇综述提出免疫失调,胃肠道炎症,自主神经系统功能障碍,肠道菌群改变和食物代谢产物可能导致脑神经炎症和功能障碍。2016年的一项综述得出结论,肠神经系统异常可能在自闭症等神经系统疾病中发挥作用。神经连接和免疫系统是一种可能允许来自肠道的疾病传播到大脑的途径。
有几个证据表明突触功能障碍是自闭症的原因。一些罕见的突变可能通过破坏某些突触途径(例如与细胞粘附有关的途径)导致自闭症。小鼠的基因替代研究表明,自闭症症状与后来的发育步骤密切相关,这些步骤依赖于突触活动和活动依赖性变化。所有与自闭症风险相关的已知致畸原(导致出生缺陷的药物)似乎在受孕后的前八周内起作用虽然这并不排除自闭症可能在以后发起或受影响的可能性,但有强有力的证据表明自闭症在发育的早期就会出现。

虽然早期研究已经发现自闭症患者的肠道菌群与正常个体间存在明显差异,但对肠道菌群与自闭症发病的因果关系缺少研究。考虑到自闭症是一种发育性疾病,其发病受孕期影响较大,本研究选取自闭症患者和正常个体的肠道菌群移植入无菌小鼠肠道中,对本体及其后代小鼠的行为学特征及组织样本进行分析。结果发现携带有自闭症患者肠道菌群的小鼠(统称ASD小鼠)表现出明显的类自闭症症状,其重复性行为增加且运动和交流能力减弱。由此可知,肠道菌群或是引起自闭症相关症状的重要因素。
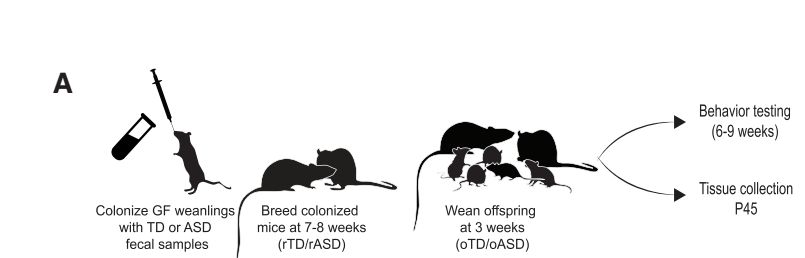
图1:实验流程:肠道菌群的移植、行为学检测及机制分析
为鉴别影响小鼠自闭症行为的关键菌种,研究者对自闭症患者的肠道菌群、移植小鼠及其后代的肠道菌群类别进行了系统分析,发现自闭症患者及ASD小鼠的肠道菌群与对照组有明显差异。其中,正常个体/小鼠中卵形拟杆菌(Bacteroides ovatus)和粪副拟杆菌(Parabacteroides merdae)有明显富集;而自闭症个体/小鼠中毛螺菌科的菌种(Lachnospiraceae)则明显多于对照组(图2)。随后的相关性分析指出,卵形拟杆菌和粪副拟杆菌与重复性行为的减少及社交行为的增加呈正相关;而毛螺菌科的菌种则恰好相反。综上研究可知,特定类型的肠道菌群或是引起自闭症相关症状的重要环节。
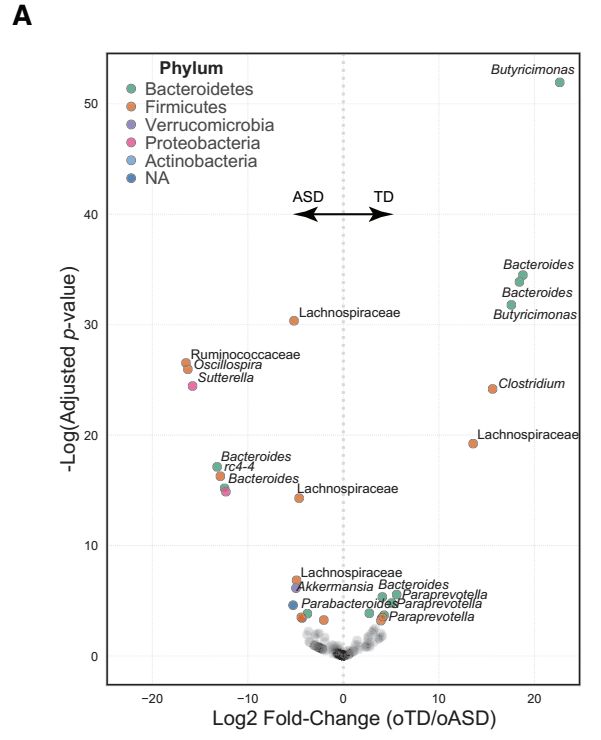
图2 :肠道菌群移植小鼠模型中有明显差异的菌种
自闭症核心症状的出现主要与大脑前额叶皮层(PFC)和纹状体的功能异常相关。为探究肠道菌群的改变对神经系统功能的影响,研究者对ASD小鼠大脑转录组进行了分析,发现除基因转录异常之外,基因的可变剪接也发生明显改变,这与自闭症患者大脑中基因可变剪接异常的表型相吻合;其中发生异常可变剪接的基因大多在神经元中高表达,且有52种基因是导致自闭症的重要候选基因。
位于肠道的菌群如何影响并不相邻的神经系统,考虑到代谢产物可随循环系统而实现远距离调控,研究者对ASD小鼠及其对照组的肠道/血液代谢组学特征进行了分析,发现有27种代谢产物在ASD小鼠的肠道中发生明显改变,其中包含多种GABA能受体及甘氨酸受体的激动剂/抑制剂,如GABA能受体激动剂5-氨基戊酸(5AV)和牛磺酸在ASD小鼠中的水平明显减少,这与自闭症患者中的结果一致;此外研究者还发现,甘氨酸受体激动剂3AIBA和多种生物活性分子如类黄酮、三羟基异黄酮和大豆甙元在ASD小鼠中的水平却明显增加(图3)。研究者注意到,与对照组相比,ASD小鼠肠道中的氨基酸水平有明显异常。为探究引发肠道氨基酸代谢异常的可能通路,研究者采用HUMAnN2和ShortBRED对代谢基因组学数据分析后指出,对照组小鼠肠道中,反式-4-羟基-L-脯氨酸经代谢产生中间产物P5C后进一步生成L-脯氨酸,最终促进5AV的产生;与之相反的是,ASD小鼠肠道中,反式-4-羟基-L-脯氨酸经代谢产生P5C后进一步生成谷氨酸,从而导致5AV水平下降。
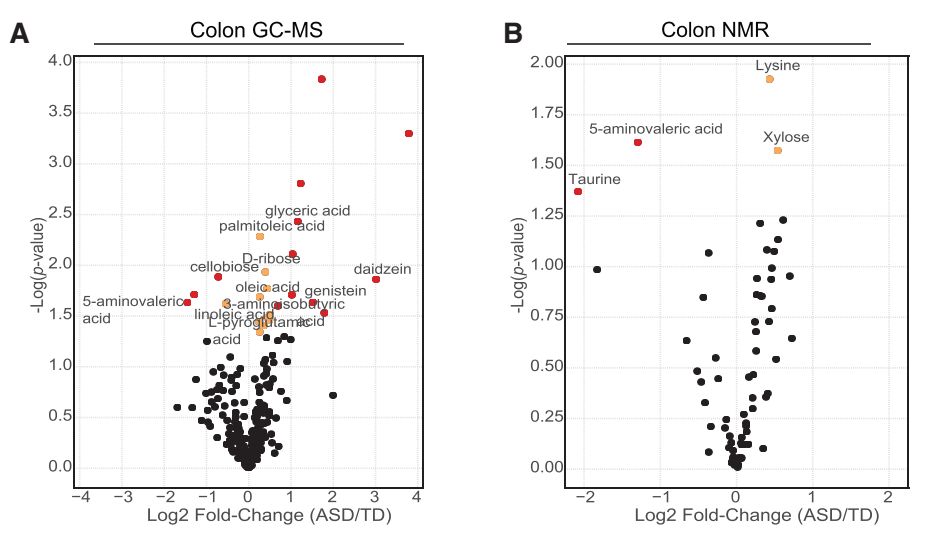
图3 肠道菌群移植小鼠模型肠道中的代谢组学改变
通过相关性分析,研究者发现,多种代谢产物与小鼠模型的行为学异常存在相关性;其中5AV和牛磺酸或具有保护性功能;三羟基异黄酮和大豆甙元则可能加重小鼠重复性行为;而三羟基异黄酮、3AIBA和赖氨酸则可能影响小鼠的运动能力。为验证5AV和牛磺酸对自闭症小鼠行为的保护效果,研究者选用BTBR小鼠(BTBR小鼠有自闭症的核心症状如社交减少和重复性行为)为模型进行后续实验。当BTBR小鼠自受孕开始口服牛磺酸至成年,其重复性行为明显减少,而社交行为明显增加;与牛磺酸类似,5AV同样能减少BTBR小鼠的重复性行为并改善其社交能力。研究还发现,孕期开始给予牛磺酸和5AV治疗至关重要,否则不能改善小鼠的行为异常。除改善行为学异常,研究者还发现,5AV能降低BTBR小鼠PFC中的神经元兴奋性,而牛磺酸则可调节皮层神经元应答GABA时的兴奋性-抑制性转变。由此可知,肠道菌群的代谢产物可影响神经系统电活动而调控小鼠的行为学改变。
本研究在早前肠道菌群与自闭症存在相关性的基础上,进一步证实肠道菌群与自闭症的发病及行为学异常之间存在直接的因果关系。机制及后续的治疗研究指出,特定肠道菌群的变化会改变肠道代谢,代谢产物的异常可能影响神经系统中基因的表达及可变剪接事件,最终导致行为学的异常。这一研究提示我们在探究基因组之外,分析肠道菌群,关注基因-环境互作或将为自闭症的机制探索和治疗提供了新的方向和维度。
https://doi.org/10.1016/j.cell.2019.05.004
参考文献
1. Baio, J., Wiggins, L., Christensen, D.L.,Maenner, M.J., Daniels, J., Warren, Z.,Kurzius-Spencer, M., Zahorodny, W.,Robinson Rosenberg, C., White, T., et al. (2018). Prevalence of Autism SpectrumDisorder Among Children Aged 8 Years - Autism and Developmental DisabilitiesMonitoring Network, 11 Sites, United States, 2014. MMWR Surveill. Summ. 67,1–23.
2. Gondalia, S.V., Palombo, E.A., Knowles, S.R.,Cox, S.B., Meyer, D., and Austin, D.W. (2012). Molecular characterisation ofgastrointestinal microbiota of children with autism (with and withoutgastrointestinal dysfunction) and their neurotypical siblings.Autism Res.5,419–427.
3. Hsiao, E.Y., McBride, S.W., Hsien, S., Sharon,G., Hyde, E.R., McCue, T., Codelli, J.A., Chow, J., Reisman, S.E., Petrosino,J.F., et al. (2013). Microbiota modulate behavioral and physiologicalabnormalities associated with neurodevelopmental disorders.Cell155,1451–1463.
4. Kang, D.-W., Adams, J.B., Gregory, A.C., Borody,T., Chittick, L., Fasano, A., Khoruts, A., Geis, E., Maldonado, J.,McDonough-Means, S., et al. (2017). Microbiota Transfer Therapy alters gutecosystem and improves gastrointestinal and autism symptoms: an open-labelstudy. Microbiome5, 10.
欢迎关注我的科普公众号“科学那些事儿”(Sciencers)

https://blog.sciencenet.cn/blog-3184854-1182518.html
上一篇:饶毅:睡眠的分子遗传学研究
下一篇:清华大学生医药博士学位答辩会