博文
[转载]峰回路转?
|||
精准医学前沿
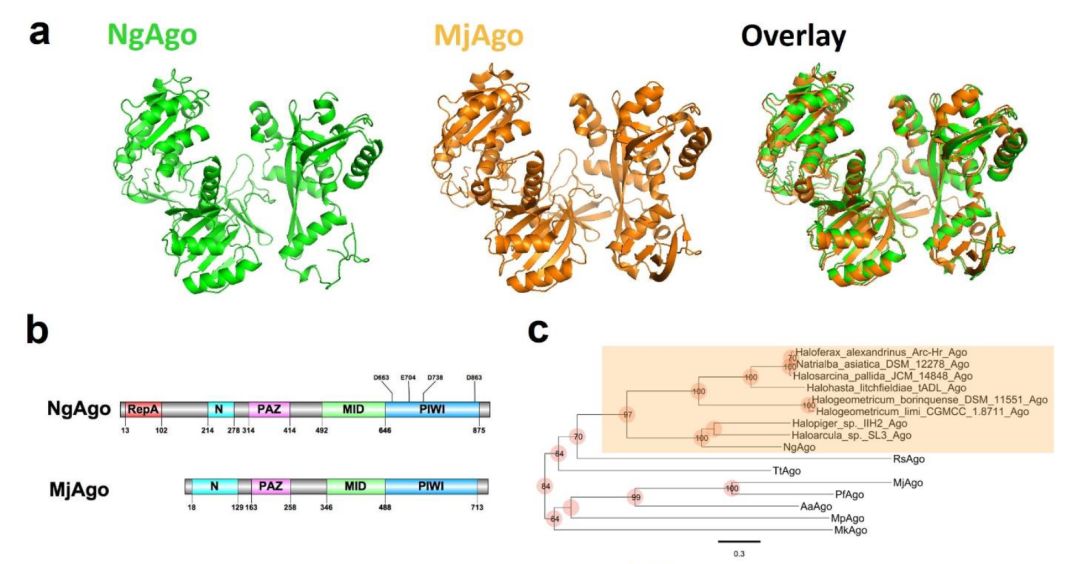
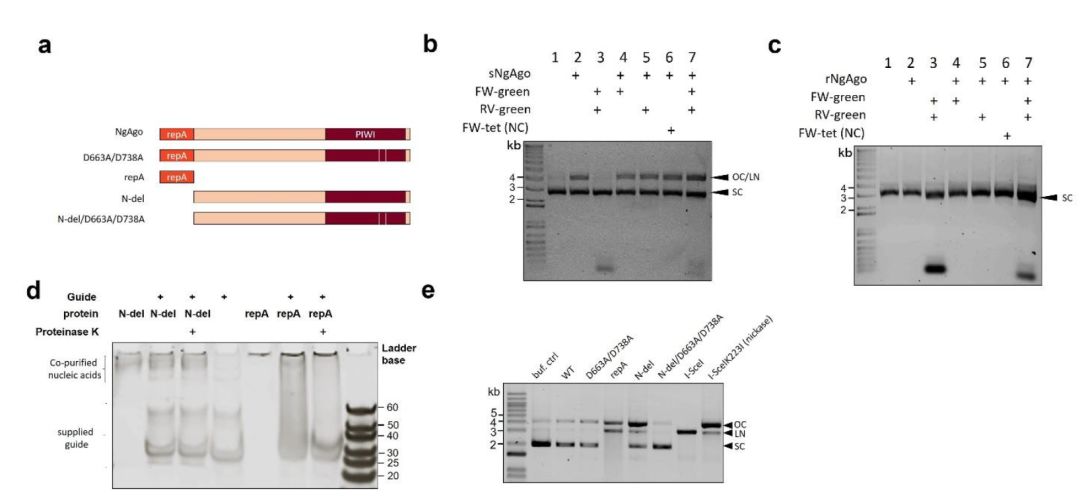
2016年5月2日,韩春雨(河北科技大学)作为通讯作者在 Nature Biotechnology 杂志发表了题为:DNA-guided genome editing using the Natronobacterium gregoryi Argonaute(使用NgAgo进行DNA引导的基因组编辑)的研究论文,该研究称NgAgo对真核生物(包括人)具有基因编辑能力。该研究很快在世界范围内爆火,随后引发广泛质疑,2017年8月3日,韩春雨撤回该论文。2018年8月31日,河北科技大学取消了韩春雨所获得的荣誉称号,终止了韩春雨团队承担的科研项目并收回了科研经费,收回了韩春雨团队所获校科研绩效奖励。 2019年4月4日,预印本网站BioRxiv刊登了一篇来自美国普渡大学研究人员的研究论文,表明NgAgo通过核酸内切酶活性介导增强大肠杆菌的同源重组。 该研究证实了NgAgo可以充当DNA内切核酸酶,还发现内切核酸酶活性对于增强大肠杆菌中NgAgo介导的同源重组或基因编辑是必需的。 论文题目:NgAgo-enhanced homologous recombination in E. coli is mediated by DNA endonuclease activity. 原核生物Argonautes(pAgos)已经被提出作为更灵活的基因编辑工具,与基于Cas9的基因编辑策略一样,单链核酸与pAgo结合并增强pAgo对互补靶核酸序列的切割,从而实现DNA修复和编辑。 pAgo不需要与其靶标相邻的基序序列就能行使功能,这与目前最流行的的CRISPR/Cas系统不同,因而具有切割任意DNA靶标的潜力。尽管有这种潜力和优势,但目前还没有开发出与Cas9基因编辑系统的简单性和功能性相媲美的pAgo基因编辑系统。 来自嗜盐古菌的NgAgo,是一个有前景的pAgo候选者,因为它被认为可以在37℃下工作,但是NgAgo到底能不能在真核生物中进行基因编辑产生了非常激烈的争论。 2019年1月22日,华中农业大学张安定、金梅林、韩丽,以及同济大学项耀祖合作,在 Nucleic Acids Research 杂志发表了题为:The prokaryotic Argonaute proteins enhance homology sequence-directed recombination in bacteria 的研究论文。 该研究表明,NgAgo可能仍然具有作为原核宿主基因编辑器的潜力,证实NgAgo的的基因编辑是通过RecA进行的同源重组介导的,而RecA与NgAgo以非预期的方式物理结合,但NgAgo的特定作用仍不清楚。 华中农业大学的研究表明:pAgo蛋白可以增强细菌中的同源序列定向重组 普渡大学的研究人员重新审视了这种NgAgo酶,并在原核生物中表征了其功能。NgAgo来源于嗜盐古菌,在非嗜盐宿主中表达很差,大部分蛋白质即使在重折叠后也不溶解和无活性。 NgAgo的结构 虽然之前的研究表明重折叠的NgAgo不能在体外切割DNA,普渡大学的这项研究表明可溶性NgAgo实际上可以在体外切割DNA。也就是说,重折叠的NgAgo可能无法完全发挥作用。 NgAgo能够在体外切割质粒 进一步研究表明,NgAgo能够在体内对大肠杆菌的进行基因组编辑。 NgAgo能够切割大肠杆菌基因组 repA和PIWI结构域均参与NgAgo的DNA切割活性。repA缺失、PIWI突变,均会降低NgAgo的切割活性,同时伴随着同源重组效率的降低。repA缺失和PIWI突变同时存在才会完全废除NgAgo的催化和基因编辑功能。因此,在repA和PIWI结构域两个功能结构域的存在下,NgAgo可以通过在靶向区域诱导双链断裂而有效地增强同源重组。 这些研究结果表明NgAgo确实是DNA内切核酸酶,NgAgo可溶性部分确实可以切割DNA。还发现这些内切核酸酶活性对于增强大肠杆菌中NgAgo引导的同源重组或基因编辑是必需的。 表明NgAgo具有重新用作DNA编辑工具的潜力。 尽管NgAgo具有可编程的DNA切割能力,但其想成为强大的基因编辑工具还存在许多挑战:高脱靶性、表达差、以及真核细胞中低活性等。 尽管如此,进一步的研究可能会通过蛋白质工程策略克服这些挑战,并开发NgAgo作为基因编辑的强大工具。 Kevin V Solomon,普渡大学农业与生物工程系助理教授。主要研究方向为:微生物与其环境相互作用,并重新编程这种反应,以有效地生产燃料,药物和其他增值化学品。 需要特别指出的是,华中农业大学和普渡大学的这两篇论文表明NgAgo对DNA有潜在的编辑能力,并未发现其对真核细胞有基因编辑能力(也就是不能证明韩春雨的研究可能正确),且普渡大学的这篇论文未经同行评议,直接发表于预印本网站BioRxiv。BioWorld如实解读该论文,至于论文结论严谨性与否,我们一起期待后续报道。 ----------------- 参见: https://www.biorxiv.org/content/10.1101/534206v2




https://www.biorxiv.org/content/10.1101/558684v1
https://www.biorxiv.org/content/10.1101/597237v1
https://blog.sciencenet.cn/blog-235-1173131.html
上一篇:事古人留迹