博文
血清磷对疾病和普通人群的潜在影响(1):回到基础
|
尽管磷是一种必需的营养素,但其过量可能通过多种参与细胞外磷内分泌调节的机制与组织损伤有关。高磷饮食对这些激素的无序调节可能是导致健康成年人肾功能衰竭、心血管疾病、癌症和骨质疏松症的关键因素,这是正在进行的研究中的重要问题。
1. 高磷血症是如何形成的?
1.1 食物来源
1.2 疾病因素
1.3 高磷血症的意义
2 健康与疾病中的磷酸盐代谢
2.1 循环中的磷与细胞外液(ECF)
2.2 Pi肠道吸收
2.3 Pi骨骼运输
2.4 Pi肌肉转运
2.5 Pi肾脏重吸收和尿液排泄
2.6 Pi的内分泌调节:FGF 23,PTH,1,25D
2.7 Pi与Ca代谢的相互作用
1. 高磷血症是如何形成的?
1.1 食物来源
出于几个原因限制磷的摄入似乎是合理的(富含磷的产品也富含钠、蛋白质、添加剂)。由于加工食品中的磷含量较高,高磷摄入量也可能反映生活方式、教育水平、文化问题等。这些变量在研究中没有普遍考虑。另一方面,坚果、豆类和鱼类等健康食品也富含磷【1】。磷存在于大多数食物中,与蛋白质含量密切相关,在美国,每克蛋白质摄入约15毫克磷。在食品标签、口服补充剂和药物中,磷含量通常不存在或缺乏记录。与化学分析相比,使用营养数据库对膳食磷含量的严重低估进一步加剧了这种不确定性。在美国饮食中,每天700毫克的推荐日摄入量(RDA)和每天580毫克的估计平均需求量(EAR)通常超过大约两倍(表1)【2】矿化和骨骼生长需要磷酸盐,许多不同的食物都含有磷,包括蔬菜、谷物、豆类、鸡蛋、鱼和肉类。此外,磷酸、磷酸钠和聚磷酸钠等磷酸盐添加剂存在于许多加工食品中。(图1)【3,4】。然而,研究表明,高磷摄入会抑制因低钙摄入而导致的血清1,25-二羟维生素D[1,25(OH)2D]浓度升高。此外,磷摄入可能是体内酸负荷的主要来源. 因此,高磷摄入是否会对骨量产生负面影响,而不是改善骨功能仍然是一个问题【3】。
Table 1 Phosphorus dietary daily intake in men/boys and women/girls and the RDA from the NHANES 2005–2006
From: Phosphate Metabolism in Health and Disease
Age(years) Men/boys (mg) Women/girls (mg) RDA (mg)
4-8 1147 1145 460
9-13 1321 1176 1250
14-18 1681 1067 1250
19-30 1656 1120 700
31-50 1727 1197 700
51-70 1492 1106 700
> 70 1270 985 700
骨骼健康取决于维生素和矿物质的饮食摄入(表2)【5】。三种主要的骨骼营养素是钙、磷和维生素D。在生长发育过程中,只有四分之一到三分之一的膳食钙被吸收,几乎全部储存在骨骼和牙齿中。相比之下,大约70%的膳食磷被吸收,吸收量取决于磷的类型:食物中有两种基本类型的磷:天然磷和添加磷,通常称为有机磷和无机磷,它们的吸收速率和吸收效率非常不同。天然磷或有机磷的吸收缓慢且效率较低(40–60%),而加工过程中添加到食品中的无机磷盐(用于保存或增强货架食品和一些烘焙食品)中的磷的吸收迅速且效率较高(80–100%)【6】。
表2。 成人肾病和非肾病患者维持骨稳态的饮食建议
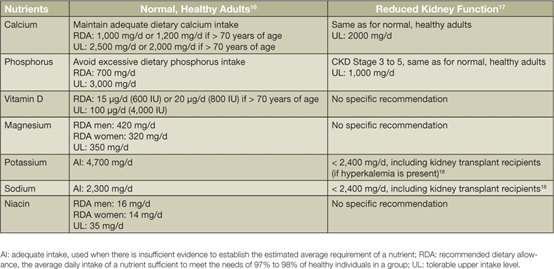
尽管磷是一种必需的营养素,但其过量可能通过多种参与细胞外磷内分泌调节的机制与组织损伤有关。高磷饮食对这些激素的无序调节可能是导致健康成年人肾功能衰竭、心血管疾病、癌症和骨质疏松症的关键因素,这是正在进行的研究中的重要问题【6】。
1.2 疾病因素
肾功能正常时,尿磷排泄量增加,与膳食摄入和胃肠道磷吸收无关,空腹血清磷保持在一个较窄的范围内。因此,由于尿液排泄减少而导致的血清磷酸盐升高是慢性肾病(CKD),晚期肾功能衰竭(ESRD)的主要表现(图1)【3,6】。
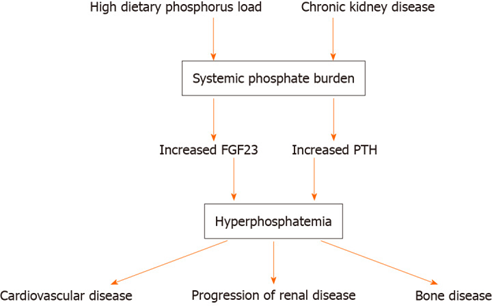
图1 高磷血症对不同器官/组织的影响
1.3 高磷血症的意义
多年前的实验研究表明,限制饮食中的磷酸盐可以防止肾功能不全的进展(图1),尽管高磷酸盐饮食会加重肾功能。血清磷与肾脏疾病进展之间的正相关性可能归因于急性磷负荷导致的内皮功能障碍延伸至肾小球内皮,以及磷诱导的钙化。另一个提出的潜在机制包括血清磷升高引起的足细胞损伤和大鼠垂体特异性正转录因子1(Pit-1)转运体的过度表达。成纤维细胞生长因子23(FGF23)是一种激素因子,在维持血清磷酸盐平衡中起重要作用。FGF23浓度从CKD早期开始逐渐增加,作为对血清磷酸盐稳态的生理适应。最终,FGF23浓度升高对这些患者的骨骼疾病起到了重要作用(图1和2)。ESRD发病率也与FGF23浓度增加有关。包括轻度CKD参与者在内的研究表明,与FGF23增加相结合,全因死亡率和进展为ESRD的风险更高。然而,有人提出FGF23、磷和CKD进展之间存在更复杂的关系,因为尽管调整了磷浓度,但这种关联仍保持稳定。考虑到磷的每日波动(图3),似乎血管钙化、内皮功能障碍、足细胞损伤和高FGF23会导致高血清磷导致肾脏疾病的进展。图 2.显示了与血清磷与肾功能不全进展之间关系相关的机制【3】。
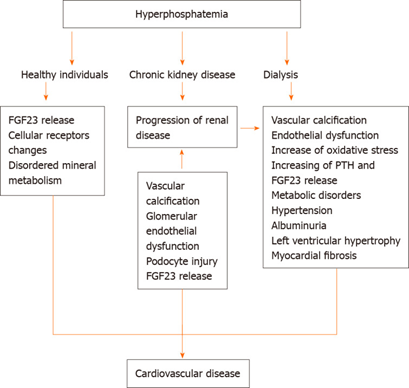
图2 不同人群中(健康群体CKD和透析)高磷血症的作用和病理生理学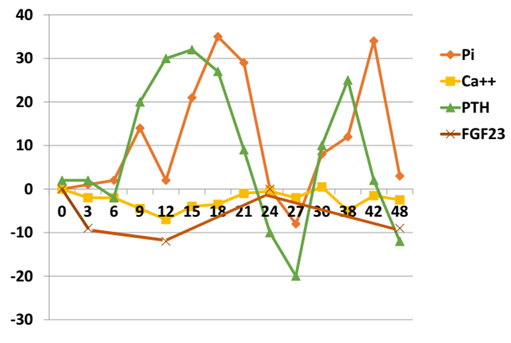
图3. 八名健康男性48小时内血清磷酸盐(Pi)、游离钙[Ca] + +] 、PTH、FGF23与基线相比的变化:血清Pi的范围为40%,而Ca为8% + +; FGF23的范围为10%,而PTH为50%。
1 健康与疾病中的磷酸盐代谢
2.1 循环中的磷与细胞外液(ECF)
循环和ECF负责Pi在参与磷酸盐(Pi)代谢的器官之间的运输(图4)。血浆中的磷含量约为12 mg/dL(3.87 mmol/L),其中约三分之一以无机磷(Pi)的形式存在。超过80%的血浆Pi是非蛋白质结合的,由三种质子化物种以及与钙、镁和钠的各种复合物组成。尽管血浆Pi约有20%与蛋白质结合,但由于道南膜效应(Donnan membrane effects),95%以上的Pi是可超滤的。因此,通常通过测量血浆中的总Pi浓度来评估Pi向肾小球滤液的转运【2】。
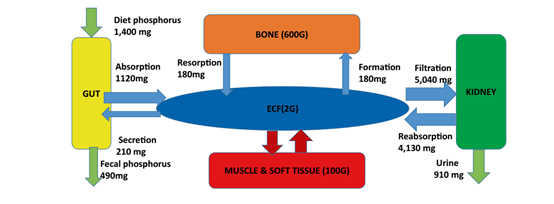
图4. Pi以毫克/24小时的速度从组织间转运。在1400毫克的膳食磷中,1120毫克的磷在上肠道被吸收到ECF,210毫克的磷通过内源性分泌返回到肠道,导致910毫克的净Pi吸收和490毫克的粪便排泄。在骨骼中,180 mg通过骨形成沉积,180 mg通过骨吸收返回ECF。在肾脏,5040 mg在肾小球过滤,4130 mg通过肾小管重吸收返回ECF,910 mg从尿液中排出。在软组织中,Pi在ECF和细胞之间交换。
成人血浆Pi的范围为2.5至4.5 mg/dl[0.81–1.45 mmol/L]。儿童的TmPi(tubular maximum reabsorptive capacity for Pi)较高,随着年龄的增长,从新生儿的约6 mg/100 mLGF逐渐降低到成人参考范围。男性和女性的成人参考范围相同,不受年龄的影响。循环中的Pi浓度是评估Pi代谢的重要指标。低磷血症和高磷血症总是反映潜在的疾病。急性低磷血症和高磷血症都是重症监护病房的常见症状,并导致重症患者的高发病率(表3)。慢性低磷血症导致肌肉骨骼疾病(表3)。它导致儿童骨矿化延迟,导致佝偻病,成人骨软化症,并导致近端肌肉无力,反映出Pi在骨骼肌化学能量转移中的关键作用。相比之下,慢性高磷血症表现为皮下、血管和神经组织中的软组织矿化(表3)。肾功能衰竭是慢性高磷血症最常见的原因,具有复杂的病理生理学。潜在的异常是ECF与磷酸钙的过度饱和,血浆总Pi x Ca浓度乘积已被用于估计这种风险【2】。
Table 3 与慢性低磷血症,急性低磷血症,高磷血症相关的条件和机制
Condition Mechanism
a: Chronic hypophosphatemia
Hyperparathyroidism: primary and secondary Decreased TmPi, increased PTH
X-linked hypophosphatemic Decreased TmPi, increased FGF 23
rickets/osteomalacia
Tumor-induced osteomalacia Decreased TmPi, increased FGF 23
Pi deficiency, oral Pi binders Decreased dietary & bioavailable Pi
Autosomal dominant hypophosphatemic Decreased TmPi, increased FGF 23
rickets/osteomalacia
Autosomal recessive hypophosphatemic Decreased TmPi, increased FGF 23
rickets/osteomalacia
Hypophosphatemic hypercalciuric kidney Decreased TmPi, decreased NaP2a & NHERF1
stones
Intravenous iron Decreased TmPi, increased FGF 23
Fibrous dysplasia Decreased TmPi, increased FGF 23
b: Acute hypophosphatemia
Alkalosis ECF & cell Pi redistribution
Carbohydrate infusion ECF & cell Pi redistribution
Insulin infusion ECF & cell Pi redistribution
Post-parathyroidectomy Increased net bone Pi accretion
‘hungry bone’ syndrome
Alcoholism ECF & cell Pi redistribution
c: Hyperphosphatemia
Chronic renal failure Decreased GFR, Pi retention
Hypoparathyroidism Low PTH, increase TmPi
Familial hyperphosphatemic Genetic mutations in FGF 23, Klotho, Galnt3
tumoral calcinosis
Rhabdomyolysis Massive muscle damage and Pi release
在ECF(包括血浆)中,磷酸盐经历三种命运之一:(1)主要通过肾脏清除,(2)运输到细胞中,或(3)沉积在骨骼或软组织中(图5)。有几种疾病与磷酸盐稳态失调有关,包括骨质疏松症、糖尿病、甲状旁腺功能亢进症、维生素D(高维生素和低维生素血症)和慢性肾病(表3)【4】。
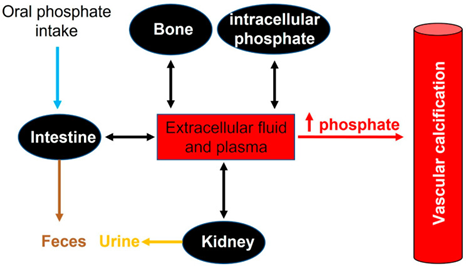
图5 磷酸盐平衡是一个复杂的过程,涉及骨肠吸收、膳食磷酸盐和肾脏磷酸盐排泄。
2.2 Pi肠道吸收
小肠有很大的Pi转运能力,并负责吸收大部分的膳食磷。吸收效率约为80%,约20%的吸收Pi作为内源性分泌物从ECF返回肠腔。吸收通过细胞旁扩散和活跃的、可饱和的跨细胞机制发生,这些机制在低磷摄入时起作用。由于膳食磷通常是过剩的需求,扩散在人类中占主导地位。然而,所有涉及的机制及其相对大小尚未完全阐明【2】。
细胞磷酸盐水平由磷酸钠共转运蛋白(NaPi)控制。磷酸钠共转运蛋白在人类临床疾病和生理过程中的作用尚未明确。主要确定了3个磷酸钠共转运蛋白家族,每个家族都有多个成员:I型(SLC17或NaPi-I),II型(也称为SLC34或NaPi II)和III型(SLC20或NaPi III),SCL34家族包括三个成员(也称为NaPi II),它们在小肠(NaPi IIb)(图6)和肾脏(NaPi IIa和NaPi IIc)中表达,这两个部位是控制磷酸盐稳态的两个重要部位。NaPi IIa主要表达于肾近端小管,在正常情况下,NaPi IIa是近端小管中负责95%磷酸盐重吸收的转运体。NaPi IIc的表达仅见于肾脏,并被描述为与生长相关。此外,SLC20溶质载体家族由Pit-1和Pit-2(III型磷酸钠共转运蛋白)表示(图6)。这两种共转运蛋白介导磷酸离子在细胞膜上的运动,每种细胞类型中Pit-1和Pit-2的表达水平不同【4】。
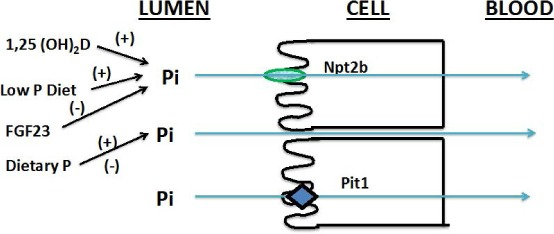
图 6。非钠依赖性磷酸盐转运蛋白2b(npt2b)和Pit1负责50%以上的磷酸盐吸收
已知Pi从肠腔到肠细胞的转运通过两个钠依赖性溶质载体家族进行。II型转运体NaPi2b[SLC34A2]积极跨细胞转运Pi。它存在于肠细胞的顶膜中,在低管腔浓度的Pi下发挥作用,其活性由1,25D/VDR调节。然而,这一途径在数量上的重要性仍不确定,因为人类SLC34A2的失活突变不会导致磷酸盐代谢的严重紊乱,尽管它们确实会导致肺泡磷酸钙微结石[23]。PiT1[SLC20A1]和PIT2[SLC20A2]也参与肠细胞对Pi的细胞内转运【2】。
另外两个因素需要强调,一种是服用大剂量骨化三醇或其类似物,已知其可增强小肠对活性磷酸盐的吸收。另一个因素是肠道游离磷酸盐浓度的降低,无论是通过饮食磷酸盐限制还是使用磷酸盐粘合剂,这是一种已知的促进小肠磷酸盐吸收的刺激因素。这两个重要因素阻碍了患者控制磷酸盐负荷的努力。所有这些考虑,尤其是最后的考虑,都导致研究者认为肠道活性磷酸盐转运是一种新的治疗靶点(图6)。在实验性肾功能衰竭和高磷血症的小鼠中,通过有条件地敲除小肠磷酸盐转运体NaP2b来纠正高磷血症,与sevelamer联合使用可减少被动磷酸盐吸收(图6)【5】。
最近,一种新型的肠道Na/H+交换抑制剂被证明在类似情况下可有效控制高磷血症。细胞旁Pi转运受肠细胞内质子浓度的调节,该浓度由钠氢交换器NHE3调节,NHE3由SCLC9A3编码。对特那帕诺(一种设计用于肠道局部作用的小分子)的研究表明,细胞旁途径是一种主要的肠道Pi转运机制,通过抑制NHE3的活性,替那帕诺减少钠向肠细胞的转运,并增加肠细胞中的质子浓度。细胞pH值的增加选择性地增加了细胞间紧密连接对Pi转运的抵抗力,并减少了Pi肠道吸收。对于肾功能衰竭和Pi潴留的患者,替那帕诺治疗可显著降低血清Pi。Pi吸收可通过放射性标记的吸收试验在人体内测量(图3)。它在许多疾病中降低,包括慢性肾功能衰竭、小肠吸收不良、维生素D缺乏性骨软化症、低磷血症性骨软化症,在原发性甲状旁腺功能亢进症和特发性肾结石形成中增加。在这些疾病中,Pi吸收分别反映了1,25D血清浓度的低和高,强调了125D/VDR在Pi吸收中的中心作用。小鼠肠道中的VDR敲除可将Pi吸收效率降低50%。然而,低膳食Pi摄入量对增加吸收的影响似乎与1,25D/VDR轴无关。FGF23对人体Pi吸收的影响主要是通过对1,25D分泌的主要影响间接产生的【2,7】。
2.3 Pi骨骼运输
骨骼是Pi的最大储存库,也是调节Pi转运的主要激素FGF 23的重要来源。骨矿物质Pi可与ECF Pi交换,但这种流量不利于ECF Pi内稳态(图5)。Pi在骨骼中有两种基本的运输途径。第一个涉及ECF-Pi进出骨的运输。第二个是Pi在骨内从成骨细胞向磷灰石晶体的运输。Pi从ECF到新骨形成和通过骨吸收回到ECF的每日净转运量小于肾脏和肠道(图4)。骨转换在骨和ECF之间传递Pi,并控制新骨的形成和多余或受损骨的再吸收。它可以促进骨骼生长、骨折修复和适应机械需求。由硬化蛋白途径调节的骨形成和由RANKL途径调节的骨吸收通常是紧密耦合的。在妊娠和哺乳等需要大量Pi和Ca在相对较长的时间内同时离开骨库的状态下,骨细胞周围的矿物质被认为通过一个名为溶骨性骨溶解的过程溶解,并通过小管进入ECF。一旦怀孕和哺乳期结束,这个过程就会逆转,耗尽的矿物质就会被完全替代。然而,并非所有的研究都证实发生了这种变化,溶骨性骨溶解的机制仍有待阐明。ECF-Pi浓度和Pi在骨中的内部运输对磷灰石的形成至关重要。ECF中的Pi浓度在一定程度上决定了Pi在骨细胞、负责维持骨健康的细胞、成骨细胞、负责骨形成的细胞和负责包裹骨组织的衬里细胞之间的传输速率。在严重的慢性低磷血症中,如发生在肿瘤诱导的骨软化、XLH]和维生素D缺乏的骨软化中,从ECF到矿化前沿的Pi降低到一定程度,以至于矿化率严重减慢,导致儿童佝偻病和成人骨软化症(表3)。在骨内,Pi也需要由成骨细胞生成和运输,以形成磷灰石。PiT1和Pit2调节活性Pi向骨细胞和骨细胞的转运。在成骨细胞中,Pi被运输到基质囊泡。基质囊泡含有孤儿磷酸酶1(PHOSPH1),这是一种生产Pi所必需的酶。大小约为200 nm的微泡被胞外释放到细胞外基质中,新生的无定形Ca–Pi晶体在其中聚集更多矿物质,形成成熟的磷灰石晶体。骨样基质液相对于Ca–Pi过饱和,一些抑制剂可以抑制不必要的矿化。碱性磷酸酶和外核苷酸焦磷酸酶磷酸二酯酶[ENPP1]调节类骨基质中关键抑制剂焦磷酸盐的浓度,同时调节Pi转运至基质囊泡的可用性。在缺乏磷酸酯酶1或碱性磷酸酶活性的情况下,骨骼无法以正常速率矿化,导致佝偻病和骨软化症,而在缺乏ENPP1的情况下,婴儿期会出现全身性动脉钙化。受金属内肽酶PEX调节的兄弟蛋白也是关键的晶体抑制剂,作用于多个部位,以防止在不需要的部位形成晶体,如骨细胞小管。因此,来自ECF的Pi供应不足或成骨细胞的Pi运输失败都会导致矿化缺陷,导致骨软化和佝偻病【2】。
2.4 Pi肌肉转运
随意肌不参与Pi的整体运输和代谢(图4)。之所以将其纳入本研究,是因为近端肌病是慢性低磷血症的一个显著特征,横纹肌溶解导致急性高磷血症。通过双x射线吸收仪(DXA)测量的男性肌肉重约为20 kg/m2,女性肌肉重约为15 kg/m2。由于其体积大,随意肌含有软组织磷的主要部分。主要以有机磷的形式存在,尤其是ATP和磷酸肌酐。肌肉中的细胞内游离Pi约为1–2 mg/dL[3–5 mmol][58],与ECF Pi呈线性相关。Pi向肌肉细胞的转运受Pit1和PIT2转运蛋白的调节。正常的ECF和肌肉细胞Pi浓度对于维持磷酸肌酐的储存和ATP作为肌肉机械活动能量来源的功能至关重要。维生素D缺乏性骨软化症和肿瘤诱导的骨软化症引起的肌病对治疗迅速反应,表明肌肉Pi供应受损是一个主要的病因【2】。
2.5 Pi肾脏重吸收和尿液排泄
肾脏处理每日Pi转运的主要部分(图4),也是调节Pi转运的关键激素1,25D(图7)的来源。肾小球滤过每24小时将超过5000 mg Pi输送至近端小管,近端小管将超过80%的Pi重新吸收回ECF(图4)。肾脏是控制血液循环中Pi浓度的主要器官。它通过肾小球滤过率(GFR)和近端小管对Pi的再吸收率来实现这一功能。由于TmPi较高,儿童的Pi浓度高于成人。随着GFR的降低,如慢性肾功能衰竭,Pi输送至近端小管的速率也相应降低。除非Pi肠道吸收代偿性减少,和/或Pi小管再吸收减少,和/或净组织Pi累积增加,否则循环中的Pi浓度不可避免地会升高。由于膳食磷通常过量,肠道无法弥补GFR的慢性下降。除生长期外,Pi在软组织和骨骼中的累积是有限的。因此,GFR降低的补偿主要取决于小管减少重吸收的能力。从肾滤液中重新吸收Pi的速率在很大程度上取决于2型磷酸钠共转运蛋白(NaPi2a/c)和3型磷酸钠共转运蛋白(PiT2)的活性(图7)。使用NaPi 2a特定抑制剂的研究表明,NaPi 2a起主要作用。Pi由包括XPR1在内的转运体从小管细胞分泌回ECF。近端小管是Pi再吸收的主要部位。它具有约2 mg/dL的Pi再吸收(TmPi)管最大容量,超过该容量,任何过滤Pi的增加都会在尿液中排出(图4)。有一个范围约为1 mg/100 mL GF的散斑,在达到完全TmPi之前,小管重吸收逐渐增加。临床上最好通过测量血浆Pi和血浆肌酐(Cr)以及在不超过1至2小时的适当时间间隔内收集的血液中收集的相应尿液Pi和尿液Cr来计算Pi的最大肾小管重吸收。不应使用24小时的时间间隔,因为血液中的Pi浓度在24小时内会发生显著变化(图3),从而导致不正确的低TmPi。在一夜禁食后收集血液和尿液,以减少饮食和GFR的可变影响,并优化个体的重复性。肾小管重吸收可表示为Pi排泄分数与肌酐清除率(血浆Pi)的关系 × 尿铬/血浆铬 × 尿(Pi)。由于GFR在表达TmPi的个体内部和个体之间存在差异,因此每单位肾小球滤过液(TmPi/GFR)提供了TmPi的估计值,可在个体内部和个体之间进行更准确的比较。根据健康受试者输注磷酸盐的数据,TmPi可以从列线图[71]或TmPi等方程中推导出来 = P − PE/1–0.1 loge(P/PE),其中Pi = 血浆磷脂酰肌醇 = 尿Pi x血浆Cr/尿Cr[63]。TmPi在新生儿中较高,并随着年龄的增长逐渐降低,直到青少年时期达到成人值。尿Pi可通过多种方式表达。作为Pi/Cr比率,它是TmPi计算的一部分。对于营养研究、代谢平衡研究和泌尿系结石形成风险的估计,使用24小时尿液收集中的Pi。在磷平衡的成年人中,24小时尿液Pi可提供膳食磷摄入量的估计值。在Pi正平衡的成长期儿童或摄入Pi粘合剂的受试者中,24小时尿Pi几乎可以降至零,但情况并非如此。24小时尿Pi仅与膳食钙摄入量呈弱正相关。然而,当摄入大量钙补充剂时,例如骨质疏松症或甲状旁腺机能减退症患者,钙作为Pi粘合剂,24小时尿Pi降低。在儿童中,在骨骼发育成熟之前,24小时尿Pi没有性别差异。此后,由于饮食Pi和GFR较高,男性的24小时绝对尿Pi高于女性,尽管他们的尿Pi/Cr比率相同。在评估肾结石形成的尿路风险因素时,24小时尿Pi作为一种浓度进行测量。在健康受试者中,Ca–Pi结晶尿是常见的,不会发生意外,反映了尿液pH值对Ca–Pi过饱和的主要影响。因此,尽管Pi是尿路结石的常见成分,但其存在依赖于pH值,并不反映Pi代谢异常。原发性甲状旁腺功能亢进症患者以磷酸钙结石为主,特发性结石病患者以草酸钙/磷酸钙混合结石为主,感染性尿液患者以磷酸铵镁结石为主。重要的是,Ca–Pi无论是作为集合小管中的晶体聚集体,还是作为肾乳头中的上皮下沉积物(Randall斑块),都是肾结石形成的关键部位【2】。
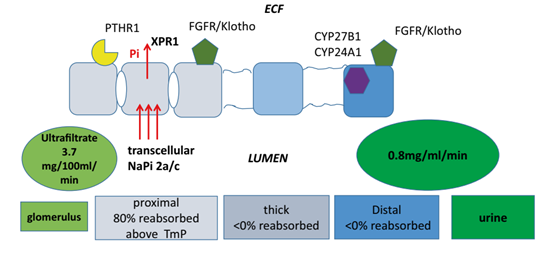
图7。大约80%的肾小球滤液磷酸盐[Pi]被近端小管中的跨细胞机制重新吸收。NaPi2a和NaPi2c调节Pi向小管细胞的转运,小管细胞通过细胞转运,并通过XPR1转运至ECF。近端小管有PTHR1和FGFR/Klotho受体。远端小管有FGFR/Klotho受体和酶CYP27B1和CYP24A1,负责将25-羟基维生素D代谢为1,25-二羟基维生素D和24,25-二羟基维生素D.
2.6 Pi的内分泌调节:FGF 23,PTH,1,25D
Pi代谢的内分泌调节是由三种激素,FGF 23、PTH和1,25D的高度综合作用实现的【8】。核心作用由骨细胞分泌的FGF 23发挥(图8)。ECF Pi浓度在数天内增加,但在数小时内没有急剧增加会上调FGF 23的分泌,进而通过近端小管中的FGFR/Klotho受体降低NaP2a和NaP2c的活性【9】。从腔液到ECF的跨细胞Pi转运减少,导致TmPi降低,ECF Pi降低。同时,肾脏1,25D产量下降,导致Pi肠道吸收减少。总体效果是预防高磷血症并维持正常的磷血症。相反,Pi ECF的减少会下调FGF 23的分泌,导致TmPi增加和Pi吸收增加。总的效果是预防低磷血症,维持正常磷酸血症(图8)。高Pi摄入导致FGF23的增加比低Pi摄入导致的增加更显著,这表明FGF23的主要功能是防止高磷血症和异位矿化。骨细胞感知ECF-Pi浓度的机制尚未建立【10】。它不涉及快速作用的正反馈回路,而是涉及ECF Pi的慢性(数天)变化。血清Pi的日变化与血清FGF23的增加无关,而血清Ca的日变化与血清PTH的变化呈负相关【11】(图3)。这种相对缓慢的正反馈回路响应可能存在于Pi传感机制中。骨细胞中的敲除研究表明,FGFR1可能是Pi感应机制的一部分,FGFR1被高浓度的Pi磷酸化【12】。此外,PiT 2和AMP活化激酶可能参与传感机制【13】。非激素刺激的FGF23分泌在低铁状态下发生(图8),其作用是将预分泌的FGF 23翻译后裂解为活性和非活性片段。这种O-糖基化调节的切割也可能参与对ECF Pi变化的相对缓慢的反应。
图8. ECF磷酸浓度[Pi]的增加刺激骨细胞分泌FGF23。增加的FGF 23作用于肾小管细胞,以减少磷酸盐重吸收[TmPi]和ECF Pi,并减少1,25二羟基维生素D[1,25D]和Pi的肠道吸收。循环Pi浓度降低[Pi]会减少FGF23的分泌,从而增加TmPi和125D的分泌。非内分泌机制导致的低铁状态增加FGF 23的分泌
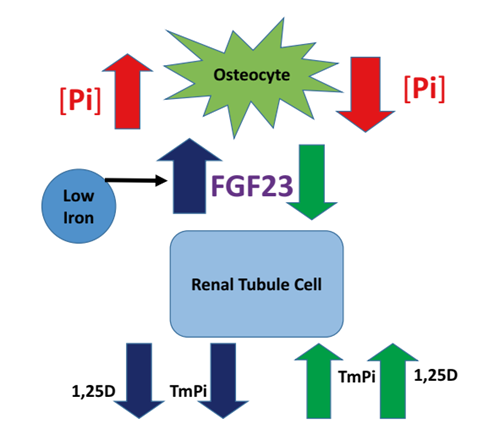
图8. ECF磷酸浓度[Pi]的增加刺激骨细胞分泌FGF23。增加的FGF 23作用于肾小管细胞,以减少磷酸盐重吸收[TmPi]和ECF Pi,并减少1,25二羟基维生素D[1,25D]和Pi的肠道吸收。循环Pi浓度降低[Pi]会减少FGF23的分泌,从而增加TmPi和125D的分泌。非内分泌机制导致的低铁状态增加FGF 23的分泌
临床上,铁状态对慢性肾衰竭等常见疾病的FGF23分泌有重要影响【14】。虽然FGF23调节Pi代谢,PTH和1,25D调节Pi和Ca代谢,但Pi ECF浓度并不直接影响PTH分泌,尽管高膳食磷摄入,口服Pi补充剂[72]通过降低ECF Ca浓度来间接影响PTH分泌。FGF 23和PTH都通过NaPi2a和NaPi2c降低TmPi,但与FGF 23减少1,25D分泌相比,PTH增加1,25D分泌(图8)。因此,这三种激素作为一个高度整合的激素轴发挥作用,旨在维持Pi和Ca代谢以及骨矿物质库。此外,这三种激素能够在体外和体内动物模型中调节彼此的分泌。FGF23减少PTH分泌,1,25D减少PTH分泌并增加FGF 23分泌,PTH增加FGF 23分泌【15】(图9)。这些后一种途径在正常生理学和疾病病理生理学中的相对重要性仍需阐明。应该注意的是,严重的磷酸盐消耗导致的低磷血症与低FGF23相关,导致高TmPi和1,25D,以及低PTH。另一方面,由于疾病(如TIO和XLH中FGF 23分泌的原发性增加而导致的低磷血症具有较低的TmPi、1,25D和较高的正常PTH【2】。
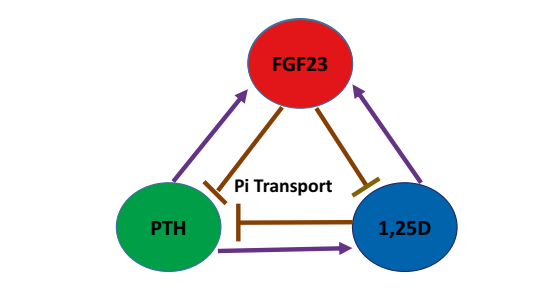
图9. FGF 23、PTH和1,25D作为一个高度整合的激素轴发挥作用,维持Pi和Ca代谢,并调节骨骼中的Pi和Ca储存
2.7 Pi与Ca代谢的相互作用
Pi和Ca的代谢并不是孤立地进行的。它们在ECF、肠道、骨骼和肾脏的转运机制中密切相互作用。此外,Pi和Ca的ECF浓度变化独立调节维持Pi和Ca稳态的激素、FGF 23、PTH和1,25D的分泌。在ECF中,八磷酸钙过饱和导致软组织矿化,而饱和不足导致骨脱矿。健康的骨形成需要来自ECF的Pi和Ca的必要供应,当骨再吸收时,Pi和Ca一起释放到ECF中的量等于它们在磷灰石中的3/5摩尔比。在饮食中,Pi和Ca密切相关。乳制品是膳食Pi和Ca的主要来源。母乳供应约150 mg Pi和180 mg Ca/100 g,与酪蛋白结合形成牛奶胶束,对生长中的婴儿来说是一种高度可吸收的供应。另一方面,钙补充剂的大量摄入显著降低了膳食Pi的生物利用度,钙补充剂在治疗慢性肾功能衰竭和甲状旁腺功能减退症时用于降低ECF Pi浓度增加的相互作用。相比之下,为治疗低磷血症而摄入的大量Pi补充剂会损害钙吸收,降低循环ECF-Ca,并导致继发性甲状旁腺功能亢进。在肾脏,即使在没有PTH的情况下,Ca-ECF浓度的增加也会降低TmPi,而在尿液中,Ca-Pi过饱和会增加结石形成的风险。Pi和Ca之间的这些多重相互作用强调,在健康或疾病中,Pi代谢不能完全独立于Ca代谢【2,16】。
影响钙生物利用度的营养和健康因素:参考 https://blog.sciencenet.cn/blog-526326-1321905.html
主要参考文献
Nutrients. 2021 Feb 27;13(3):789.
Calcif Tissue Int. 2021 Jan;108(1):3-15.
World J Nephrol. 2021 Sep 25;10(5):76-87
Int J Mol Sci. 2021 Dec 17;22(24):13536
Methodist Debakey Cardiovasc J Oct-Dec 2016;12(4 Suppl):6-9.
Adv Nutr 2015 Nov 13;6(6):860-2.
Kidney Med. 2021 Aug 27;3(6):1057-1064.
8. Rev Endocr Metab Disord 2015,16:165–174
9. J Bone Miner Metab 2007,25:419–422
10. Clin Nephrol 2013,79:57–65
11. Nephrol Dial Transplant 2014,29:385–392
12. Proc Natl Acad Sci USA 2019,116:11418–11427
13. Kidney Int 2018,94:491–501
14. Curr Opin Nephrol Hypertens 2014,23:411–419
15. Bone 2011, 49:636–643
16. Clin J Am Soc Nephrol 2010,5(Suppl 1):S23–30
https://blog.sciencenet.cn/blog-526326-1325776.html
上一篇:图游济南(3):夜游月牙泉
下一篇:为学日益 ,为道日损