博文
Cell 重磅丨不依赖泛素蛋白酶降解途径的新型 PROTAC - MCE
|
上述分子的体现了降解剂的结构与应用类型的丰富性,但降解剂类分子的合理设计与不断优化以及活性检测仍有很长的路要走。
“钟” 模型与协同效应
前文我们已经介绍过,PROTAC 分子的设计之初,靶蛋白配体、E3 连接酶配体和两者中间的连接子三者应该分别考量。
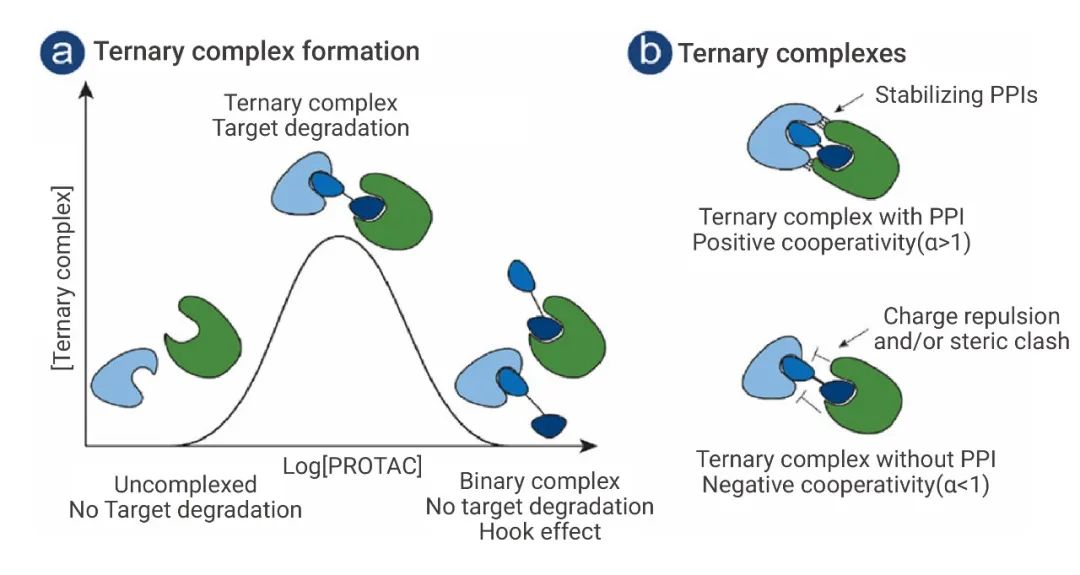
在 PROTAC 介导的蛋白降解途径中,其中靶标配体 (POI)-PROTAC-E3 连接酶等三元复合物的有效形成同样起到重要作用。三元复合物的任一单元的浓度改变带来的不仅仅是线性变化,“钟” 形模型常常被用来解释这样的活性与浓度相关性,文献中提及的 hook effect 也正是形容这种情形。
另外,在活性研究中,协同效应 (cooperativity, α) 这一词汇,被用于解释 PROTAC 受 POI 与 E3 连接酶配体间蛋白蛋白相互作用 (PPI) 的影响。当 α 大于 1 时,POI 和 E3 是正协同效应,对三元复合物的形成有利。
图 1. PROTAC 降解能力的“钟”形模型与协同效应示意图[1]
不依赖泛素蛋白酶的降解体系
1. 依赖溶酶体途径的降解类分子
PROTAC 主要依赖泛素-蛋白酶体途径,其对应降解的大多为胞质蛋白与核蛋白。Bertozzi 教授的研究团队报道了一项靶向胞外蛋白的降解技术——溶酶体靶向嵌合体 (LYTAC)。已证明 LYTAC 成功降解了表皮生长因子受体 (EGFR)、程序性死亡配体 1 (PD-L1) 等膜上蛋白。
对于细胞中一些非蛋白成分,Targeting lipid droplets for autophagic degradation by ATTEC 一文展示了一种通过自噬束缚化合物 (ATTECs) 降解非蛋白质生物分子的新策略,使用脂滴作为示例靶标并成功降解。
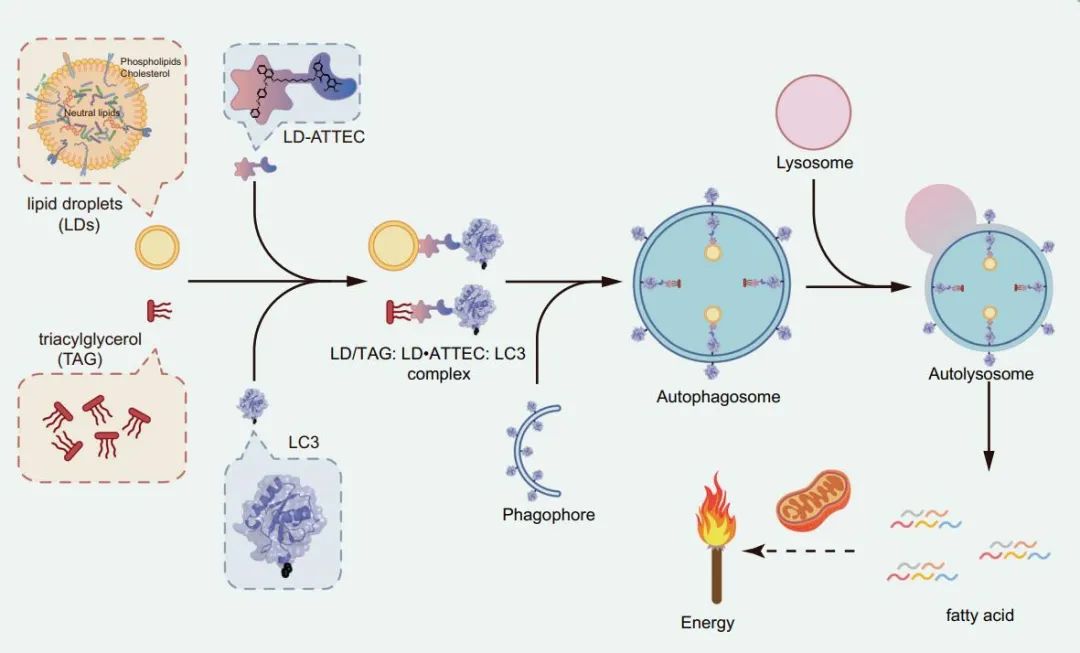
图 2. ATTECs 对脂滴的降解[5]
LD·ATTECs 通过疏水作用与 LD 以及自噬体蛋白 LC3 结合,形成LD/TAG LD·ATTEC LC3三元复合物,复合物与自噬体溶酶体融合并最终被自噬体降解。
但不论是 PROTAC 还是上述其他方式,它们都靶向真核生物细胞内物质的降解,均不能在细菌和其他原核生物中发挥功能。
2. 依赖 ClpCP 酶的 BacPROTAC
今年 6 月,Morreale 团队等人在 Cell 发表的 BacPROTACs mediate targeted protein degradation in bacteria 一文报道了一种用于革兰氏阳性菌和分枝杆菌靶向蛋白降解的创新技术,BacPROTAC。
他们基于 Clausen 实验室之前的一项发现:在枯草芽孢杆菌和其他革兰氏阳性菌中,AAA 去折叠酶 ClpC 和蛋白酶 ClpP 组成的 ClpC–ClpP (ClpCP) 蛋白酶是降解细菌中未折叠和聚集蛋白质的重要蛋白水解酶。由于磷酸精氨酸的对接位点位于 ClpC ATP 酶的氨基末端结构域,磷酸精氨酸 (pArg) 可作为 ClpCP 蛋白酶复合体的降解标签。
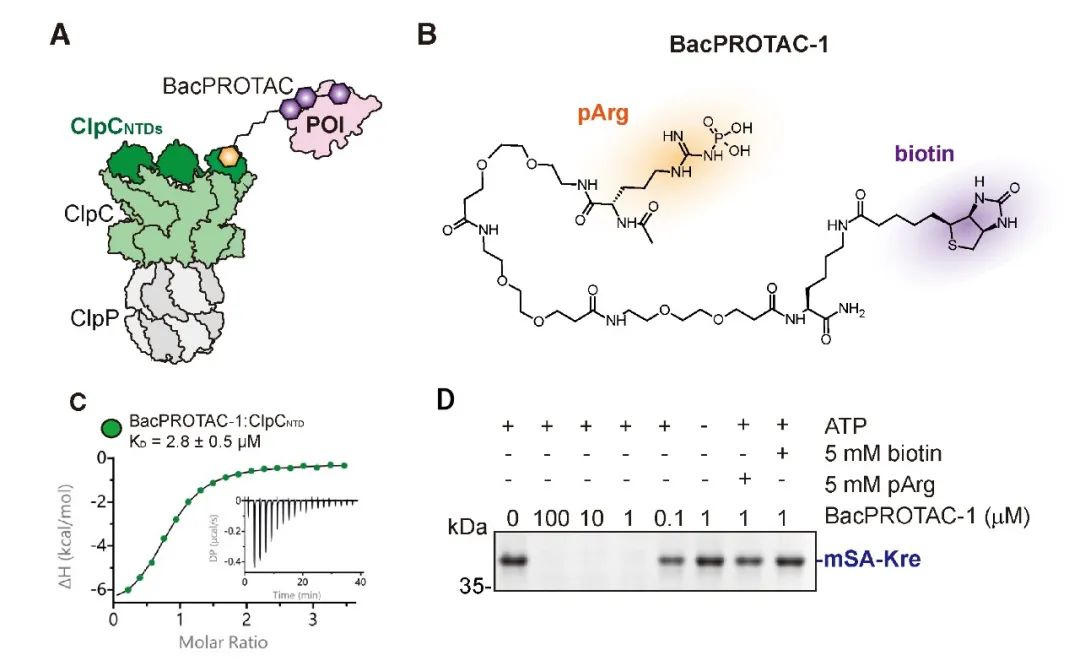
Morreale 等人报道的细菌 PROTACs (BacPROTACs) 由 POI 配体、Linker 和 ClpCNTDs 配体组成,可诱导细菌这种没有泛素蛋白酶体的非真核生物蛋白的体内外降解。如图 3A,研究团队在体外首先以单体链霉亲和素 (mSA) 作为模型蛋白,通过 BacPROTAC 将 pArg (ClpCNTD 配体) 与生物素 (mSA 的配体) 结合,形成 BacPROTAC-1 三元复合物,有效降解靶蛋白。BacPROTAC-1 与 mSA 和 ClpCNTD 结合的 KD 为 3.9 和 2.8 μM (如图 3C)。
图 3. BacPROTAC-1 对枯草芽孢杆菌 ClpCP 的体外重编程[6]
由于磷精氨酸的化学稳定性等方面存在问题,在体内的应用有限。作者团队将内源性的磷酸化精氨酸残基 (pArg) 换成了高选择性的 sCym-1。sCym-1 不但可以和枯草芽孢杆菌的 ClpCP 结合,还可以与分歧杆菌的 ClpC1P1P2 结合。
图 4. BacPROTACs 对分枝杆菌 ClpC1P1P2 进行重编程[6]
由于细胞生物素会竞争性与 mSA 结合,一定程度上阻碍 BacPROTAC 活性 (图 5),作者团队确定以 Bromodomain-1 (BD1) 作为更吸引人的模型底物,并将 JQ1 作为新的POI配体,天然环素 dCymM 作为 ClpCNTD 结合基团。BacPROTACs 以浓度依赖性的方式促进 BRDTBD1 的降解。
图 5. BacPROTACs 可以对分枝杆菌 ClpC1P1P2 进行重编程[6]
上:BRDTBD1-directed BacPROTACs: 通过不同的 Linker 和连接位点连接 JQ1 到dCymM。下:分枝杆菌 ClpC1P1P2 与 BD1 孵育后降解的 SDS-PAGE 分析。
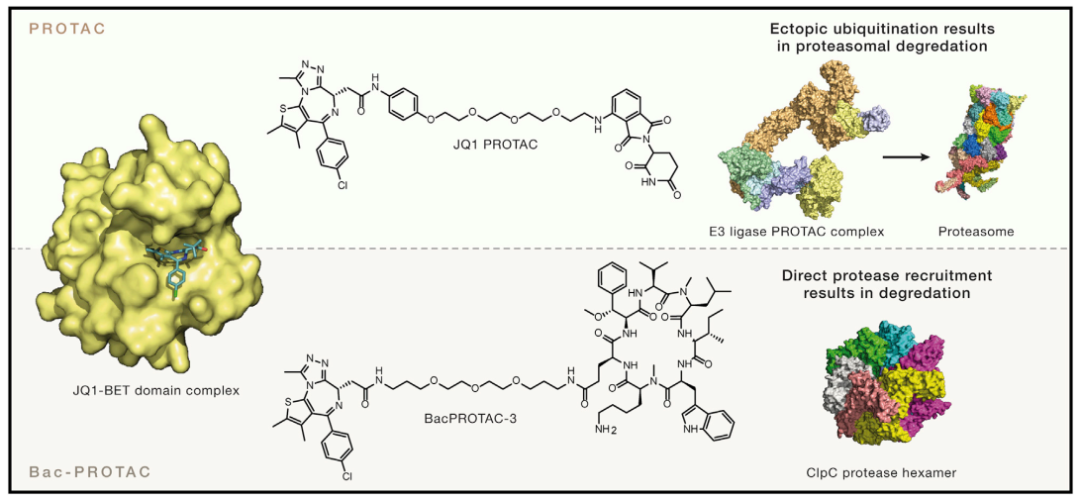
总之,如图 6 所示:PROTACs 通过招募 E3 连接酶来诱导蛋白质降解,E3 连接酶使得靶蛋白贴上泛素化标签,最后蛋白酶体降解泛素化的蛋白质。
BacPROTACs 以高度特异的方式将细菌 ClpCP 蛋白酶定向到底物上,它不但可以诱导底物和蛋白酶之间的接近,并且通过结合诱导无活性的 ClpCP 十聚体重组为有活性的六聚体形式,直接启动 ClpCP 水解靶标蛋白。
图 6. 蛋白质降解的异双功能方法[5]
没有 Linker 的降解剂?
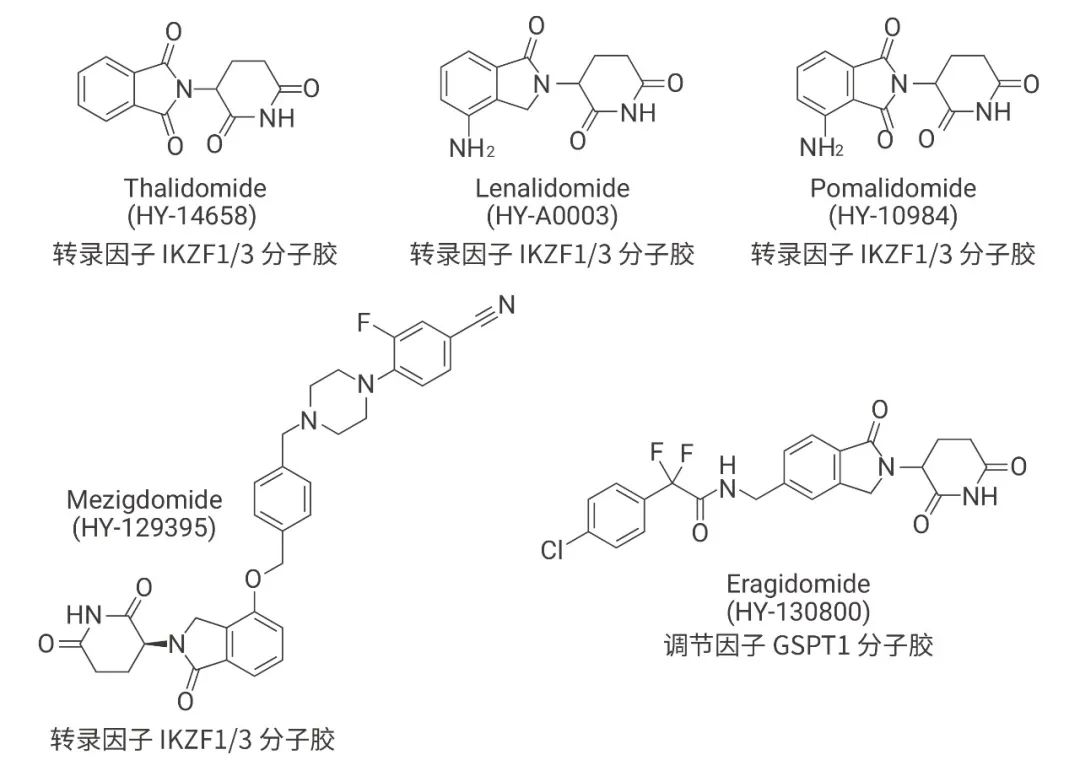
在降解剂分类里,分子胶 (Molecular glues) 指同样发挥诱导蛋白降解作用却无 Linker 连接的一类分子,如Thalidomide、CC-92480、CC-90009 等结构。分子胶在结构上更接近传统小分子,在膜透过性和生物利用度上更具优势,是 PROTAC 型降解剂的一个改造方向。
图 7. 分子胶的种类与降解剂类分子胶结构
降解能力评价
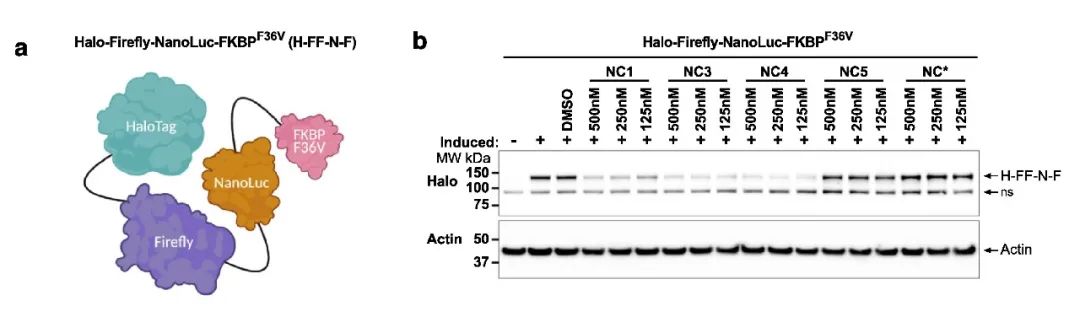
降解剂的最终目的是降解相关的蛋白, 无论是依赖泛素酶途径的 PROTAC,依赖蛋白酶体途径的 LYTAC,依赖 (ClpCP) 蛋白酶的 BacPROTAC。除 Kd 值测定之外,Western Blot 实验在验证蛋白降解方面更为直观,因此常常被用于 PROTAC 类分子活性的测试。
图 8. 靶蛋白与 Western Blot 实验结果[9]
总结
PROTAC 已经衍生出一类
“POI 配体-Linker-降解系统导向物” 模式的分子,这类分子补足了 PROTAC
作为降解剂在某些蛋白与非蛋白分子降解上的不足,赋予了降解剂这一概念更多的可能性。除了分子自身作用机制带来活性测试结果上与常规分子的差异,合适的降解途径对活性的影响尤其巨大。
MCE 是全球前沿的科研化学品和生物活性化合物供应商,可以为科学家提供 PROTAC 类相关产品,目前我们已有 PROTAC、AUTAC、ATTEC、分子胶以及它们的构成模块等各种产品在线。同时,我们还提供 PROTAC 类产品的一体化合成服务。
ATTEC |
LC3-mHTT-IN-AN2 (Compound AN2) 是一种 mHTT-LC3 连接化合物,LC3-mHTT-IN-AN2 与突变型亨廷顿蛋白 (mHTT) 和 LC3B 相互作用,但不与 wtHTT 或无关的对照蛋白相互作用。LC3-mHTT-IN-AN2 以等位基因选择性的方式降低了亨廷顿病 (HD) 小鼠神经元中mHTT水平。 |
LC3-mHTT-IN-AN1 (Compound AN1) 是一种 mHTT-LC3 连接化合物,LC3-mHTT-IN-AN1 与突变型亨廷顿蛋白 (mHTT) 和 LC3B 相互作用,但不与 wtHTT 或无关的对照蛋白相互作用。LC3-mHTT-IN-AN1 以等位基因选择性的方式降低了亨廷顿病 (HD) 小鼠神经元中mHTT水平。 |
AUTAC |
AUTAC1是一种 MetAP2 靶向自噬介导降解体 (AUTAC)。AUTACs 包含一个降解标签和一个弹头确保靶向特异性。AUTAC1 包含一个 FBnG 和一个 Fumagillol 部分。Fumagillol 共价结合到 MetAP2 上。 |
AUTAC2 是一种 FKBP12 靶向自噬介导降解体 (AUTAC)。AUTAC2 包含一个 FBnG 和 SLF 部分,其中 SLF 与FKBP12 非共价结合。 |
Molecular Glues |
Mezigdomide (CC-92480) 是一种 cereblon E3 泛素连接酶调节药物 (CELMoD),以分子胶的方式作用。Mezigdomide 与 cereblon 有较强的亲和力,具有抗骨髓瘤活性。 |
Eragidomide (CC-90009) 是首创的 GSPT1 选择性 cereblon (CRBN) E3 连接酶调节剂,以分子胶的方式作用。Eragidomide 通过 CRL4CRBN 选择性靶向 GSPT1 进行泛素化和蛋白酶体降解。 |
FPFT-2216 是一种“分子胶”化合物,可降解磷酸二酯酶 6D (PDE6D)、锌指转录因子 Ikaros (IKZF1)、Aiolos (IKZF3) 和酪蛋白激酶 1α (CK1α)。FPFT-2216 可用于癌症和炎症疾病的研究。 |
MCE 的所有产品仅用作科学研究或药证申报,我们不为任何个人用途提供产品和服务。
参考文献
1. Jin J, Wu
Y, Chen J, Shen Y, Zhang L, Zhang H, Chen L, Yuan H, Chen H, Zhang W,
Luan X. The peptide PROTAC modality: a novel strategy for targeted
protein ubiquitination. Theranostics. 2020 Aug 8;10(22):10141-10153.
2. Fischer F, Alves Avelar LA, Murray L, Kurz T. Designing HDAC-PROTACs: lessons learned so far. Future Med Chem. 2022 Jan;14(3):143-166.
3. Pettersson M, Crews CM. PROteolysis TArgeting Chimeras (PROTACs) - Past, present and future. Drug Discov Today Technol. 2019 Apr;31:15-27.
4. Ahn G, Banik SM, Miller CL, Riley NM, Cochran JR, Bertozzi CR. LYTACs that engage the asialoglycoprotein receptor for targeted protein degradation. Nat Chem Biol. 2021 Sep;17(9):937-946.
5. Fu Y, Lu B. Targeting lipid droplets for autophagic degradation by ATTEC. Autophagy. 2021 Dec;17(12):4486-4488.
6. Morreale FE, Kleine S, Leodolter J, Junker S, Hoi DM, Ovchinnikov S, Okun A, Kley J, Kurzbauer R, Junk L, Guha S, Podlesainski D, Kazmaier U, Boehmelt G, Weinstabl H, Rumpel K, Schmiedel VM, Hartl M, Haselbach D, Meinhart A, Kaiser M, Clausen T. BacPROTACs mediate targeted protein degradation in bacteria. Cell. 2022 Jun 1:S0092-8674(22)00593-1.
7. Schreiber SL. The Rise of Molecular Glues. Cell. 2021 Jan; 184(1): 3-9.
8. Li Z, Wang C, Wang Z, Zhu C, Li J, Sha T, Ma L, Gao C, Yang Y, Sun Y, Wang J, Sun X, Lu C, Difiglia M, Mei Y, Ding C, Luo S, Dang Y, Ding Y, Fei Y, Lu B. Allele-selective lowering of mutant HTT protein by HTT-LC3 linker compounds. Nature. 2019 Nov;575(7781):203-209.
9. Grohmann, C., Magtoto, C.M., Walker, J.R. et al. Development of NanoLuc-targeting protein degraders and a universal reporter system to benchmark tag-targeted degradation platforms. Nat Commun. 2022 Apr; 13:2073.
https://blog.sciencenet.cn/blog-3506747-1360326.html
上一篇:2022 上半年 FDA 小分子药物盘点 - MedChemExpress
下一篇:外泌体介绍 - MedChemExpress
全部作者的其他最新博文
- • 钙离子通道阻断剂库是开发降压药物进行心血管疾病研究的有用工具 | MedChemExpress (MCE)
- • 硼酸类化合物库可以用于癌症等疾病研究 | MedChemExpress (MCE)
- • 自身免疫病化合物库是筛选自身免疫病药物的有用工具 | MedChemExpress (MCE)
- • 抗病毒中药单体化合物库是从中药中发现抗病毒药物的有效工具 | MedChemExpress (MCE)
- • 抗寄生虫化合物库可以用于新适应症的开发及新型抗寄生虫靶点的鉴定 | MedChemExpress (MCE)
- • 抗氧化化合物库是开发新的抗氧化剂和研究氧化应激的有用工具 | MedChemExpress (MCE)