博文
高温高压下甲烷-水体系中甲烷行为的拉曼光谱研究
||
高温高压下甲烷-水体系中甲烷行为的拉曼光谱研究*
(北京大学造山带与地壳演化教育部重点实验室,
摘要 用金刚石压腔和激光拉曼光谱研究了甲烷-水体系的相态及P-T关系。研究结果表明,在不同的温度和压力下,甲烷-水体系具有以下三种不同的状态:(1)状态1:在75-150℃和相应压力下,甲烷呈低密度不混溶态与水共存;(2)状态2:在175-220℃和相应压力下,甲烷呈高密度不混溶态与水共存;(3)状态3:在高于225℃和更高压力下甲烷与水完全互溶为溶解态甲烷。其中高密度甲烷转变为溶解态甲烷时其体系压力突然降低,反映了其体系的总体积发生了明显缩小。各不同状态下,体系的P-T关系以及甲烷的拉曼峰和半高宽与温度和压力之间的关系均存在明显的不连续。这表明,多组分体系中相态的转变及各相态之间的相互作用方式变化均会造成体系性质如体积的突然变化。另外,由实验还获得了不同状态甲烷的dv/dT和dv/dP值。因此甲烷的状态可以通过其拉曼光谱特征及其与温度和压力之间的关系进行区分。
关键词:甲烷,水,拉曼光谱,混溶,高温,高压
引言
含甲烷的流体存在于许多地质环境,如洋中脊 (Kelley, 1996)、火山(Carroll and Holloway, 1994)、煤田和油田 (Roedder, 1979; Kisch and Van Den Kerkhof, 1991; Hedenquist and Lowenstern, 1994; Dubessy et al., 2001)以及流体包裹体中(Mullis et al., 1994),因此了解CH4-H2O体系的性质及其状态方程等无论是理论和实际均具有重要意义。目前,已经有不少纯甲烷体系的状态方程等方面的研究资料(Blencoe等,1992;Redlich等,1949;Jacobs等,1981;Saxena等,1987;Duan等,1992a, 1996;Friend等,1989)。然而,有关甲烷-水体系的相关系及其状态方程方面的高温高压实验研究数据非常有限。例如,温度低于650℃的实验压力均小于25MPa,温度高于650℃的实验压力也仅限于300MPa(Welsch,1973;Christotoforakos,1985;Sretenskaya et al.,1986;Joffrion and Eubank,1988, 1989;Shmonov et al.,1993;Abdulagatov et al.,1993a,b;Hnedkovsky et al. ,1996;Fenghour et al.,1996)。最近,一些研究者用分子水平的计算机模拟方法研究了更高温度和压力下甲烷-水体系的PVTx关系(Zhang等,2007;Konrad O.,2005),但其结果的正确性仍需要检验。另外,流体包裹体中甲烷的拉曼光谱可以测定其内压和研究其形成压力。但甲烷的拉曼位移与温度和压力之间的关系仍缺少较高温度和压力的实验数据。最近我们进行温度和压力分别达300和500MPa下甲烷-水体系的原位观察时发现,与水共存的甲烷在不同的温度和压力下存在着低密度和高密度两种状态,且二者的拉曼位移与温度和压力关系明显不同。另外,当甲烷溶解于水中时,其宏观性质和拉曼位移与温度和压力的关系均发生了突变。本文是该研究的报道之一。
实验方法
高温高压原位观察实验采用的金刚石压腔类似于Bassett(1994)的水热金刚石压腔。该压腔通过上下两个微型电炉对金刚石压腔进行加温,温度由K型热电偶进行测量,其测量精度为±0.5℃。实验用的垫片为0.35mm厚的铼片,样品孔直径为0.3mm。实验体系中的样品用Renishaw 1000 型显微激光拉曼光谱仪进行测量,仪器的狭缝宽度为50微米;用波长为514.5nm的氩离子激光器激发样品,其功率为25mW,收集时间为10 秒。
实验用的甲烷样品在中国科学院地质与地球物理研究所合成。其合成方法采用国际常用的的冰加入甲烷气体的方法(Stern,1996,1998;Helgerud,2001,伍向阳,2004)。装甲烷水合物前,先将压腔和工具在冰柜中冷冻1小时。装样时首先将作为压力标定的石英装入样品孔中,然后用冷的镊子取少量甲烷水合物放在垫片的圆孔上,迅速把两个压砧压上,旋紧螺丝即可把甲烷水合物密封在压腔中。
金刚石压腔中的压力由石英的464cm-1 拉曼峰与压力和温度的关系确定(Christian S,2000):
P(MPa) = 0.36079•[(∆Vp)464]2 +110.86 •(∆Vp)464
(∆Vp)464, p=0.1MPa (cm-1) = 2.50136•10-11•T4 + 1.46454•10-8•T3 – 1.801• 10-5 •T2 – 0.01216•T + 0.29
式中0 <(∆Vp)464 ≤ 20。该式的适用条件是:-196 ≤T(℃)≤560 和压力小于2.0GPa 下。
结果和讨论
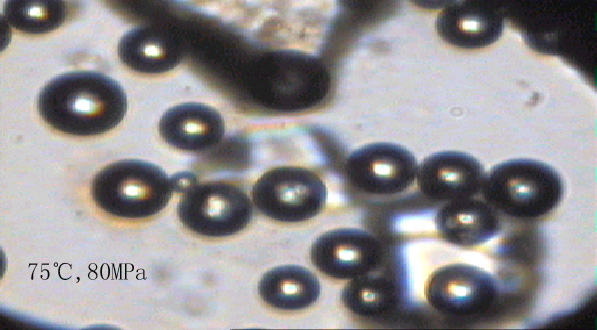
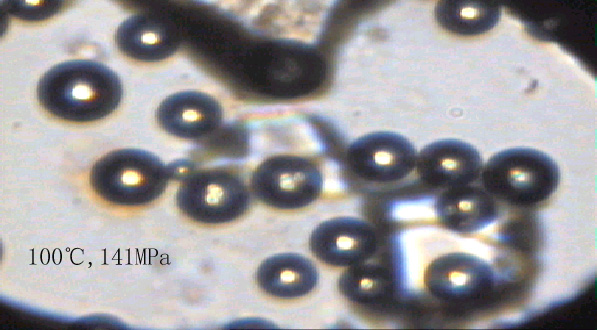
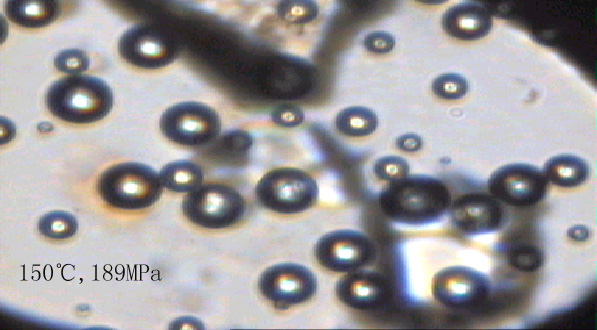
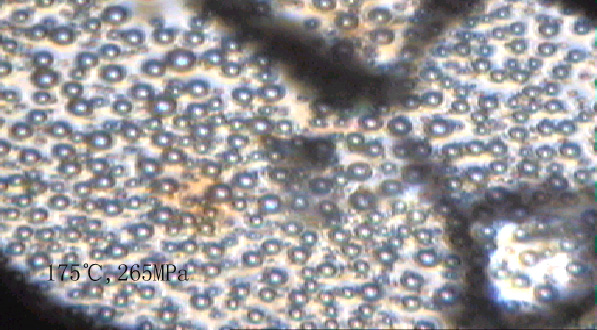
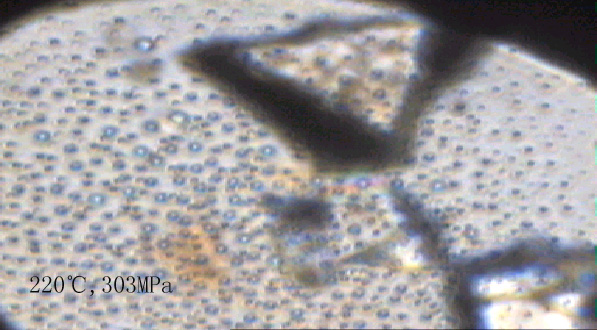
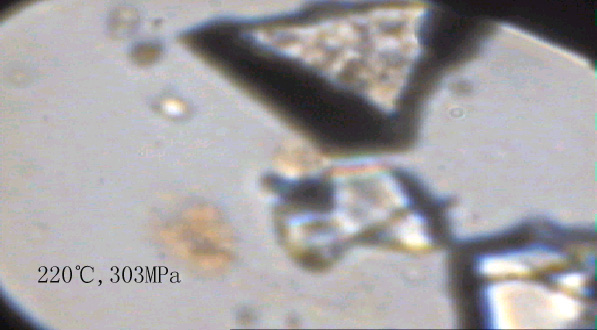
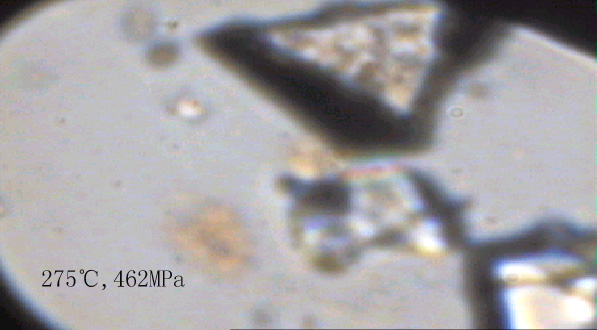
图1是在不同温度和压力下的实验中甲烷-水体系相态的显微照片。由照片可以看出,在75-150℃的温度范围及其相应压力下的甲烷气泡边缘有着明显宽的黑边,反映气泡中的甲烷与水的折射率差异较大。气泡的拉曼分析结果证明它们主要是甲烷,因此气泡边缘光的折射特征也反映了甲烷相对于水具有明显低的密度。由于实验的温度和压力均高于甲烷的临界点,因此该状态应称之为低密度甲烷(状态1)。在175-220℃的温度及其相应压力下,甲烷气泡明显缩小,但同时数量大大增加。与低密度的甲烷气泡相比,其与水相邻部分的黑边明显浅和变窄。这显示出其密度明显增大,表明此时的甲烷具有明显不同于低密度(状态1)态甲烷的性质。这里我们称其为高密度甲烷(状态2)。当达到220℃及以上温度和压力的条件时甲烷全部溶解于水中而呈完全均一的状态。我们称其为完全溶于水中的甲烷或溶解态甲烷(状态3)。
甲烷的状态及其与水之间的相互作用在其P-T关系上也有明显的反映。图2是体系中甲烷-水体系的温度与压力的关系图。由图可以看到,甲烷-水体系的P-T关系也可划分出三个不同的温度和压力区间。其中低密度甲烷与高密度甲烷的温度与压力关系基本连续,但高密度甲烷较之低密度甲烷具有稍大一些的压力对温度的变化率(斜率)。由图还可以看到,高密度甲烷向溶解态甲烷转变时的温度压力关系出现了明显的不连续。即在温度220℃和压力约350MPa时发生了压力的突然下降。其压力降大约为100MPa。
表 1 高温高压下不同相态甲烷的拉曼位移和半高宽
温度(℃) | 压力(MPa) | 甲烷拉曼峰(cm-1) | 甲烷拉曼峰半高宽(cm-1) |
75 | 80 | 2912.42 | 5.36 |
100 | 141 | 2912.20 | 5.36 |
125 | 144 | 2911.96 | 6.23 |
150 | 189 | 2911.57 | 6.67 |
157 | 242 | 2911.34 | 8.69 |
175 | 265 | 2911.69 | 8.01 |
200 | 357 | 2911.69 | 8.26 |
220 | 303 | 2910.04 | 14.50 |
225 | 324 | 2910.17 | 13.92 |
250 | 324 | 2910.28 | 16.15 |
275 | 426 | 2910.60 | 16.87 |
300 | 488 | 2910.87 | 17.82 |
|
|
|
|
|
|
|
|
|
|
其中粗黑边气泡部分为低密度甲烷(75-150℃),气泡以外为水;细小的气泡部分为高密度甲烷(175-220℃),气泡以外为水;无气泡的为溶解态甲烷(220-300℃),不规则形状的物质是作为压标的石英
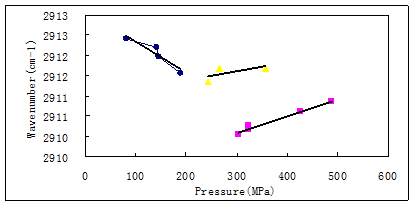
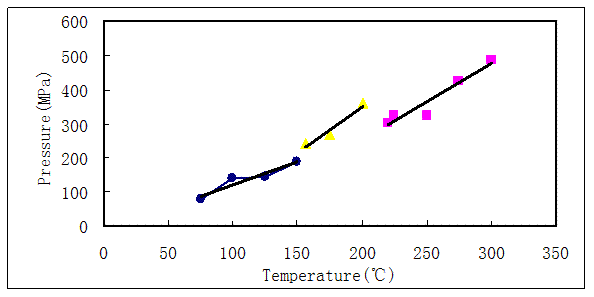
图3 是甲烷-水体系中甲烷拉曼位移与温度和压力的关系图。由图也可以看到,各不同状态的甲烷与温度或压力之间同样也存在着明显的不连续。其中低密度态的甲烷拉曼峰波数随温度和压力的增大而降低。而高密度态甲烷和溶解态甲烷却与低密度态甲烷的变化关系相反,不同的是二者的拉曼峰波数与温度和压力关系的斜率稍有差异。这表明高密度态和溶解态的甲烷分子处于完全不同于低密度态甲烷的环境,其性质也与状态1 的低密度甲烷完全不同。另外,各状态的拉曼峰半高宽与温度和压力的关系也存在着不连续。例如,低密度态和溶解态的甲烷拉曼峰的半高宽随温度和压力的升高而变宽,但高密度态则与其相反;且溶解态与高密度态之间有着明显的突然上跳特征。上述甲烷在不同温度和压力下的不连续现象表明:(1)在进行分子水平的计算机模拟时必须注意其不同状态的模型参数差异;(2)在进行流体包裹体中甲烷的研究和测量时也必须区分低密度和高密度甲烷;(3)地球内部多组分流体相互作用对于深部系统体积的影响。
上述现象的原因可以从甲烷分子所处的状态及其与水之间的相互作用进行解释。其中低密度态和高密度态的甲烷均属于与水不混溶的独立甲烷体系,其中大部分的甲烷与水分子之间不存在相互作用或只有很小的相互作用,而是在甲烷分子之间存在着主要的相互作用。因此它们的行为基本上遵循纯甲烷的行为。状态3的甲烷完全溶解在水中,因此甲烷分子周围必然存在着不同数量的水分子并与其发生着相互作用。对于低密度态的甲烷,由于其密度较低,当环境的温度升高而引起的压力增大可以通过增大密度得到缓冲,因此其随温度的增高体系的压力增加较少(等容线的斜率较小);而高密度态的甲烷体系具有较高的密度,其相对不容易被压缩,因此高密度态甲烷具有比低密度态甲烷大一些的压力对温度的变化率。至于溶解态甲烷发生的压力突然降低,可以归结为甲烷溶解于水中发生相互作用而导致的不理想混合。换句话说,即甲烷溶解于水中后,其总体积明显小于二者呈独立状态(独立相)时的总体积。这意味着在此温度和压力条件下,甲烷与水的混合具有负的过剩体积。
从不同状态甲烷的拉曼峰波数和半高宽变化可以大致了解其相互作用的性质。由图3可以看到,甲烷-水体系由高密度甲烷转变为溶解态甲烷时,其甲烷的拉曼峰突然下降约2cm-1。根据振动光谱理论,拉曼峰的频率与键强度(或力常数)和质点的质量相关。由于甲烷发生溶解于水中的过程并未发生甲烷分子内化学键的变化(即C-H键并未发生变化,其力常数亦未变化),因此溶解态的甲烷拉曼峰波数突然降低显然与甲烷分子中的碳和氢与水分子的氧和氢发生了缔合作用有关。即这种作用造成了甲烷分子中振动质点的折合质量增大,从而使拉曼峰的波数突然降低。另外,溶解态的甲烷拉曼峰半高宽明显变宽也可归因于其与水分子之间发生了缔合作用。其性质是否类似于氢键的作用还有待于进一步研究。
由实验测量数据可以获得不同状态甲烷的拉曼位移与温度和压力关系的dv/dT和dv/dP(表2)。由表2 可以看出,不混溶的低密度甲烷具有负的dv/dT和正的dv/dP值,不混溶的高密度甲烷则与之相反;而溶解于水中的甲烷的这些值均是正的。另外,温度和压力对不同状态的甲烷拉曼峰的影响也有明显的不同。其中温度对低密度甲烷和高密度甲烷的影响较接近,只是作用结果相反;而压力对高密度的甲烷明显强于低密度甲烷。另外,温度和压力对溶解态的甲烷影响明显小于低密度态甲烷 和高密度态的甲烷。这反映了高密度态的甲烷周围所存在的水分子对温度和压力的影响起到了屏蔽作用。
|
|
|
|
图3 甲烷-水体系的甲烷拉曼位移和半高宽与温度或压力的关系图
不混溶低密度甲烷 | 不混溶高密度甲烷 | 溶解甲烷 | |
甲烷拉曼位移(cm-1) 0℃,0.1MPa | 2913 | 2908 | 2908 |
dv/dT(cm-1/℃) | -0.01134 | 0.02961 | 0.005343 |
dv/dP(cm-1/MPa) | 0.0001392 | -0.007497 | 0.001985 |
结论
由以上实验观察和数据分析结果可以得出以下结论:
(1)在实验的温度和压力条件下,甲烷-水体系在高温高压下存在着三种不同的状态:不混溶的低密度态甲烷、不混溶的高密度态甲烷和溶解于水中的溶解态甲烷;
(2)各不同状态的甲烷具有不同的拉曼参数与温度和压力的关系;
(3) 由低密度甲烷向高密度甲烷转变时,其温度与压力的关系没有间断点,但存在着斜率上的差别;而由不混溶的高密度甲烷转变为溶解态甲烷时体系的体积将缩小,并造成压力的突降。这意味着地球内部多组分流体相互作用对于深部系统体积将产生重要影响。
参考文献
[1]Kelley D. S. (1996) Methane-bearing fluids in the oceanic crust: Gabbro-hosted fluid inclusions from the southwest Indian Ridge. J. Geophys. Res. 101, 2943–2962.
[2]Carroll M. R., and Holloway, J. R. (1994) Volatiles in Magmas. In Rev. Mineral. (ed. P. H. Ribbe). Mineralogical Society ofAmerica.
[3]Roedder E. (1979) Fluid inclusions as samples of ore fluids. In Geochemistry of Hydrothermal Ore Deposits (ed. H. Barnes). Wiley-Interscience, pp. 684–737.
[4]Kisch H. J., and Van Den Kerkhof A. M. (1991) CH4-rich inclusions from quartz veins in the Valley- and Ridge province and the anthracite fields of the Pennsylvania Appalachians. Am. Mineral. 76, 320–340.
[5]Hedenquist J. W., and Lowenstern J. B. (1994) The role of magmas in the formation of hydrothermal ore deposits. Nature 370, 519–526.
[6]Dubessy J., Buschaert S., Lamb W., Pironon J., and Thiery R. (2001) Methane-bearing aqueous fluid inclusions: Raman analysis, thermodynamic modelling and application to petroleum basins. Chem. Geol. 173(1–3), 193–205.
[7]Welsch (1973) Die system xenon-wasser und methan-wasser beiholen drticken und temperaturen. Ph.D thesis, University of Karlsruhe.
[8]Christotoforakos, M. (1985). Uberkritische systeme uder hohem Drucj. Eine statistisch- thermodynamisch entwickelte Zustandsgleichung und experimentelle Untersuchungen. Ph.D University of Karlsruhe.
[9]Sretenskaya N. G., Zhakirov I. V., Shmonov V. M., and Shmulovich K. I. (1986) Vodosoderzhaschie Fluidnye Systemy (Water-bearing Fluid Systems). Nauka Publishing House.
[10]Joffrion L. L., and Eubank P. T. (1988) P–V–T data and virialcoefficients for gaseous methane-water mixtures with correction for adsorption effects. Fluid Phase Equilibr. 43(2-3), 263–294.
[11]Shmonov V. M., Sadus R. J., and Franck E. U. (1993) High pressure phase-equilibria and supercritical PVT data of the binary water plus methane mixture to 723 K and 200 Mpa. J. Phys. Chem. 97(35), 9054–9059.
[12]Abdulagatov I. M., Bazaev A. R., and Ramazanova A. E. (1993b) Volumetric properties and virial coefficients of (water + methane). J. Chem. Thermodyn. 25(2), 249–259.
[13]Hnedkovsky L., Wood R. H., and Majer V. (1996) Volumes of aqueous solutions of CH4, CO2, H2S, and NH3 at temperatures from 298.15 K to 705 K and pressures to 35 MPa. J. Chem. Thermodyn. 28(2), 125–142.
[14]Fenghour A., Wakeham W. A., and Watson J. T. R. (1996),Densities of (water plus methane) in the temperature range 430 K to 699 K and at pressures up to 30 MPa. J. Chem. Thermodyn. 28(4), 447–458.
[15]Chi Zhang, Zhenhao Duan, Zhigang Zhang,2007,Molecular dynamics simulation of the CH4 and CH4–H2O,systems up to 10 GPa and 2573 K,Geochimica et Cosmochimica Acta 71, 2036–2055.
[16]Konrad O., and Lankau T. (2005) Solubility of methane in water: the significance of the methane–water interaction potential. J. Phys. Chem. B 109(49), 23596–23604.
[17] Bassett W.A., Shen A.H., Bucknum M., A new diamond cell for hydrothermal studies to 2.5 GPa and from -190 ℃ to 1200℃, 1994, Rev. Sci. Instrum. 64(8): 2340.
[18] 伍向阳,段体玉,杨伟, 孙樯,2008,不同压力下型甲烷水合物拉曼光谱,岩石学报,vol.24(1)171-175.
[19] Schmidt C, Ziemann MA. In-situ Raman spectroscopy of quartz: A pressure sensor for hydrothermal diamond-anvil cell experiments at elevated temperatures. American Mineralogist, 2000, 85: 1725-1734.
[20]Duan Z. H., Moller N., and Weare J. H. (1992a) An equation of state for the CH4–CO2–H2O system: I. Pure systems from 0 to 1000 _C and 0 to 8000 bar. Geochim. Cosmochim. Acta 56(7), 2605–2617.
[21]Duan Z. H., Moller N., and Weare J. H. (1992b) An equation of state for the CH4–CO2–H2O system: II. Mixtures from 50 to 1000 _C and 0 to 1000 bar. Geochim. Cosmochim. Acta 56(7), 2619–2631.
*国家重点基础研究发展计划资助项目(资助号: 2006CB403508) ;国家自然科学基金资助项目(批准号:40873047)
https://blog.sciencenet.cn/blog-3451795-1256084.html
上一篇:立方氮化硼压标的研究
下一篇:金刚石压腔顶砧的调平方法