博文
142 野生动物狂犬病疫苗
|||
野生动物狂犬病疫苗
摘要
自20世纪70年代第一次原理性实验研究以来,口服狂犬病疫苗在控制和消除野生动物狂犬病方面获得了很高的声誉。口服狂犬病疫苗( oral rabies vaccination,ORV)从仅从几个强毒狂犬病病毒分离株中获得的经典减毒病毒疫苗开始,首次提供了新的机会,并在全球范围内开辟了抗击这种致命人畜共患病的新途径,特别是在其犬类野生动物宿主中。除了传统方法之外,生物技术工具已经越来越多地用于生产新的口服狂犬病疫苗,目的是提高各种犬类野生动物宿主物种的安全性、免疫原性和效力。尽管已经开发了异源载体系统来表达狂犬病病毒( rabies virus,RABV)的具有免疫活性的糖蛋白(G),但重组DNA技术和病毒反向遗传学的最新进展有助于通过定向修饰和定向减毒狂犬病病毒构建体来促进疫苗开发。与人类、宠物和家畜不同,除了使用改良的活病毒疫苗之外,目前还没有替代方法可以在种群水平上有效地给犬类野生动物宿主接种疫苗。与其他兽医用疫苗相比,除了安全有效的疫苗结构外,吸引人的物种特异性诱饵以及明确的分配系统/策略是任何野生动物口服狂犬病疫苗不可或缺的组成部分。由于诱饵在该领域的成功应用中起着决定性作用,因此它们是许可程序的一个组成部分。本章总结了野生动物口服狂犬病病毒疫苗的最新信息,并对未来野生动物疫苗开发的挑战进行了展望。
介绍
疫苗仍然是人类聪明才智、科学努力以及全球公共和动物健康团体共同努力的最伟大成就之一。疫苗是主要为防止疾病或病原体感染而开发的生物制剂。它们通常含有弱化、杀死或修饰形式的相应病原、表面蛋白或其毒素,这些病原、表面蛋白或其毒素刺激人类和动物的自然防御机制,从而产生活性的获得性细胞和/或体液免疫反应,以防止感染野毒株。
国际上越来越认识到安全有效的疫苗和其他干预措施的重要性,它们是抗击人类病毒性和细菌性疾病的一揽子措施的一部分。疫苗的设计应防止感染,而不是防止疾病的临床症状,并应尽可能产生无菌免疫。爱德华·詹纳对免疫接种有创新性贡献,这是通过有意使用疫苗接种控制传染病的首次成功尝试,疫苗接种和疫苗开发领域总体上也受到早期狂犬病研究的决定性影响。自上千年以来,狂犬病是人类已知但被忽视的最古老的病毒性人畜共患病,对全世界的公共健康构成了严重威胁。路易斯·巴斯德于1885年首次用暴露于干燥空气中而减毒的粗狂犬病病毒进行人类疫苗接种,这被认为是今天人类暴露前和暴露后有效的狂犬病预防和动物预防性疫苗接种的基础。
至于后者,使用疫苗接种控制动物中的病毒和细菌疾病已经成为全球关注的焦点,以防止由于家畜、宠物和野生动物中的严重疾病爆发而导致的经济、动物福利和公共卫生成本。兽医用疫苗不仅可用于保护动物健康,还可用于保护人类健康免受人畜共患病感染,例如动物狂犬病疫苗接种。考虑到疫苗接种不仅在个体水平上具有积极的免疫影响,而且在群体水平上也具有积极的免疫影响,对犬类(人类狂犬病暴露的主要媒介)进行大规模疫苗接种,使用有效的灭活疫苗,在欧洲、北美、日本和许多其他岛屿消除了犬类介导的狂犬病。此外,拉丁美洲为通过大规模疫苗接种运动成功减少犬传播的人狂犬病病例提供了蓝本,为国际商定的到2030年消除犬传播的人狂犬病病例的目标铺平了道路。
然而,除了犬是狂犬病病毒(RABV)唯一公认的家养动物宿主外,这种病毒的多种谱系在广泛的野生哺乳动物宿主中循环并共同进化,主要在食肉动物目中,包括犬科、浣熊科、獴科、臭鼬科、灵猫科和鼬科(表1)。然而,翼手目动物也是在美洲的RABV的主要宿主。正如在世界许多地区一样,野生动物狂犬病监测并不存在,野生动物储存宿主的名单很可能在不久的将来随着监测强度的增加而迅速扩大。一个好例子是狨猴(Callithrix jacchus),它被确定为巴西新的野生狂犬病宿主。
表1世界地理范围内食肉动物目中狂犬病的主要动物宿主
区域 | 物种 | 学名 | 拉丁学名 |
北极 | 北极狐 | 北极狐(学名:Vulpes lagopus) | 犬科Canidae |
欧洲 | 红狐 | 红狐狸Vulpes vulpes | 犬科Canidae |
貉子 | 貉(学名:Nyctereutes procyonoides) | 犬科Canidae | |
非洲 | 条纹豺 | 侧纹胡狼(学名:Canis adustus) | 犬科Canidae
|
黑背豺狼 | 黑背胡狼Canis mesomelas | ||
大耳狐 | 大耳狐Otocyon megalotis | ||
蓬灰貂獴 | 蓬灰貂獴 Galerella pulverulenta | 獴科(Herpestidae) | |
笔尾獴 | 笔尾獴Cynictis penicillata
| ||
非洲獴 | 缟獴Mungos mungo | ||
北美 | 浣熊 | 北美浣熊Procyon lotor | 浣熊科 Procyonidae |
条纹臭鼬
| 条纹臭鼬Mephitis mephitis
| 臭鼬科 Mephitidae
| |
红狐 | 红狐狸Vulpes vulpes
| 犬科Canidae
| |
郊狼
| 郊狼Canis latrans
| ||
灰狐
| 灰狐(学名:Urocyon cinereoargenteus)
| ||
加勒比群岛 | 小印度猫鼬 | 红颊獴Herpestes auropunctatis
| 獴科 Herpestidae
|
南美洲 | 食蟹狐
| 食蟹狐Cerdocyon sp
| 犬科Canidae
|
中东 | 红狐 | 红狐狸Vulpes vulpes
| 犬科Canidae
|
亚洲胡狼 | 金豺Canis aureus
| ||
亚洲-远东 | 红狐 | 红狐狸Vulpes vulpes
| 犬科Canidae
|
草原狐狸 | 沙狐(学名:Vulpes corsac)
| ||
貉
| 貉(学名:Nyctereutes procyonoides) | ||
獴
| 赤獴(学名 Herpestes smithii)
| 獴科(Herpestidae) | |
中國鼬獾 | 鼬獾Melogale moschata
| 鼬科Mustelidae
| |
金色的椰子猫 | 金椰子猫Paradoxurus zeylonensis | 灵猫科Viverridae
|
直到20世纪70年代,通过接种疫苗来控制欧洲和北美的野生动物狂犬病似乎是不可思议的。为了打破自然感染链,传统的疾病控制方法是专门针对野生动物储存宿主的种群密度的急剧下降。除了少数例外,长达十年的痛苦经历表明,包括集中扑杀、施毒和荷尔蒙绝育在内的所有这些措施都无法在更大范围内控制疾病,或者相反,是适得其反的。这是一个合乎逻辑的结果,也是从1980年以来犬的成功中得到的启发,控制野生动物狂犬病的重点转移到各自主要宿主的疫苗接种上。然而,许多障碍必须克服。一般来说,虽然对单个动物的影响决定于疫苗的效力,但对群体的影响决定了疫苗的效果。尽管灭活疫苗在野生食肉动物狂犬病宿主中诱导了足够的免疫反应,但它们不是真正的替代物,因为它们的肠胃外应用本身排除了它们用于野生动物的大规模疫苗接种,因此,它们仅用于捕获-接种疫苗-释放(trap–vaccinate–release,TVR)运动。
自20世纪70年代进行第一次原理验证实验研究以来,口服狂犬病疫苗为在野生动物中对抗狂犬病开辟了新的途径。从传统的减毒方法到生物技术衍生的方法,已经开发了多种用于野生动物的口服狂犬病病毒构建体。所有成功的方法都是基于复制能力强的病毒,因为口服灭活狂犬病疫苗无效。
减毒狂犬病疫苗
在过去的40年里,几种狂犬病减毒活疫苗株已经获得了野生动物口服使用的市场授权。图1总结了现有狂犬病减毒活疫苗毒株的假定祖先和传代历史。几乎所有这些疫苗株都是1935年从美国阿拉巴马州的一只患狂犬病的犬身上分离出来的,最初只在小鼠大脑中繁殖。然而,疫苗株巴斯德病毒和作为SAD相关疫苗代表的SAD B19之间的密切遗传关系在某种程度上引起了人们的注意,并且事实上,可能会对各自疫苗株的起源和传代历史提出质疑。当时,美国前疾病控制中心位于阿拉巴马州的蒙哥马利。所以,“阿拉巴马”这个词也可以指实验室,而不是犬的起源。
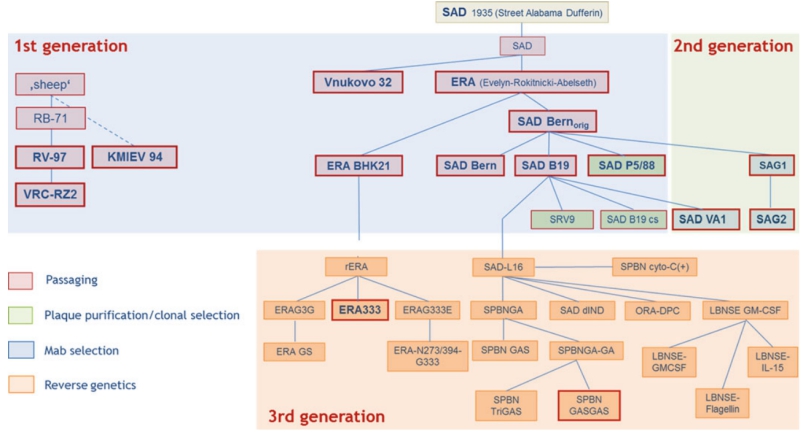
图1第一代、第二代和第三代减毒狂犬病疫苗株的历史和演变。突出显示(框出)的疫苗株已获得疫苗许可和/或用于野外。显示了用于生成相应病毒的方法(参见图例)
随后在各种非神经细胞(例如仓鼠肾细胞、鸡胚和猪肾细胞)中连续传代SAD,导致高度减毒的、细胞培养适应的“ERA”菌株。经口服途径免疫后,证明衍生的高滴度商业ERA疫苗对红狐有效。通过增强对幼仓鼠肾(BHK)细胞的适应和额外的热稳定化产生疫苗病毒株,进一步开发了ERA疫苗株,当转移到欧洲时,该疫苗病毒株随后被重新命名为“SAD Bern”(SAD Bern orig)。
ERA和SAD Bernorig株都是当今绝大多数先进形式的ERA和SAD为基础的第一代野生动物口服狂犬病减毒活疫苗的祖先。这些第一代疫苗中的一些包含通过在原代BHK细胞或克隆的BHK/BSR细胞上持续传代和适应而产生的后代,例如,ERA-BHK21疫苗、Vnukovo-32 、Bio-10-SAD Bern、SAD B19 、SAD P5/88 以及SRV9。其他用于野生动物口服疫苗接种的第一代疫苗是来自哈萨克斯坦的VRC-RZ2和俄罗斯疫苗株RV-97。有趣的是,RV-97及其减毒前体病毒RB-71和“绵羊”在系统发育上与日本的疫苗株更为相关,如Nishigara株。RABV核蛋白(N)编码基因的高序列同一性(99%)表明来自哈萨克斯坦的毒株VRC-RZ2是RV-97 的直接后代。根据传代历史,白俄罗斯疫苗株KMIEV-94是通过在不同细胞培养物中连续传代获得的狂犬病病毒株71-Bel-NIIEV VGNKI的衍生物。VRC-RZ2和KMIEV-94这两个毒株是否可以追溯到同一祖先菌株(RB-71)还有待证明。这组疫苗株已被用于哈萨克斯坦、白俄罗斯和乌克兰等国家的野生动物口服狂犬病疫苗。
针对第一代疫苗在幼儿和免疫受损的啮齿动物中的与实验上已知的残留致病性有关的安全性问题,通过使用抗-G单克隆抗体产生选择突变体,改善了安全性。结果,获得疫苗株SAD VA1、SAG 1和SAG 2。后者的特征在于在RABV G (G333E)残基333用谷氨酸替代精氨酸,这进一步降低了致病性。然而,第二代口服狂犬病疫苗也不完全是无致病性的,正如在免疫低下和近交系小鼠中所显示的那样。尽管SAD衍生的第一代和第二代口服狂犬病疫苗的密切遗传关系已被全基因组测序和下一代测序所证实,后者揭示SAD衍生的口服狂犬病疫苗可能由或多或少的异源病毒群体组成。
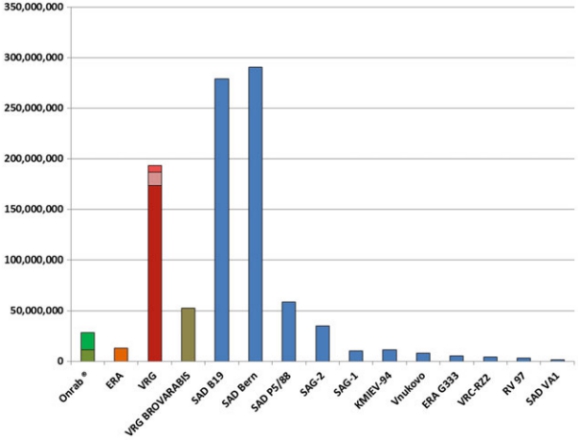
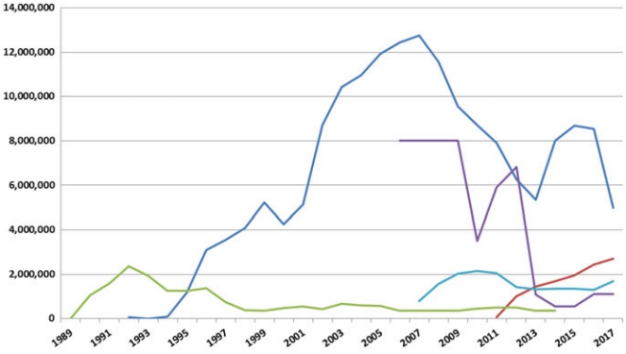
在1978年至2017年期间,欧洲和北美共分发了超过10亿剂含有不同口服狂犬病疫苗的诱饵,第一代和第二代口服狂犬病疫苗诱饵的数量约为7.2亿个(图2)。北美在1989年至2004年期间仅在ORV战役中使用了一种减毒疫苗株(ERA-BHK21),消除了加拿大安大略省东部的狂犬病,与之相反,在此期间,ORV在整个欧洲使用了10种不同的第一代和第二代口服狂犬病疫苗,SAD B19和SAD Bern是迄今为止使用最广泛的疫苗病毒株(图2)。
|
|
图2 1978年至2017年间在欧洲和北美分发的口服狂犬病疫苗诱饵的累积数量。对欧洲来说,数字是从其他地方描述的接种疫苗的地区推断出来的,并由欧洲狂犬病数据库的数据集完成。
在整个期间,从红狐的口服疫苗接种区以及欧洲和北美的非目标物种报告了23例疫苗诱导的狂犬病病例,r ERA-BHK21、SAD Bern、SAD B19和 SADP5/88引起的狂犬病发生率为4800万分之一。最近使用下一代测序进行的深入分析显示,在那些疫苗诱导的病例中,病毒群体是克隆的,与它们的亲代疫苗相反,表明在感染期间存在强瓶颈,而不是回复到毒力。疫苗诱导的狂犬病病例必须在药物警戒的框架内报告。然而,这些病例都没有在时间和空间上联系起来,也没有在目标物种中建立起来种群,因此,没有流行病学相关性。此外,在欧洲和北美野生动物ORV的过去40年中,在无意的人类接触后,没有任何口服狂犬病减毒疫苗的不良反应或其他严重事件的报告。
基于载体的疫苗
病毒载体不仅能耐受大的外源基因的插入,还能在各种疾病模型中充分展示免疫反应的外源抗原。由于分子技术的进步,RABV蛋白(G)的插入成为一个选择,特别是使用痘病毒作为载体的。因此,基于重组载体的活疫苗可为野生动物狂犬病的控制提供某些优势,特别是在安全性方面,因为狂犬病病毒相关疾病不能在接种的动物中发生。表达重组狂犬病病毒基因的重组痘苗病毒哥本哈根株是第一个基于重组痘病毒的口服狂犬病疫苗。1989年至2017年间,批准的疫苗已被广泛用于北美的浣熊、灰狐狸和郊狼、加拿大的浣熊、以色列的豺狼以及几个西欧国家的红狐的口服疫苗接种,投放了超过2.45亿剂V-RG诱饵(图2和图3)。尽管它在许多宿主中有效,但在臭鼬中,V-RG不能诱导足够的保护性免疫,并且在控制浣熊狂犬病中似乎效率较低。
|
图3 1989年至2017年间在欧洲和北美部署的基于载体的口服狂犬病病毒疫苗数量的发展。非欧洲ORV项目中使用的口服狂犬病疫苗的数据要么是从现有文献中检索到的,要么是由致谢中提到的人善意提供的。
替代,作为疫苗诱饵ONRAB®的一部分,表达RABV G(AdR 1.3)的具有复制能力的重组人腺病毒5能够在实验室和野外对目标动物中引发针对狂犬病的免疫应答。在2007年和2017年期间,加拿大和美国共发放了约2,850万个ONRAB®诱饵(图2和图3)。
虽然动物中的不良事件非常有限,并且据报道仅限于昏睡、腹泻和呕吐,但是暴露于病毒-RG与严重的皮肤炎症和在人类中引起系统性痘苗病毒感染的可能性相关。尝试使用无毒的改良型安卡拉痘苗病毒(MVA)作为骨架失败,因为口服后,它不能诱导足够的免疫反应。
载体疫苗的另一个缺点是预先存在的针对载体的免疫的潜在干扰,这可能抑制对推荐物的摄取并阻止产生足够的抗RABV免疫。事实上,它表明在欧洲的红狐和北美的浣熊中可检测到正痘病毒特异性抗体。在犬1型腺病毒(CAV-1)和CAV-2之间有大量交叉反应的背景下,针对犬腺病毒的抗体在野生犬中的流行排除了这些载体作为野生动物的潜在疫苗。在过去的几十年中,已经构建了多种其他载体病毒来表达狂犬病病毒基因(表2)。这些病毒载体包括几个病毒属和科,并且局限于大多数有希望的概念验证研究。到目前为止,除了病毒RG和ONRAB之外,没有一个经过长时间的广泛测试后获得了预防和控制野生动物狂犬病的许可。
基于反向遗传学的疫苗
自从开发出有效的减毒活疫苗以来,除了利用成熟载体的新疫苗制剂之外,反向遗传学继续塑造狂犬病疫苗发现和开发的领域。当前RNA病毒反向遗传系统利用RNA病毒生物学的多个共同特征。使用反向遗传技术制造疫苗的一种常见方法是利用质粒合成减毒病毒。这种技术的一大优点是,它能够通过定点诱变来靶向改变病毒基因组,即删除或插入选定的基因组序列和点突变。
对于减毒活疫苗,安全性是首要标准。根据世界卫生组织(World Health Organization,WHO)的建议,任何可用于野生动物免疫接种的口服狂犬病疫苗都不得在脑内感染后对免疫活性小鼠造成疾病。随后,为了进一步提高安全性或增强免疫原性,近年来使用反向遗传学开发了几种新的狂犬病疫苗病毒构建体(图1),也称为第三代口服狂犬病疫苗。
使用反向遗传学产生的绝大多数口服狂犬病疫苗构建体来自病毒构建体SAD L16,这是口服狂犬病病毒疫苗株SAD B19 的一个cDNA克隆,并产生一个名为SPBN的骨干病毒(该名称是限制性酶Sma、PacI、BsiWI和NheI的缩写)。基于这种骨干的病毒仍然显示出残留的致病性,特别是当鼻内给药时。因此,进一步的修改是必要的。疫苗构建体SPBN GAS,一种来源于SPBN遗传物质的构建体(Arg333变为Glu333),缺乏假基因(ψ),并在RABV G中显示出额外的改变,其中氨基酸(aa) Asn194被Ser取代。通过插入额外的一个(SPBN GASGAS)和两个(SPBN TriGAS)含有相同遗传修饰的相同G基因,可以进一步增强安全性。RABV G的这种过表达导致细胞凋亡和抗病毒免疫应答的增强。细胞色素c的过度表达导致免疫原性的强烈增加,伴随着显著的减少致病性,使SAD SPBN-细胞c(+)构建物成为活狂犬病病毒疫苗的候选物。今天,其他的SAD骨干(BNSP)已经建立了。
表2最终可用作野生动物口服狂犬病疫苗的载体病毒构建体概述
病毒家族
| 属 | 病毒种类
| 构建体名称 | 免疫原性的成分 | 接种方式 | 目标动物 |
痘病毒科
| 副痘病毒属
| 副痘病毒
| ORFV121RABV-G
| G-蛋白 | i.m .
| 牛,猪
|
D1701-V-RabG | G-蛋白 | i.m . 其他的 | 伴侣动物,其它 | |||
正痘病毒属
| 浣熊痘病毒
| RCN-G
| G-蛋白 | i.m . 粘膜
| 蝙蝠,其 它 | |
副粘病毒科
| 鸟新城疫病毒1
| rL-RVG
| G-蛋白 | i.m .
| 狗,猫
| |
呼吸病毒
| 人类呼吸道病毒5(副流感病毒5) | rPIV5-RV-G
| G-蛋白 | i.m .口服
| 老鼠,其它
| |
腺病毒科
| 哺乳动物腺病毒
| 人类腺病毒C(人类腺病毒类型5)
| Ad-0910G、Ad-0910N
| G-蛋白,N-蛋白
| 口服
| 貉
|
nrAd5-SRV9-G, nrAd5- Flury-LEP-G, nrAd5- BD06-G
|
G-蛋白 | i.m .
| 多种动物 | |||
HAd5-GB
| G-蛋白+鞭毛蛋白
| i.m . 口服 | 鼠,其它 | |||
human Ad5 HCMV–intron–ERA
| G-蛋白 | 口服 | 老鼠,狐狸,犬
| |||
犬腺病毒A(犬腺病毒2)
| CAV2-RVG
| G-蛋白 | 口服 | 浣熊,臭鼬
| ||
CAV-2-E3 -RGP
| G-蛋白 | 口头的
| 雪貂,其它野生动物
|
定点突变用于删除指定RABV磷酸蛋白aa 176-181的密码子(P)。产生的被称为SAD-DiND的构建体更有效地激活干扰素调节因子3 (IRF-3),从而阻止干扰素1型诱导。重组狂犬病毒构建体ORA-DPC用编码 G的 Arg333替换Asp333操作SAD和CVS 。此外,该构建体还在残基143至149或139至149中具有7-10 aa缺失,包含P蛋白中保守的LC8相互作用基序(K/RXTQT)。包括粒细胞巨噬细胞集落刺激因子(GM-CSF)在内的树突状细胞激活分子在狂犬病病毒中的表达被证明能增强对疫苗接种的先天和适应性免疫应答。将粒细胞集落刺激因子、细菌鞭毛蛋白和白细胞介素-15克隆到具有两个G蛋白突变的SAD B19毒株的重组减毒衍生物中,分别建体LBNSE粒细胞集落刺激因子、LBNSE鞭毛蛋白和LBNNSE白细胞介素-15产生了比亲本病毒更具免疫原性的病毒的病毒。
使用定点诱变的几乎相同的概念验证方法被用于在重组ERA (rERA)骨架中产生重组口服狂犬病病毒构建体(图1)。而衰减的ERA333 、rERAG333E和 ERAG3G疫苗构建体在G蛋白残基333处具有与 SAG2相同的突变,重组RABV ERA GS 中的遗传改变与SPBN GAS ((Asn194→Ser194; Arg333→ Glu333)。这些本质上相同的方法是否能被认为是狂犬病疫苗学领域的创新贡献,这是非常值得怀疑的。一个例外可能是ERA-N273/394-G333构建体,其在RABV的G和N蛋白中具有突变。该构建体是通过组合G333和N273/394 (Phe273→ Leu273和Tyr394 →His394))。
总之,除了ERA 333 和SPBN GASPAS之外,这些新开发的具有更高安全性的构建体都没有在许可框架内对潜在的野生动物目标和非目标物种进行过测试。
野生动物免疫的其它产品线
除了活疫苗之外,口服从重组杆状病毒感染细胞中获得的纯化RABV G在浣熊中诱导保护性免疫,但这一途径没有进一步探讨,也许是因为纯化的经济效益一般不划算,因为产生的保护性抗原数量少。另一种生产和递送疫苗抗原的技术是重组植物病毒颗粒。已经开发了几种表达RABV G或基于植物病毒的狂犬病疫苗的转基因植物,并在中进行了测试。通过口服途径给动物接种疫苗的其他可能性减毒活菌如沙门氏菌属、志贺氏菌属和李斯特氏菌属作为疫苗表达外源抗原的发展。尽管活的细菌载体疫苗的使用具有某些优点,例如相对容易以低成本制造和安全优点,并且尽管开发了几种用于口服递送疫苗的细菌载体,但是还没有尝试用于狂犬病。
DNA疫苗使用编码所需抗原的脱氧核糖核酸序列,在真核生物启动子的调控下,该抗原被插入细菌质粒,从而可以被转录成核糖核酸。然后将纯化的质粒直接接种到宿主体内,在宿主体内可以转染细胞。一旦进入宿主细胞的细胞核,该信使核糖核酸就被翻译成编码蛋白,并随后提交给免疫系统。迄今为止,尽管许多研究已经证明了基于DNA的狂犬病疫苗在诱导RABV特异性VNA和保护方面的相对有效性。
除了概念验证研究,几乎没有什么进展。由于只有口服疫苗对野生动物是可行的,质粒DNA可以在体外包装成病毒样颗粒(VLP),这在口服后也能引发免疫反应,这一事实似乎很有希望。
野生动物口服狂犬病疫苗的法律依据和要求
世界动物卫生组织提供了兽用疫苗生产的总体框架和野生动物口服狂犬病疫苗的相应要求。事实上,口服狂犬病疫苗的有效性和安全性标准最初是由世卫组织兽医公共卫生部讨论和确定的。监管机构(即欧洲医疗机构 和美国农业部( United States Department of Agriculture,USDA)也已在官方要求中规定了口服狂犬病疫苗的营销授权和/或许可指南,见第9篇《[联邦法规准则》。为了最大限度地减少在疫苗营销授权和/或许可框架内为不同国家的监管当局进行单独或额外研究的需要,建立了《兽医产品注册技术要求协调国际合作》( Internationa Cooperation onHarmonization of Technical Requirements for the Registration of Veterinary Medicinal ProductsVICH)。迄今为止,欧洲联盟、美国和日本正在参加VICH会议,关于协调的谈判正在进行中。
实验室条件下进行的研究应按照良好实验室规范的原则进行和管理(Good Laboratory Practices,GLP),而现场安全性研究应按照VICH良好临床规范(GCP) 的原则进行。这同样适用于相应的商业产品的制造过程,这些产品也必须处于GMP(类似)条件下。
原则上,野生动物口服疫苗应该在各自的目标物种中证明它们的免疫原性和效力。对于功效测试接种疫苗的动物,至少25只动物应被用作疫苗。接受挑战性试验的标准应是至少80%的对照动物死于狂犬病,而至少22/25、26/30或统计上同等数量的疫苗(如果使用了更多数量的疫苗)应能在强毒狂犬病病毒挑战后存活90天。仍然有一些偏差,例如,在欧洲专论中,挑战的时间点是接种疫苗后180天,美国的许可要求是接种疫苗后365天后的挑战。
由于该产品是一种具有复制能力的活病毒,因此疫苗的安全性非常重要,应在目标和非目标物种中进行评估。对非目标物种的特殊关注是口服狂犬病疫苗所独有的,因为诱饵是在无人监管的情况下分发的,任何感兴趣的动物都可以找到并食用。这使得很难确定疫苗应该在哪些物种中进行测试,因为疫苗被用于许多不同动物物种居住的许多不同栖息地。此外,对于重组疫苗,在现场使用之前,应对动物、人类和环境的风险进行风险评估。
由于免疫原性和效力直接受疫苗病毒滴度的影响,在上市前应确定最低有效滴度,代表能保护100%目标实验动物免受强毒狂犬病攻击的疫苗最低滴度。为了补偿在环境中分配后的滴度损失,疫苗诱饵中的分批释放滴度应该高于最低有效滴度。
口服疫苗的另一个影响因素是诱饵的浓度。诱饵基质应在野外条件下保持几天的热稳定性,如果其保持其原始形状,则评估其稳定性。
讨论
毫无疑问,口服狂犬病疫苗在控制北半球野生动物的狂犬病方面已经获得了很大的声誉。在过去的40年中,这些疫苗与明确的疫苗接种策略相结合,为在西欧、中欧和北美的广大地区消除红狐介导的狂犬病奠定了基础。直到大约2011年,10个欧洲国家由于长期和大规模实施ORV计划而自我宣布没有狂犬病,近年来,爱沙尼亚(2013年)、拉托维亚(2015年)和斯洛文尼亚(2016年)加入了欧洲无狂犬病国家的行列。根据OIE的定义,另外三个国家,包括斯洛伐克、立陶宛和克罗地亚,符合无狂犬病标准( http://www.oie.int/index.php? id¼169&L¼0&htmfile¼chapitre_rabies.htm)。
而在北美,基于载体的口服狂犬病疫苗对于消除郊狼和灰狐狸的狂犬病至关重要,它们在控制浣熊和臭鼬介导的狂犬病方面仍然发挥着重要作用。
然而,前面仍有障碍,例如,从实践、科学和监管的角度来看。实际上,如果相关的诱饵不容易被目标物种接受,最好的疫苗构建就不起作用。在这方面,人们试图修改标准诱饵,以提高除狐狸以外的其他物种的诱饵成功率。最近在台湾岛的台湾獾身上出现的狂犬病和用各种配方进行的诱饵试验表明,当使用为一个特定目标物种开发和优化的诱饵对付其他物种时,存在困难。除了更有效的口服狂犬病疫苗和物种特异性诱饵外,为这些储存宿主开发有效的诱饵投放和疫苗接种策略仍是一项艰巨的任务。
令人惊讶的是,在经历了几十年的ORV之后,口服疫苗引发免疫反应的确切机制仍然知之甚少。特别的挑战是,在不同的储存宿主中,尤其是浣熊和臭鼬,在ORV之后,诱导针对狂犬病的保护性免疫反应所需的疫苗滴度的差异。对红狐和臭鼬的研究表明,腭扁桃体在疫苗病毒摄取中起着关键作用。臭鼬的腭扁桃体中缺乏病毒感染细胞表明疫苗病毒的吸收或感染效率较低,这可能导致对口服疫苗接种的较低反应性。需要进一步的研究来阐明那些对口服疫苗相当难的物种的机制。
安全性和/或免疫原性更强的疫苗的最初目标在某种程度上与监管障碍相矛盾,无论是许可还是在该领域的实际应用。例如,尽管基于载体的口服狂犬病疫苗和基于反向遗传学的口服狂犬病疫苗都是转基因生物,但不管它们的安全性如何,它们的使用经常受到争议。风险评估需要评估插入的外源序列/转基因,它们在人群和环境中的再转化、重组和传播能力。这同样适用于基于植物的疫苗,这种疫苗能够在口服后保护绵羊免受狂犬病的攻击。
因为狂犬病是一种致命的疾病,对于口服减毒狂犬病活疫苗来说,对目标和非目标人群(人类和竞争性物种)的安全性至关重要。事实上,在一个方面或另一个方面,第一代和第二代基于载体的口服狂犬病疫苗都没有完全满足口服狂犬病疫苗在对目标和非目标物种的无毒性、遗传稳定性和没有活病毒的排泄方面的要求。为此,已经应用了不同的方法(如本章所述)来开发用于中食肉动物口服疫苗的高度减毒狂犬病病毒疫苗。在这方面,虽然第三代口服狂犬病疫苗的安全性已得到证实,但其他候选疫苗的安全性仍有待评估。无论如何,确定和改善安全性和有效性之间的平衡是一件微妙的事情,因为由于疫苗病毒的复制适应性降低,增强的减毒或过度减毒将有丧失免疫原性的风险。
开发野生动物疫苗的开创性工作也在保护方面有所帮助。狂犬病不仅是一个重要的公共和兽医卫生负担,但它也可以威胁到濒危野生动物物种[202],如花果狸,非洲野犬和埃塞俄比亚狼(西尼斯犬)。对于后两种物种,野生动物狂犬病疫苗接种计划的目标不是消除感染,而是保护这些高度濒危物种。
流浪犬和野犬也是使用注射疫苗控制狂犬病的一个挑战。为此,与野生动物相似,ORV可能有助于提高这些犬的群体免疫力,使其达到阻断狂犬病传播周期的水平。
致谢:
本章节:Rabies Vaccines for Wildlife
作者:T. Müller and C. M. Freuling
来源:本内容翻译自《Rabies and Rabies Vaccines》,翻译该章节完全出于个人兴趣,不用做其它。
原书:ISBN 978-3-030-21083-0 ISBN 978-3-030-21084-7 (eBook) https://doi.org/10.1007/978-3-030-21084-7
翻译:孟胜利
https://blog.sciencenet.cn/blog-55647-1240511.html
上一篇:141 被狗咬伤得狂犬病的概率有多高
下一篇:143 接种狂犬病疫苗期间有哪些禁忌吗