博文
和疾病赛跑!癌症患者的诊断救星:数字PCR技术
 精选
精选
|||

精准医疗(Precision Medicine)是一种将个人基因、环境与生活习惯差异考虑在内的疾病预防与治疗的新领域。2015年1月,时任美国总统奥巴马在国情咨文中提出“精准医学计划”,同年2月,中国成立精准医疗战略专家组,这标志着“精准医疗”计划同时在两个国家启动。15年6月,国家卫计委发布《肿瘤个体化治疗检测技术指南》,数字PCR技术也是九种肿瘤个体化检测技术之一。
2015年9月,MIT Technology Review 杂志发布了“2015 年度十大突破技术(Breakthrough Technologies2015)”,与肿瘤个性化医疗密切相关的“液体活检(Liquid Biopsy)”名列其中。液体活检在转化医学研究中是一个快速扩张的领域,对于癌症病人的个性化医疗过程的多个环节具有重要意义,可用于早期诊断、转移复发或进展的风险评估、疗效实时监测、用药靶点和耐药机制的鉴定,也有助于探明肿瘤在病人中的转移过程。几乎所有的体液都可用于液体活检,包括全血、血清、血浆、唾液、胸腔积水、腹水、脑脊液、尿液、眼泪、痰液等等,因此液体活检具有极大的临床应用范围和深远的意义。
“液态活检”的概念其实就解决了一个问题:新的检测样品。因为以“血液循环肿瘤DNA”(cfDNA或ctDNA)为检测对象,能很好地克服部分情况下病症组织难以获得的困难,样品的收集是无创或微创的,可以随时采样,对病灶相关生物标志物实时掌握,解决了肿瘤进展及治疗过程中时间维度上的异质性;血液内的ctDNA能综合地反映肿瘤整体情况,排除空间上的异质性。目前已经有相当数量的文献对于不同肿瘤的研究证实,血液ctDNA的检测与组织样品的检测呈现非常好的相关性,换句话说,通过血液样品中ctDNA的分析能够反映病灶肿瘤细胞的整体水平。
1997年,Dennis Lo通过普通PCR扩增的方法证明了胎儿游离DNA的存在,该发现奠定了日后通过母体血浆中胎儿游离DNA的分析进行无创产前检测(Non-invasive Prenatal Testing,NIPT)的基础。早期对胎儿游离DNA的检测主要集中在对父源性特异序列的定性分析,如果在母体血浆中检测到这些靶标序列,那就证明胎儿经遗传获得了父本的特异性序列。该策略的一个早期应用是通过RHD基因的序列分析进行Rh阴性血怀孕妇女的监控。
目前通过对父源性血浆游离DNA的分析进行NIPT,已经扩展到常染色体显性遗传类疾病,如软骨发育不全、肌强直性营养不良和亨廷顿氏舞蹈症等。但该策略不能应用于其他遗传模式的疾病,诸如母源性导致的常染色体显性遗传类疾病、常染色体隐性遗传类疾病和染色体的非整倍性疾病。因为这些情况下,无论胎儿是否获得致病序列,在血浆内都能检测到来源于母体的靶标序列。因此需要更精确的检测技术及更强大的数据处理方式。
疾病超早期诊断 ——“液体活检”
随着研究的展开,很多实验室发现基于数字PCR对诸如血液、痰液、尿液等体液样品中核酸水平的疾病相关标记分子(DNA、mtDNA、miRNA等)的检测,其发现疾病的时间远早于影像学或其他蛋白类标记物的相关检测,大大提前了疾病发现和治疗的窗口期,更好地实现对疾病的早发现,早治疗。
肿瘤是一类多阶段、多基因变异累积导致的复杂病变,正常细胞向癌细胞恶性转化过程需要十余年甚至更长时间。在肿瘤形成的超早期,就会出现肿瘤细胞的坏死和凋亡,这些凋亡或坏死的肿瘤细胞会释放其DNA进入外周血形成游离的肿瘤DNA,因此通过分析循环血液中是否含有肿瘤特异的游离DNA可以达到肿瘤早期筛查的目的。利用数字PCR技术对外周血中肿瘤游离DNA进行检测,对肿瘤的发现要远早于影像学及其他蛋白或多糖类肿瘤标记物的检测手段。被检测者可在肿瘤形成的启动阶段就采取相应的干预措施,阻止和减缓肿瘤的恶化过程。总之,通过高灵敏的检测技术,对肿瘤组织、胸腹腔积液、外周血、尿液、痰液等可重复取样的体液标本进行肿瘤标志物的无创检测逐渐受到人们的认可和重视。
然而肿瘤的体液样本和组织样本,往往呈异质性,即样本中同时含有正常体细胞DNA和癌细胞 DNA,且正常体细胞DNA的量是远大于肿瘤细胞DNA的,往往会干扰和湮没肿瘤细胞DNA的检测信号。数字PCR系统通过对样本的分液处理,能在每个微反应单元中有效的降低正常体细胞DNA背景的干扰,不仅能实现对肿瘤标记物的有效检测,还能定量监测突变频率变化,量化检测标准。目前已有大量文献和实例报道了数字PCR技术成功应用于EGFR、KARS、BRAF、PIK3CA、DNMT3A等各种涉癌基因突变检测以及癌症相关的如HER2基因扩增检测。
国内外已有医学检验中心相继开发出以数字PCR技术为平台的肿瘤继发性耐药无创检测和恶性肿瘤无创实时监控(Cell free circulating tumor DNA)等检测产品与项目。
血液中cfDNA的释放和提取见图1。
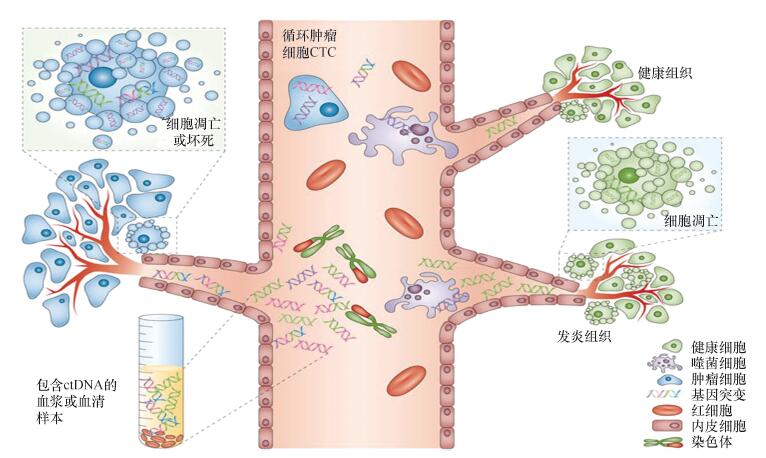
图1 血液中cfDNA的释放和提取
随着研究的深入,越来越多的疾病分子标志物被发现,并成为治疗的预后和疗效评价的有效指标。例如通过数字PCR定量分析BCR-ABL1融合序列拷贝数以检测慢性髓细胞性白血病CML微小残留病,评估疗效和预后;通过数字PCR检测PIK3CA突变,定量分析乳腺癌化疗或手术治疗后微小残留病,以评估复发风险;通过检测器官移植后受体外周血中的供体cfDNA含量作为早期器官排异反应的预警指标;通过检测血清中非甲基化状态INS基因的比例来判断胰岛β细胞的死亡情况,从而帮助临床掌握糖尿病的发展情况;病毒抗逆转录治疗后残留病毒量的检测等。
对于液体活检样本,数字PCR不仅能够检测出含量极低的突变,还能精确计算出每一种突变的频率。Day等人就对数字PCR超高的突变检测灵敏度在突变等位基因频率(MAF)检测方面的应用进行了研究和分析。如图2所示,对于每一种肺癌中常见的EGFR突变(例如导致对TKIs靶向药物敏感的L858R突变和造成对TKIs药物产生抗性的T790M突变),图2A所示为仅含有L858R突变而不含T790M突变的肿瘤组织,传统sanger测序(灵敏度为20%~30%)即可检测出该突变;图2B中,肿瘤组织常常出现含有T790M突变的局部细胞克隆,这样的稀有突变需要灵敏度更高的检测手段方能检出;图2C为另一种可能出现的情况,肿瘤中存在三种局部细胞克隆,但占优势的正常细胞克隆不含有任何EGFR突变。当前针对上述三种情况的癌症普遍采用相同的靶向治疗方案,但是这三种肺癌对EGFR TKIs靶向药物的反应却有很大差异。数字PCR技术结合“液体活检”的理念就可以很好地解决上述问题,实现对肿瘤的实时动态基因分型,从而为个体化用药和预后提供必要信息。

图2 利用数字PCR检测等位基因突变频率及灵敏度
慢性粒细胞白血病是一种发生于造血干细胞的增生性疾病,受累的细胞系中可以找到bcr/ab基因重排,针对bcr/abl靶点的药物有伊马替尼、TKIs等。白血病患者经过化疗达到完全缓解仍会复发,这是因为髓外某些隐蔽处仍残留白血病细胞,为了彻底治疗白血病,不仅要及时发现,还要对其进行定量检测以指导治疗判断预后。在慢性白血病治疗中,使用实时荧光定量RT-PCR是常规临床检查手段,经分子水平检测完全缓解后停用靶向药物,大约60%患者复发。这是因为实时荧光定量RT-PCR对bcr/abl融合基因检测灵敏度不够高。对bcr/abl进行RT-ddPCR定量分析的研究证实了RT-ddPCR较实时荧光定量RT-PCR具有更低的检测下限,可以更精细的帮助临床医生把握停止使用TKIs时间,减少复发几率,并且操作更简单。
miRNA是一类内源性的具有调控功能的非编码RNA,他们参与调节细胞功能,并且稳定的存在于外周循环中,可发展为癌症早期检测的生物标志物。qPCR已被广泛用于血液样品miRNA的分析测试,但研究人员发现,血清或血浆中的miRNA qPCR测量出现了极高的差异性,无法用作稳定的血液生物标志物的检测标准,因此,研究人员寻求一种能获得更可靠结果的新方法。有学者表示,在循环系统miRNA诊断领域,数字PCR可以帮助他们进行生物标记物研究,直接比较同一实验室跨天多次试验,甚至不同实验室之间的检测结果。对低丰度的血浆miRNA的绝对定量是qPCR的巨大挑战。一项头对头的研究,分别用qPCR和液滴式数字PCR量化36例肺癌患者和38名健康对照血浆中miRNA-21-5p(血浆相对高丰度)和miRNA-335-3p(相对低丰度)的拷贝数。液滴式数字PCR能检测并计数miR-21-5p和miR-335-3p的拷贝数,而定量PCR仅能检测miR-21-5p的存在,从而表明液滴式数字PCR在微量miRNAs的检测灵敏性和拷贝数的精确定量有优势。微量miRNAs即使在复杂背景中仍然可以被数字PCR精确计数。Hindson等人对血清miRNA进行qPCR和数字PCR并列比较检测,他们收集了20例晚期前列腺癌患者和20例年龄相匹配的男性对照血清样品,分析其中的miR-141丰度,miR-141是一种已被证明的晚期前列腺癌的生物标志物。研究人员分别在不同的时间里准备了用于qPCR和数字PCR分析的不同稀释浓度的样品,并进行了检测,结果发现数字PCR相比于qPCR,重复性提高了7倍,这在对照研究中也得到了证实,数字PCR的结果更为可信(P=0.0036 vs P=0.1199),如图3、4所示。
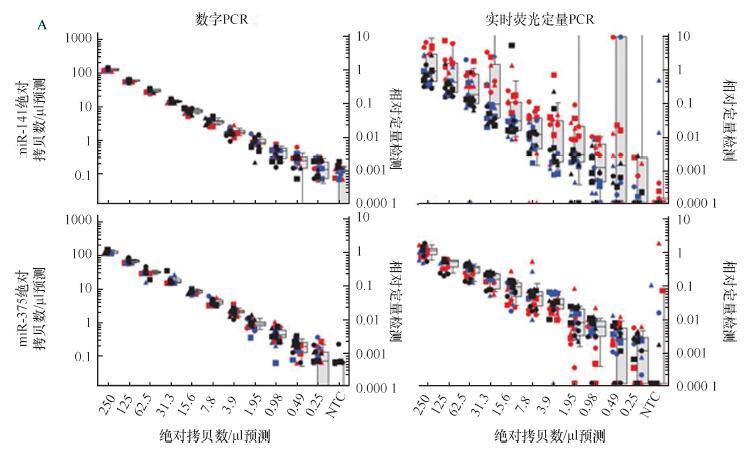
图3 数字PCR与RT-PCRmiRNA定量检测
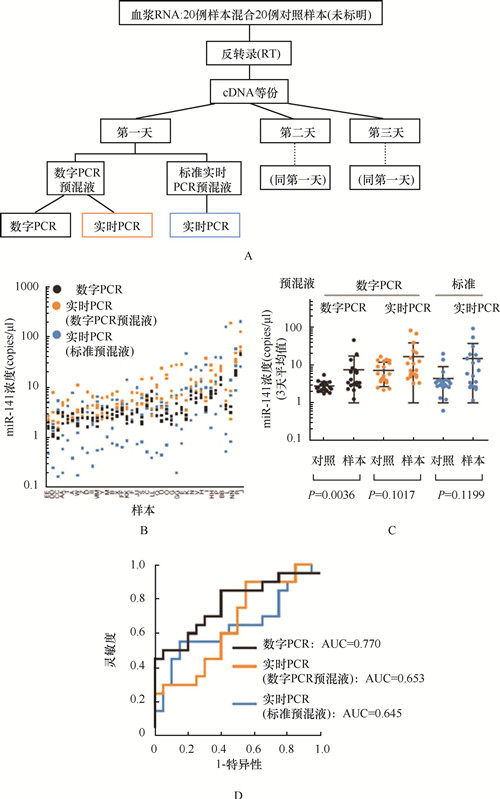
图4 数字PCR与qPCR循环miRNA定量检测

责编:郝文娜,杨卫华
北京:科学出版社,2017.4
ISBN:978-7-03-052065-4
数字PCR以聚合酶链式反应的理论和技术体系为基础,结合现代微机电和光学检测技术,实现单分子水平的核酸精确定量检测。数字PCR作为第三代PCR技术,是实时荧光定量PCR原理与现代微机电、微纳制造工程技术相结合的典范。数字PCR的核心是将核酸样品平行划分为大规模单分子水平的微反应单元,然后对众多微反应单元内的靶序列进行扩增和光学检测,实现绝对定量和痕量分析。
《数字PCR——原理、技术及应用》重点介绍了数字PCR的原理和技术特征、仪器系统、实验设计、数据处理和典型应用及最新科研进展。拓展介绍了一些实验细节、微流控工程知识。
(本期责编:李文超)

一起阅读科学!
科学出版社│微信ID:sciencepress-cspm
专业品质 学术价值
原创好读 科学品味
点击文中书名、作者、封面可购买本书。
https://blog.sciencenet.cn/blog-528739-1054485.html
上一篇:《中国科学: 物理学 力学 天文学》(中英文版)2016年度优秀论文奖
下一篇:如何从遗传角度科学地证明你是你?
