博文
高效且安全的新冠病毒疫苗:用狂犬病毒作载体
||
高效且安全的新冠病毒疫苗:用狂犬病毒作载体
据10月16日发表在Nature杂志的子刊Vaccines上的研究论文(见参考文献),美国费城托马斯-杰斐逊( Thomas Jefferson)大学的研究人员已快速开发出一种新型、高效、安全的SARS-CoV-2(新冠病毒)疫苗CORAVAX™,该疫苗用一种经特殊改造的狂犬病毒为载体,含有SARS-CoV-2 剌突(spike) 蛋白S1。该疫苗有许多独特的有价值的优点。该疫苗可同时提供针对狂犬病毒和新冠病毒的保护作用,在作为减毒活疫苗或化学灭活的疫苗使用时都是安全的,都能诱导高效价的病毒中和抗体(VNA),抗体水平比恢复期患者血清中的抗体水平还要高得多。此外,由于RABV疫苗通常能提供终身免疫,该疫苗针对SARS-CoV-2免疫应答的长期稳定性还将在未来的研究中继续进行评估。综上所述,本项研究的结果为进一步开发这一安全且已牢固建立的COVID-19(新冠肺炎)疫苗平台提供了依据。
前言
在导致人类呼吸系统疾病的7种冠状病毒中,有4种(229E、NL63、OC43和HKU1)只引起轻度感染,另有 3种(SARS-CoV、MERS-CoV和SARS-CoV-2)则是高致病性病毒。SARS-CoV-2很可能起源于蝙蝠,并通过中间动物宿主传播给人类,这在其他高致病性人冠状病毒MERS-CoV(中东呼吸綜合症冠狀病毒)和SARS-CoV中已经得到证明。
决定SARS-CoV-2的高传播性和致病性的分子机制目前仍然还只是推测,但S蛋白上的突变导致新增Furin 蛋白酶切位点,以及在受体结合区段的突变允许S蛋白结合人血管紧张素转换酶(ACE2)似乎是关键/重要因素。这些分子特征的存在使得SARS-CoV-2成为三种高致病性冠状病毒中最容易传播的一种。与SARS不同的是,SARS-CoV-2可能不会被消除(eliminated),而且在有效疫苗出现之前很难得到有效控制。
已经发现ACE2受体介导SARS-CoV-2和其他冠状病毒进入细胞,包括NL63和SARS-CoV, 后者与SARS-CoV-2有76%的氨基酸同源。表达ACE2的细胞对SARS-CoV-2 的S糖蛋白敏感,这些糖蛋白镶嵌在SARS-CoV-2病毒粒子外膜表面,可用作ACE2的配体( ligands)。在人类,中和抗体和/或T细胞免疫反应针对几种SARS-CoV-2蛋白,但主要针对S蛋白,这表明S蛋白特异性免疫反应在对宿主的免疫保护中发挥重要作用。因此,目前大多数疫苗使用SARS-CoV 的S蛋白或其一部分,作为疫苗的免疫原。
目前至少有139种不同的COVID-19疫苗正处于临床前开发阶段;其中30个正在进行临床试验。这些疫苗分别属于三种不同平台中的一种:基于DNA或RNA的合成疫苗;病毒样颗粒;表达SARS-CoV-2部分基因的灭活病毒粒子或病毒载体。
虽然目前尚未确定一种有效的候选疫苗,但最有希望的候选疫苗都有望诱导病毒中和抗体(VNA),这种抗体已被描述为能提供针对冠状病毒的保护作用的标志。
实验结果
基于之前对MERS-CoV(中东呼吸綜合症冠狀病毒)的研究,作者们将SARS-CoV-2 的S1蛋白和一个额外的狂犬病毒G蛋白(RABV-G)引入到减毒的RABV载体中(见下图),构建的疫苗命名为CORAVAX™。
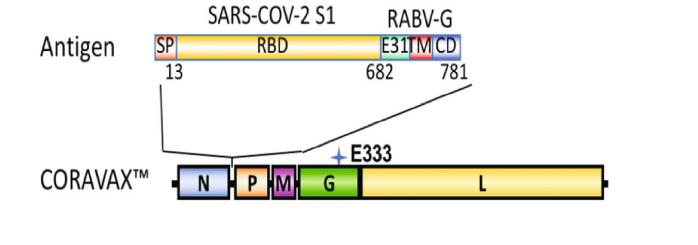
所使用的RABV疫苗载体来源于减毒RABV的SAD-B19疫苗株。为了提高亲本的安全性和使外源基因的表达最大化,曾对亲本进行了一些修饰。通过对RABV 的N和P基因间外源抗原的表达以及对人类细胞靶基因密码子的优化,外源抗原的表达水平达到最高。
早先的研究用MERS-CoV的全长S蛋白基因,结果表明,全长的冠状病毒S蛋白会显著降低病毒滴度,所以采用SARS-CoV-2 S蛋白的S1亚单位。更重要的是,S1区段包含的受体结合域( receptor-binding domain,RBD)的保守程度不如S2融合域(fusion domain),这两者与冠状病毒的同一性分别是64%和90%。
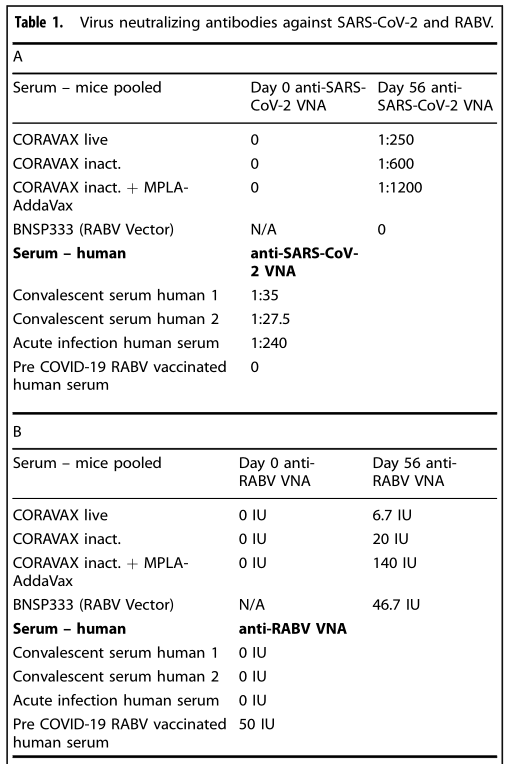
CORAVAX疫苗免疫小鼠的血清可同时中和SARS-CoV-2和RABV。采用中和试验分析了免疫0天和56天后小鼠的混合血清对Vero细胞培养的SARS-CoV-2的中和活性。通过免疫染色检测SARS-CoV-2感染,显示的能检测到病毒时血清的最低稀释倍数为两个独立实验的平均值(见下表,A组)。狂犬病中和滴度采用RFFIT测定并以国际单位(IU)表示(见下表,B组)。
讨论
这项临床前研究的结果表明,CORAVAX是一种很好的抗COVID-19候选疫苗。
虽然目前已有几种候选SARS-CoV-2疫苗处于临床试验的后期,但对其有效性的担忧仍然存在。有人担心,由于对COVID-19疫苗的迫切需求,一些疫苗在没有足够免疫原性的情况下进行了人体试验,可能还需要对抗体介导的病理学作进一步的研究。
最先进的mRNA疫苗目前还没有动物数据或临床评估发表,相关信息只能依赖于相关公司的新闻稿。有两个小组用DNA疫苗平台测试了它们在小鼠、豚鼠和NHPs(Nonhuman Primate,非人灵长类)中的疫苗反应,证明可激发免疫原性,但VNA(病毒中和抗体)滴度较低。另一种主要候选病毒,表达SARS-CoV S蛋白的腺病毒5型(Ad5)载体,已证明具有免疫原性,但在人体内诱导的VNA滴度较低。在另一项研究中,接种了ChAdOx1 nCoV-19(以腺病毒为载体的疫苗)的 NHPs(非人灵长类)随后用SARS-CoV-2进行攻毒,在动物的鼻拭子中仍然有一些病毒RNA残留,这引起了人们对接种疫苗的人仍然具有传染性的担忧。另一个要考虑的因素是诱导免疫反应的持续时间(寿命)。早先分析的基于腺病毒载体的EBOV(Ebola病毒)疫苗未能诱导长期免疫,免疫三个月后,对EBOV的保护反应减弱,需要用一种不相关的疫苗载体进行增强。
使用S1结构域,而不是全长S蛋白,可能会避免与S2特异性非中和抗体结合,从而可避免炎症反应增强可能导致的严重病理后果。某些抗体-病毒免疫复合物可与肺泡巨噬细胞上活化的Fc受体结合,诱导IL-6、CCL2等促炎因子的表达。抗体-病毒免疫复合物也可激活补体系统,进一步加剧炎症。
早先的研究表明,超过90%的人已经具有抗四种人类冠状病毒(HCoVs,如229E、OC43、NL63、HKU1) 的抗体。这四种人冠状病毒与SARS-CoV-2 S2结构域之间的几个高度保守区段是交叉反应抗体的潜在靶点。因此,用SARS-CoV-2 的S蛋白免疫可能增强这些保守的抗原表位(epitopes),并阻止对S1区段新的抗原表位的应答。
虽然没有在冠状病毒中观察到,但早先已经证明,曾暴露于黄病毒(flaviviruses)的人预先存在的免疫力可以显著改变他们对未来黄病毒感染的B细胞反应。
除了疫苗的免疫原性外,在人体内使用COVID-19疫苗还需要考虑两个问题:如早先所见的与RSV(呼吸道合胞病毒)相关的抗体依赖性增强(antibody-dependent enhancement,ADE)和疫苗相关的增强型呼吸道疾病(vaccine-associated enhanced respiratory disease,VAERD)。虽然很少有证据表明冠状病毒中存在ADE,可能是因为巨噬细胞不是人冠状病毒的主要靶标,但存在对VAERD的担忧。接种用改良痘苗病毒安卡拉(MVA)株构建的疫苗以后,所诱导产生的S特异性免疫导致感染SARS-CoV的中国猕猴发生严重的急性肺损伤( acute lung injury,ALI),与载体MVA对照的结果相似。在进行大规模的人类疫苗接种之前,需要在动物系统中解决这些可能的不良反应。
除基于VSV(水疱性口炎病毒)的EBOV(Ebola virus )活疫苗外,开发基于病毒载体的疫苗的成功率一直很低。CORAVAX的显著优势在于,它是一种基于狂犬病毒载体的灭活疫苗,已安全有效地用于孕妇、儿童、老年人以及免疫功能低下者,并能引发持久反应(CDC、MMWR)。此外,在NHP( 非人灵长类)研究中,狂犬病毒载体EBOV(埃博拉病毒)灭活疫苗FiloRab1对EBOV攻毒提供了100%的保护。总之,作者开发出了一种在动物模型中具有高度免疫原性的新型COVID-19疫苗,诱导的VNA滴度明显高于人恢复期血清的VNA滴度。
虽然作为首次概念验证性研究,本次试验使用了高剂量的活病毒(10 7 ffu),但对于低剂量的活病毒和不同数量的灭活疫苗的研究,随后将继续进行。值得注意的是,最近对腺病毒或DNA疫苗的研究分别使用了高达10 11 pfu的病毒滴度和高达100微克的RNA。为了达到保护目的,目前正在进一步鉴定不同疫苗剂量和接种日程安排对免疫反应的影响,分析潜在的毒性。目前试验用疫苗已经生产出来。第一期临床试验预计将于2020年10月开始。
参考文献:
Kurup, D., et al. Rabies virus-based COVID-19 vaccine CORAVAX™ induces high levels of neutralizing antibodies against SARS-CoV-2. npj Vaccines 5, 98 (2020). https://doi.org/10.1038/s41541-020-00248-6
https://blog.sciencenet.cn/blog-347754-1257457.html
上一篇:哈尔滨主城区狂犬病疫苗告罄? 疫苗滥用的恶果!疫苗滥用的黑样板!
下一篇:T淋巴细胞对冠状病毒感染的反应:情况相当复杂