博文
高精度3D打印生物支架定制
||

01 片状支架
高精度膜片

多尺度膜片

高精度图案

02 管状支架
高精度管道
类血管支架
可定制参数
03 应用案例
细胞行为研究
常规的3D打印聚合物,精度只能控制在100-200微米数量级,而近场直写打印的支架精度为3-50微米(接近细胞尺度),可以很好地促进细胞粘附、增殖、分化及定向,可用于纯结构调控细胞行为研究。
细胞膜片构建
结构诱导细胞定向
器官芯片构建
高精度支架作为柔性线框模具,可实现微纳尺度的高效制造,方便灵活地制造微流控芯片,用于细胞定向、细胞图案化、器官芯片研究。
凝胶芯片制造及细胞定向诱导

多尺度血管芯片制造
水凝胶增强
针对软组织修复用水凝胶无法满足强度、韧性和缝合性要求的瓶颈,利用高精度支架作为结构增强相,基于协同增强效应来提高水凝胶的力学性能,提高组织修复成功率。
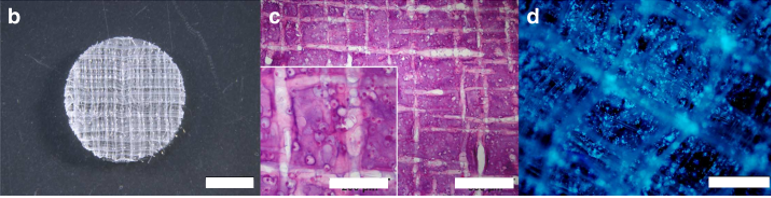
高精度支架复合GelMA水凝胶用于软骨修复

高精度支架复合fibrin水凝胶用于瓣膜修复
参考文献
[1] Xie Chaoqi, Gao Qing, Wang Peng, et al. Structure-inducedcell growth by 3D printing of heterogeneous scaffolds with ultrafine fibers.Materials & Design, 2019.
[2]Gao Qing, Xie Chaoqi, WangPeng, et al. 3D printed multi-scale scaffolds with ultrafine fibers for providingexcellent biocompatibility. Materials Science and Engineering: C, 2019.
[3] Jin Yuan, Gao Qing, Xie Chaoqi, et al.Fabricationof heterogeneous scaffolds using melt electrospinning writing: Design and optimization. Materials & Design, 2019.
[4] Lv Shang, Nie Jing, Gao Qing, et al. Micro/nanofabrication of brittle hydrogels using 3D printed soft ultrafine fiber moldsfor damage-free demolding. Biofabrication, 2019.
[5] Nie Jing,Gao Qing, Xie Chaoqi, et al. Construction of multi-scalevascular chips and modelling of the interaction between tumours and bloodvessels. Materials Horizons, 2019.
[6] ArielA. Szklanny, Lior Debbi, Uri Merdler, et al. High-Throughput Scaffold Systemfor Studying the Effect of Local Geometry and Topology on the Development and Orientationof Sprouting Blood Vessels. Advanced Functional Materials, 2019.
[7]JetzeVisser, Ferry P.W. Melchels, June E. Jeon, et al. Reinforcement of hydrogelsusing three-dimensionally printed microfibers. Nature Communications, 2015.
[8] Navid T. Saidy, Frederic Wolf, Onur Bas, et al. BiologicallyInspired Scaffolds for Heart Valve Tissue Engineering via Melt Electrowriting.Small, 2019.
https://blog.sciencenet.cn/blog-3427880-1233560.html
上一篇:AFM:悬浮支撑打印类软骨组织