博文
肿瘤免疫治疗后为何会复发?中国医学科学院黄波团队破解T细胞耗竭之谜
||
北京时间2021年1月12日凌晨0时,中国医学科学院黄波团队在《自然—免疫》在线发表论文——“IL-2 regulates tumor-reactive CD8+ T cell exhaustion by activating the aryl hydrocarbon receptor”。
该研究发现,肿瘤部位细胞因子IL-2是诱导杀肿瘤的CD8+ T细胞进入耗竭的驱动因子。

当前,以抗PD-1及抗CTLA-4抗体为代表的免疫检查点疗法,在临床实体肿瘤治疗上实现“0”到“1”的突破,也开创肿瘤免疫治疗新篇章。与之相呼应,采用人工嵌和受体的CAR-T细胞回输治疗B细胞白血病,更是取得空前成功。
鉴于肿瘤免疫治疗具有特异高效,并使机体免于伤害性治疗等优点,业内专家认为,随着肿瘤免疫学理论的深入研究和技术的不断进步,其有望实现根治肿瘤的新突破,成为肿瘤治疗的主流方法。
然而,即便这些疗法效果良好,大部分病人治疗后依然会复发。弄清楚其背后的原因,是目前肿瘤免疫治疗领域最急迫的科学问题。
所谓的肿瘤免疫治疗是通过主动或被动方式使机体产生肿瘤特异性免疫应答,发挥其抑制和杀伤肿瘤功能的治疗方法。其主要包括免疫检查点抑制剂(ICB)、过继性细胞转移疗法(ACT)、肿瘤特异性疫苗、小分子免疫药物等。
“这种治疗方法主要依赖活化的T细胞对肿瘤细胞的杀伤,其核心是T细胞。而当前无论是免疫检查点疗法还是CAR-T 细胞疗法都是通过增强肿瘤特异性T细胞的杀伤功能实现的。”中国医学科学院基础医学研究所研究员黄波表示,杀肿瘤的T细胞在对肿瘤细胞杀伤过程中,会逐渐进入一种过渡疲劳的状态,从而丧失杀肿瘤细胞的能力,免疫学上将之称为T细胞耗竭。
由此可见,阻断T细胞耗竭或者逆转耗竭的T细胞,使其恢复先前杀肿瘤细胞的能力,是提升临床肿瘤免疫治疗的一个关键点。然而至今为止,T细胞耗竭的始动因素还是一个谜。
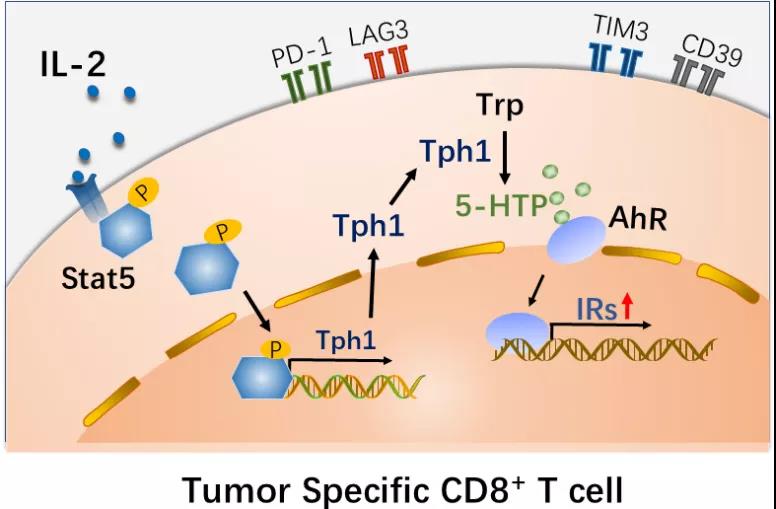
黄波团队的最新研究则揭开了这一谜团。该论文的第一作者、中国医学科学院基础医学研究所副研究员刘玉英表示,IL-2是免疫学研究领域的核心细胞因子,其为T细胞增殖、生长提供关键信号。研究发现,IL-2能够提供激活STAT5的信号, 诱导CD8+ T细胞大量合成色氨酸羟化酶1(TPH1),此酶催化色氨酸生成羟色氨酸(5HTP),而5HTP结合芳香烃碳氢化合物受体(AhR),促进AhR入核,其直接上调免疫抑制性受体(IR),如PD-1、 TIM3、 LAG3、CD39等的表达,从而诱导T细胞耗竭。
此外,研究团队还发现,肿瘤部位导致T细胞耗竭的IL-2主要来源于CD4+ T细胞。这种T细胞耗竭机制的阐明,再次提示机体免疫系统的复杂与阴阳两面性。
在审稿环节中,审稿人提出了一个非常重要的问题:业内普遍认为IL-2是促进T细胞生长的因子,为什么此项研究却提出IL-2导致T细胞衰竭呢?
为此,研究团队设计了一系列的实验,比如分别在肿瘤早期以及晚期给与抗IL-2抗体治疗,观测肿瘤生长情况,以此推测IL-2在肿瘤发展过程中的作用。
“我们发现,在肿瘤早期,阻断IL-2信号,能促进肿瘤生长,这提示早期IL-2信号发挥抗肿瘤的作用。但是在肿瘤中晚期,阻断IL-2信号,则能抑制肿瘤生长,这又提示IL-2有抑制性功能。”刘玉英表示。
“这项研究工作回答了肿瘤免疫非常核心的基本问题,不仅对当前的肿瘤免疫治疗具有指导意义,而且还有助于发展新的肿瘤免疫疗法。”黄波表示。
据悉,该研究得到了国家自然科学基金基础科学项目和中国医学科学院医学与健康科技创新工程的资助。
相关论文信息:
https://doi.org/10.1038/s41590-020-00850-9
https://blog.sciencenet.cn/blog-3423233-1266887.html
上一篇:美国休斯敦卫理公会医院杨静研究团队揭示肥胖促进多发性骨髓瘤发生发展的新机制
下一篇:刘聪/李丹前瞻性综述多级化学调控决定神经退行性疾病中致病蛋白聚集多态性